2019年初中化学常见题型知识点专练 29 计算题
试卷更新日期:2019-05-22 类型:二轮复习
一、计算题
-
1. 某纯碱样品中含有少量NaCl,小丽同学取该样品23g全部溶解于150g水中,再逐滴加入160g稀盐酸,反应中产生的气体的质量与盐酸的用量关系如图所示。(提示:相关反应为Na2CO3+2HCl=2NaCl+H2O+CO2↑)计算当恰好完全反应时:
 (1)、产生的二氧化碳的质量是克。(2)、此时所得到的溶液中溶质的质量分数(写出必要的计算过程,结果保留到0.1%)。2. 某化学兴趣小组对粉体中碳酸钙含量进行了探究:小组成员从一包粉体产品中取出样品5.10g放入烧杯中,并逐滴加入相同浓度的稀盐酸(假设样品中的杂质不与盐酸反应),实验测得烧杯中物质总质量与加入稀盐酸的总质量关系如下表所示:
(1)、产生的二氧化碳的质量是克。(2)、此时所得到的溶液中溶质的质量分数(写出必要的计算过程,结果保留到0.1%)。2. 某化学兴趣小组对粉体中碳酸钙含量进行了探究:小组成员从一包粉体产品中取出样品5.10g放入烧杯中,并逐滴加入相同浓度的稀盐酸(假设样品中的杂质不与盐酸反应),实验测得烧杯中物质总质量与加入稀盐酸的总质量关系如下表所示:稀盐酸的总质量(g)
10.00
20.00
30.00
40.00
50.00
60.00
70.00
烧杯中物质总质量(g)
14.66
24.22
m
43.34
52.90
62.90
72.90
(1)、上表中m=。(2)、求样品中碳酸钙的质量分数(结果保留两位小数)。3. 某化工厂新进一批工业用盐,该工业用盐的主要成分为氯化钠,杂质为氯化钡。为测定其中氧化钠的质量分数做如下实验:取20.8g该工业盐加入足量水使其全部溶解,向溶液中逐滴加入溶质质量分数为14.2%的硫酸钠溶液至恰好完全反应,得到沉淀2.33g。请根据实验计算:(1)、加入硫酸钠溶液的质量为多少克?(2)、该工业盐中氯化钠的质量分数为多少?4. 已知:Cu与稀硫酸(H2SO4)不反应,Zn+H2SO4=ZnSO4+H2↑。某同学将20g黄铜(铜和锌的混合物)放入烧杯中,向烧杯中滴加稀硫酸至过量,实验测得加入稀硫酸的质量与产生氢气质量的关系如下图所示。请计算: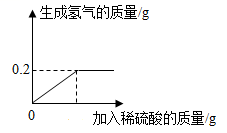 (1)、恰好完全反应时生成氢气的质量是多少g;(2)、该黄铜中锌的质量分数是多少?(3)、若恰好完全反应时加入稀硫酸的质量为100g,则恰好完全反应时烧杯内物质的质量为多少g。5. 取Cu-Zn合金10g,放入烧杯中,再向其中加入50g稀盐酸恰好完全反应后,测得烧杯内剩余物质的质量共为59.8g。(1)、生成氢气的质量。(2)、求该合金中铜的质量分数。6. 波尔多液是一种运用广泛的农药,由熟石灰和硫酸铜配制而成.某工厂用以下反应2Cu+O2+2H2SO4=2CuSO4+2H2O来生产硫酸铜.现有128kg纯铜。
(1)、恰好完全反应时生成氢气的质量是多少g;(2)、该黄铜中锌的质量分数是多少?(3)、若恰好完全反应时加入稀硫酸的质量为100g,则恰好完全反应时烧杯内物质的质量为多少g。5. 取Cu-Zn合金10g,放入烧杯中,再向其中加入50g稀盐酸恰好完全反应后,测得烧杯内剩余物质的质量共为59.8g。(1)、生成氢气的质量。(2)、求该合金中铜的质量分数。6. 波尔多液是一种运用广泛的农药,由熟石灰和硫酸铜配制而成.某工厂用以下反应2Cu+O2+2H2SO4=2CuSO4+2H2O来生产硫酸铜.现有128kg纯铜。试计算:
(1)、需要溶质质量分数为10%的稀硫酸溶液的质量.(2)、充分反应后所得溶液中溶质质量分数.(结果保留一位小数)7. 向100g溶质质量分数为14.6%的稀盐酸溶液,加入一定质量的Na2CO3溶液,充分反应后 得到仍含HCl质量分数3.65%的混合溶液200g。(1)、参加反应的HCl质量为g;(2)、所加入Na2CO3溶液的溶质质量分数为?(写出计算过程,结果保留0.1%)(3)、若要使反应后的混合溶液中HCl质量分数恢复到14.6%,需要向混合溶液中通入并溶解HCl气体g(结果保留0.1g)。8. 鸡蛋壳的主要成分是碳酸钙。为了测定某鸡蛋壳中碳酸钙的质量分数,小军同学进行了如下实验:将鸡蛋壳洗净、干燥并捣碎后,与足量稀盐酸在烧杯中反应(假设鸡蛋壳中杂质不与稀盐酸反应)。
有关实验数据如表:
反应前
反应后
实验
数据
稀盐酸的质量
鸡蛋壳的质量
剩余物的质量
100g
12g
108.7g
(1)、根据质量守恒定律可知,反应中产生二氧化碳气体g。(2)、计算该鸡蛋壳中碳酸钙的质量。