2019年初中化学知识点专练 21 溶液
试卷更新日期:2019-05-22 类型:二轮复习
一、填空题
-
1. 将30g甲、乙两种物质在t2℃时分别放入100g水中,充分溶解如图所示。试回答:

 (1)、A试管中放的物质是(填“甲”或“乙”),此时另一支试管中的溶液是(填“饱和”或“不饱和”),该溶液中溶质质量分数是(保留1位小数),若将温度降至t1℃时,试管B中的现象是。(2)、在t2℃时,若要让试管A中的固体全部溶解,可向烧杯的水中加入(填序号)。
(1)、A试管中放的物质是(填“甲”或“乙”),此时另一支试管中的溶液是(填“饱和”或“不饱和”),该溶液中溶质质量分数是(保留1位小数),若将温度降至t1℃时,试管B中的现象是。(2)、在t2℃时,若要让试管A中的固体全部溶解,可向烧杯的水中加入(填序号)。①硝酸铵 ②氢氧化钠 ③氯化钠
2. 氯化钠在工农业上具有广泛的用途。(1)、配制500mL质量分数6%的氯化钠溶液(密度1.04g/cm3),需要氯化钠的质量为g。(2)、用托盘天平称量所需氯化钠,托盘天平调节平衡后,接下来的操作顺序是___。A、先在左盘纸片上加氯化钠,后在右盘纸片上加砝码和移动游码 B、先在右盘纸片上加砝码和移动游码,后在左盘纸片上加氯化钠(3)、若用质量分数为6%的氯化钠溶液配制100g质量分数为4%的氯化钠溶液。①需要6%的氯化钠溶液的质量为g(精确到0.1g)。
②该溶液配制过程中除用到量筒、玻璃棒和胶头滴管外,还需要的玻璃仪器是。
3. 甲和乙两种固体物质的溶解度曲线如上图所示。℃时,甲和乙的溶解度相等;若使一定质量接近饱和的物质甲的溶液变为饱和溶液,可采用的方法是(写一种即可);将t2℃时70g甲物质的饱和溶液溶质质量分数稀释为10%,需加水 g。 4. 根据下表回答相关问题。
4. 根据下表回答相关问题。温度(℃)
0
20
40
50
60
80
100
溶解度
(g/100g 水)
KNO3
13.3
31.6
63.9
86.0
110.0
169.0
246.0
NaCl
35.7
36.0
36.6
37.0
37.3
38.4
39.8
①20℃时两种物质溶解度的关系是 KNO3NaCl(填“>”或“=”或“<”)。
②除去硝酸钾溶液中含有少量氯化钠的方法是。
③配制 200g0.9%的生理盐水,需要称取氯化钠固体g。
④60℃时,50g 水中溶解 43g 硝酸钾形成不饱和溶液,欲使该溶液恰好达到饱和,可以恒温蒸发水的质量g(精确到 0.1);当其它条件不变时,也可以降温到℃恰好饱和。
5. 试管 a、b 中分别放入等质量的甲和乙,再分别加入等质量的水(析出固体不含结晶水)。
①t1℃ 时,甲的溶解度乙的溶解度(用“>”“<”“=”填空)。
②p 点的含义是。
③图 2,a 中加入的物质是(填“甲”或“乙”);
④t3℃ 时,若将 25g 甲物质加入到 50g 水中,充分溶解后得到溶液质量为。
⑤关于图 2 说法中正确的是。
A t1℃ 时 a 和 b 中溶剂质量相等
B t2℃ 时 a 和 b 均为不饱和溶液
C t3℃ 时 a 中溶质质量分数大于 b 中溶质质量分数
D t3℃ 时若使 a 和 b 均恰好饱和,a 中加入对应溶质质量大于 b 中加入对应溶质质量
6. 甲和乙的溶解度曲线如图所示,请回答:
①图中a点的含义是 , 10℃时两物质中溶解度较大的是;
②当乙中含有少量甲时,可采用的方法提纯乙;
③某同学将甲乙固体各30克分别加入100克水中后,进行了如下图所示的实验:

则上述实验中m的取值范围为;
④40℃时,取等质量的甲乙两种物质的饱和溶液分别蒸发等量的水后,恢复到40℃,下列说法正确的是(填字母)。
A.恢复到原温度后,溶液中溶剂的质量:甲=乙
B.恢复到原温度后,析出晶体的质量:乙>甲
C.若再降温到20℃时,溶液的质量:甲>乙
D.若再降温到20℃时,溶液的溶质质量分数甲乙
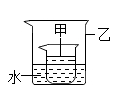
7. 如图是甲、乙、丙三种固体物质的溶解度曲线。t1℃时,甲、丙两种物质的饱和溶液中溶质的质量分数(填相等或不相等);t2℃时,分别溶解等质量的这三种固体,将它们配制成饱和溶液,所得溶液的质量最大的是;甲的饱和溶液中含有少量的丙,要从中获得较纯的甲,可采用的方法为。 8. T1℃时,将等质量的硝酸钾和氯化钾分别加入到各盛有100g水的两个烧杯中,充分搅拌后观象如图一所示。硝酸钾和氯化钾的溶解变曲线如图二所示。下列说法正确的是
8. T1℃时,将等质量的硝酸钾和氯化钾分别加入到各盛有100g水的两个烧杯中,充分搅拌后观象如图一所示。硝酸钾和氯化钾的溶解变曲线如图二所示。下列说法正确的是
A.烧杯乙中上层清液是不饱和溶液
B.烧杯甲中溶解的溶质是氯化钾
C.烧杯甲溶液中溶质的质量分数等于烧杯乙溶液中溶质的质量分数
D.将温度由T1℃开高到T2℃,充分提拌,烧杯乙中固体
9. 硝酸钾的部分溶解度数据见下表。温度(℃)
10
20
40
60
溶解度(g/100g 水)
20.9
31.6
63.9
110
 (1)、20℃时,称取 10.0 克硝酸钾固体加入到 40 克水中,用(写出仪器名称)搅拌,充分溶解后得到(选填“饱和”或“不饱和”)溶液。(2)、将上述溶液升温至 60℃,所得溶液的溶质质量分数为。(3)、将 60℃的硝酸钾溶液进行如图所示操作。
(1)、20℃时,称取 10.0 克硝酸钾固体加入到 40 克水中,用(写出仪器名称)搅拌,充分溶解后得到(选填“饱和”或“不饱和”)溶液。(2)、将上述溶液升温至 60℃,所得溶液的溶质质量分数为。(3)、将 60℃的硝酸钾溶液进行如图所示操作。将溶液 I 降温,开始析出硝酸钾晶体的温度介于_____℃(选填编号之间。
A、40-60 B、20-40 C、10-20 D、低于 10(4)、为得到 60℃时硝酸钾饱和溶液,将溶液 II 恒温蒸发 15 克水,请分析该操作能否达到实验目的并说明理由。10. 如图是A,B,C 三种物质的溶解度曲线,回答下列问题:
①A、B 两种物质在℃时溶解度相同。
②t2℃时,B 物质的溶解度是。
③t2℃时,等质量的三种饱和溶液中溶剂质量最少的是。
④t2℃时,将三种物质各 ag 分别加入到 100g 水中,充分溶解后,若只有一种物质能形成饱和溶液,则a的取值范围是。(用“ > ”、“ < ”、“ ≤”、“ ≥”、“ = ”表示)
⑤A中混有少量 B,要得到较纯净的A,可采取的方法是。
⑥A的不饱和溶液变成饱和,可采用的方法是。(写一种)
⑦如图烧杯甲中盛有饱和的C溶液。现向烧杯乙中加入生石灰后,烧杯甲中有晶体析出,可能的原因是。
⑧t2℃时,将三种物质的饱和溶液各100g,分别加热蒸发10g水后,再恢复到 t2℃,剩余溶液的质量由大到小的顺序是 , 此时A的溶质质量分数是。(列式即可)
11. 依据下列20℃时的实验和数据回答问题。已知20℃时,NaCl和NaNO3的溶解度分别为36g和88g.
 (1)、①~⑤所得溶液属于饱和溶液的是。(2)、下列关于①~⑤所得溶液的说法错误的是______________________。A、溶质质量:①<② B、溶液质量:②<④ C、溶质质量分数:①=③ D、⑤中溶质与溶剂的质量比为9:1012. 氯化钠的部分溶解度如下:
(1)、①~⑤所得溶液属于饱和溶液的是。(2)、下列关于①~⑤所得溶液的说法错误的是______________________。A、溶质质量:①<② B、溶液质量:②<④ C、溶质质量分数:①=③ D、⑤中溶质与溶剂的质量比为9:1012. 氯化钠的部分溶解度如下:温度(℃)
10℃
20℃
30℃
40℃
60℃
80℃
100℃
溶解度(g/100g水)
35.8
36.0
36.1
36.4
37.1
38.0
39.2
①80℃氯化钠的溶解度是g/100g水。
②20℃时,15g水中溶解g氯化钠刚好形成饱和溶液。
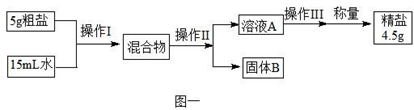
③粗盐(含有泥沙的氯化钠)提纯的实验过程如图一所示,溶液A是溶液(选填“饱和”或“不饱和”);操作Ⅱ是。
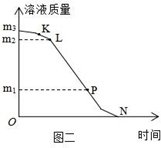
④操作Ⅲ过程中溶液质量与时间变化关系示意图如图二所示,相关分析正确的是(选填编号)
a.m3=20g
b.L、P表示的溶液,溶质质量分数相同
c.(m2-m1)是减少的水的质量
d.N点时,停止加热