湖南省邵阳市2018-2019学年中考化学二模考试试卷
试卷更新日期:2019-05-06 类型:中考模拟
一、单选题
-
1. 下来变化中属于化学变化的是( )A、蜡烛燃烧 B、汽车爆胎 C、蔬菜榨汁 D、玻璃破碎2. 节日期间的商场里顾客很多,有人会感觉到闷热缺氧,测定出氧气的体积分数可能是( )A、1% B、19% C、25% D、78%3. 在野外游玩禁止乱扔烟头,以防发生火灾。你认为烟头引起火灾的主要原因是( )。A、提供氧气 B、改变可燃物的着火点 C、提供可燃物 D、使可燃物的温度达到着火点4. 下列图标的实验操作正确的是( )A、氧气验满
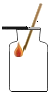 B、取用药品
B、取用药品 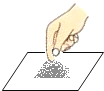 C、称取NaCl
C、称取NaCl 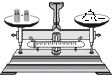 D、稀释浓硫酸
D、稀释浓硫酸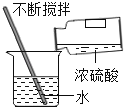 5. 下列有关说法符合科学事实的是( )A、通过炼丹发明长生不老药 B、通过“点石成金”使贱金属变成贵黄金 C、纯净的水中不含任何物质 D、金刚石在空气里高温加热后消失了6. 对下列一些事实的解释错误的是( )
5. 下列有关说法符合科学事实的是( )A、通过炼丹发明长生不老药 B、通过“点石成金”使贱金属变成贵黄金 C、纯净的水中不含任何物质 D、金刚石在空气里高温加热后消失了6. 对下列一些事实的解释错误的是( )事 实
解 释
A
墙内开花墙外香
分子在不断地运动
B
H2O2能杀菌消毒,而H2O不能
两种物质的分子构成不同
C
温度计中的水银热胀冷缩
原子的大小发生改变
D
50mL水与50mL酒精混合后总体积小于100mL
分子间有间隔
A、A B、B C、C D、D7. 下图是电解水反应的示意图。该图说明了( )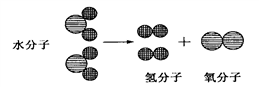 A、水分子是由氢分子和氧分子构成的 B、水分子在化学反应中不能再分 C、化学变化的本质是原子重新组合的过程 D、分子是化学变化中的最小粒子8. 下列叙述错误的是()A、原子是不能再分的最小粒子 B、碳还原氧化铜的反应属于置换反应 C、混合物中也可能只含有一种元素 D、中和反应一定属于复分解反应9. 下列实验操作、现象和结论对应正确的是( )
A、水分子是由氢分子和氧分子构成的 B、水分子在化学反应中不能再分 C、化学变化的本质是原子重新组合的过程 D、分子是化学变化中的最小粒子8. 下列叙述错误的是()A、原子是不能再分的最小粒子 B、碳还原氧化铜的反应属于置换反应 C、混合物中也可能只含有一种元素 D、中和反应一定属于复分解反应9. 下列实验操作、现象和结论对应正确的是( )实验操作
现象
结论
A
向久置于空气中的NaOH溶液滴加稀H2SO4
有气泡产生
NaOH和H2SO4发生了化学反应
B
向某溶液中滴加BaCl2溶液
有白色沉淀
原溶液含有SO42﹣
C
向集满CO2的软塑料瓶中加入约 体积滴有石蕊试液的水,旋紧瓶盖,振荡
塑料瓶变瘪,
溶液变红
CO2能与石蕊反应
D
将质量相同的Mg、Zn分别投入到足量的稀HCl中
镁条表面产生气体更多、更快
金属活动性:Mg>Zn
A、A B、B C、C D、D10. 在化学反应aC2H6+bO2=mCO2+nH2O中,各化学式系数之间的关系正确的是()A、a=3m B、m=2a C、3n=a D、2b=m+n11. 化学与生活息息相关,下列有关的说法中错误的是( )A、用点燃闻气味的方法区分羊毛制品和化纤制品 B、利用厨房中的食盐除去水壶中的水垢 C、可利用硝酸铵制作简易冰袋 D、碳酸氢钠俗称小苏打,是焙制糕点所用的发酵粉的主要成分之一12. 下列有关的叙述正确的是( )A、硝酸铵(NH4NO3)中氮元素的化合价为﹣3价 B、在原子里质子数等于中子数 C、氢气中氢元素的化合价为+1价 D、在化学变化中,原子不能再分,它是化学变化中的最小粒子13. 有关实验操作正确的是()A、加热蒸发皿时垫上石棉网 B、将氢氧化钠固体放入烧杯中称量 C、在量筒中溶解氯化钠固体 D、将pH试纸浸入待测液中测定pH14. 蔗糖是储藏在甘蔗、甜菜中的糖,其化学式为C12H22O11 . 下列有关蔗糖的叙述中,正确的是()A、蔗糖中碳元素的质量分数为40% B、蔗糖中碳、氢、氧原子的个数比是12:22:11 C、蔗糖分子中碳、氢、氧元素的质量比是1:2:1 D、蔗糖的相对分子质量为18015. 学校食堂提供了下列5种食物:
小亮为自己安排的午餐食谱中,较合理的是( )
A、①②③ B、①③⑤ C、①④⑤ D、③④⑤16. 在一密闭容器中有X、Y、Z、W四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表所示。下列说法中正确的是()物质
X
Y
Z
W
反应前的质量/g
8
10
1
21
反应后的质量/g
0
21
待测
9
A、反应后Z的质量为9g B、反应中Y与W发生改变的质量比为1:1 C、反应生成Y的质量为11g D、Z在该反应中作催化剂17. 已知R2﹣核外有18个电子,则R的质子数为( )A、18 B、16 C、20 D、不能确定18. 下列有关灭火原理的说法中,错误的是( )A、清除可燃物 B、使可燃物与其他物品隔离 C、隔绝空气 D、降低可燃物的着火点19. 下列关于物质用途的描述错误的是()A、氧气可用作燃料 B、二氧化碳可用作气体肥料 C、干冰可用于人工降雨 D、铜丝可用作导线20. 在点燃条件下,A和B反应生成C和D,反应前后分子变化的微观示意图如图所示,下列判断错误的是()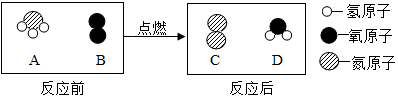 A、该反应中有两种化合物分子 B、该反应中,参加反应的 A、 B分子的个数比为4:3 C、物质C的化学性质不活泼,常用作保护气 D、在该反应中,生成C和D的质量比为14:921. 下列反应既属于氧化反应,又属于化合反应的是( )A、 氧化汞
A、该反应中有两种化合物分子 B、该反应中,参加反应的 A、 B分子的个数比为4:3 C、物质C的化学性质不活泼,常用作保护气 D、在该反应中,生成C和D的质量比为14:921. 下列反应既属于氧化反应,又属于化合反应的是( )A、 氧化汞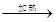 汞+氧气
B、 乙炔+氧气
汞+氧气
B、 乙炔+氧气 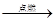 二氧化碳+水
C、 一氧化碳+氧气
二氧化碳+水
C、 一氧化碳+氧气  二氧化碳
D、 水
二氧化碳
D、 水  氢气+氧气
22. 生活中的下列做法,你认为正确的是( )A、用氢氧化钠的稀溶液治疗胃酸过多 B、用碳酸氢钠做焙制糕点的发酵粉 C、用聚氯乙烯来包装食品 D、住宅发生火灾时应马上打开窗户散热降温23. 现有等质量甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中化合价均为+2价)。则下列说法中错误的是()
氢气+氧气
22. 生活中的下列做法,你认为正确的是( )A、用氢氧化钠的稀溶液治疗胃酸过多 B、用碳酸氢钠做焙制糕点的发酵粉 C、用聚氯乙烯来包装食品 D、住宅发生火灾时应马上打开窗户散热降温23. 现有等质量甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中化合价均为+2价)。则下列说法中错误的是()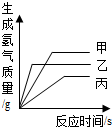 A、生成氢气的质量:甲 乙 丙 B、相对原子质量:乙 丙 甲 C、金属活动性:乙 甲 丙 D、消耗硫酸的质量:甲 乙 丙24. 下列关于物质鉴别和提纯的方法正确的是()A、用水鉴别白色粉末硫酸铜和硫酸钠 B、用通过铜网的方法除去CO2中混有的少量O2 C、用高温加热的方法除去C粉中的CuO D、用稀盐酸鉴别碳酸钠和碳酸钙粉末25. 七星岩的岩石主要成分是碳酸钙,取一块岩石样品测其含碳酸钙75%,则该岩石样品含钙(设其它成分不含钙)的质量分数为( )A、25% B、30% C、40% D、75%
A、生成氢气的质量:甲 乙 丙 B、相对原子质量:乙 丙 甲 C、金属活动性:乙 甲 丙 D、消耗硫酸的质量:甲 乙 丙24. 下列关于物质鉴别和提纯的方法正确的是()A、用水鉴别白色粉末硫酸铜和硫酸钠 B、用通过铜网的方法除去CO2中混有的少量O2 C、用高温加热的方法除去C粉中的CuO D、用稀盐酸鉴别碳酸钠和碳酸钙粉末25. 七星岩的岩石主要成分是碳酸钙,取一块岩石样品测其含碳酸钙75%,则该岩石样品含钙(设其它成分不含钙)的质量分数为( )A、25% B、30% C、40% D、75%二、填空题
-
26. 用数字和化学符号表示:(1)、2个亚铁离子;(2)、3个铵根离子;(3)、保持氮气化学性质的最小微粒;(4)、碳酸钠中碳元素的化合价为+4价;(5)、铯(Cs)原子的结构示意图为
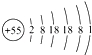 ,铯原子在化学反应中易形成铯离子; (6)、+6价硫元素的氧化物的化学式。27. 人们日常生活与化学密切相关。(1)、汽车燃烧的汽油和做饭燃烧的天然气等均为化石燃料产品。化石燃料属(填“可再生”或“不可再生”)能源。(2)、雨后晴天的空气清新洁净,此时的空气属于(填“纯净物”或“混合物”)。(3)、下列着火的应急处理不合理的是(填序号)。
,铯原子在化学反应中易形成铯离子; (6)、+6价硫元素的氧化物的化学式。27. 人们日常生活与化学密切相关。(1)、汽车燃烧的汽油和做饭燃烧的天然气等均为化石燃料产品。化石燃料属(填“可再生”或“不可再生”)能源。(2)、雨后晴天的空气清新洁净,此时的空气属于(填“纯净物”或“混合物”)。(3)、下列着火的应急处理不合理的是(填序号)。① 实验室燃着的酒精灯被碰倒着火,立即用湿毛巾盖灭
② 油在炒菜锅内因温度过高着火,立即向锅内倒入冷水灭火
③ 电器着火时,立即断电,再用干粉灭火器灭火
28. 如图中A,B,C,D是四种粒子的结构示意图,E是银元素在元素周期表中的信息.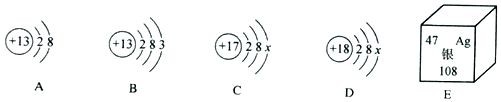
请回答下列问题:
(1)、图中A,B,C,D粒子共表示种元素.(2)、D中x= .(3)、E中银元素原子的质子数为 , 一个银原子质量是一个碳﹣12原子质量的倍.(4)、写出A中的粒子符号: .三、简答题
-
29. a、b、c三种固体物质的溶解度曲线如图所示:
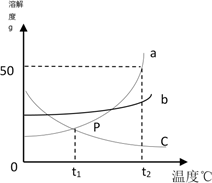 (1)、P点表示。(2)、将接近饱和的c溶液变为饱和溶液,可采用的方法(写出一种)。(3)、t2℃时,将30g的a物质加入到50g水中充分搅拌,所得溶液质量为g。30. 铁是生产、生活中应用最广泛的金属,答下列有关铁的问题.(1)、铁锅用于烹饪食物,利用铁具有良好的性.(2)、铁制品易生锈,原因是铁易与反应的结果.(3)、用稀硫酸故除去铁钉上的铁锈(主要成分是Fe2O3),以重新使用.请用化学方程式表示除锈的化学原理:。(4)、铁制品进行“烤蓝”处理后,其表面会形成致密的氧化膜可增强抗腐蚀性能.“烤蓝”的过程的化学原理为:36Fe+4NaNO2+9NaNO3+2H2O═12X+13NaOH+13NH3↑,反应中X的化学式为 .
(1)、P点表示。(2)、将接近饱和的c溶液变为饱和溶液,可采用的方法(写出一种)。(3)、t2℃时,将30g的a物质加入到50g水中充分搅拌,所得溶液质量为g。30. 铁是生产、生活中应用最广泛的金属,答下列有关铁的问题.(1)、铁锅用于烹饪食物,利用铁具有良好的性.(2)、铁制品易生锈,原因是铁易与反应的结果.(3)、用稀硫酸故除去铁钉上的铁锈(主要成分是Fe2O3),以重新使用.请用化学方程式表示除锈的化学原理:。(4)、铁制品进行“烤蓝”处理后,其表面会形成致密的氧化膜可增强抗腐蚀性能.“烤蓝”的过程的化学原理为:36Fe+4NaNO2+9NaNO3+2H2O═12X+13NaOH+13NH3↑,反应中X的化学式为 .四、流程题
-
31. 以焦炭和碳酸钙为原料生产碳化钙(CaC2),并制备重要工业原料乙炔(C2H2)气体,其工艺流程如下图:
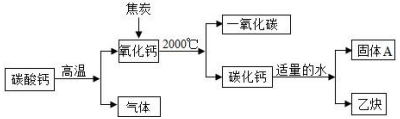 (1)、写出碳酸钙分解的化学方程式。(2)、将氧化钙和焦炭反应的化学方程式补充完整CaO+C®CaC2+CO ;生成的CO不能排放到空气中,是因为。(3)、猜想:固体 A 的成分可能是氢氧化钙或碳酸钙。
(1)、写出碳酸钙分解的化学方程式。(2)、将氧化钙和焦炭反应的化学方程式补充完整CaO+C®CaC2+CO ;生成的CO不能排放到空气中,是因为。(3)、猜想:固体 A 的成分可能是氢氧化钙或碳酸钙。设计实验证明猜想。
实验
现象
结论
固体A的成分不是碳酸钙
五、实验题
-
32. 以下是研究实验室制取氧气的装置图,请按要求回答下列问题.
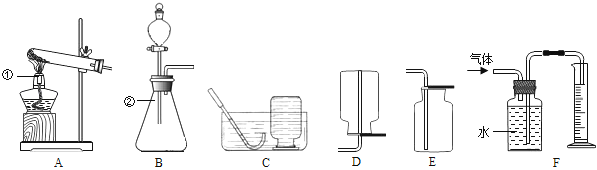 (1)、写出图中标号仪器的名称:①;② .(2)、实验室用高锰酸钾制取氧气,应选用的发生装置是(填字母序号,下同),若要收集一瓶干燥的氧气,应选择的收集装置是 .(3)、实验室用H2O2溶液和MnO2混合制氧气,其中MnO2起作用,该反应的化学方程式为 . 同学们利用B和F装置,通过排水量来测定生成氧气的体积,反应结束后,发现量筒内收集到的水的体积总是比理论值偏大(水的体积测量标准),其主要原因是 .33. 如图是小华配制NaCl溶液的实验操作示意图:
(1)、写出图中标号仪器的名称:①;② .(2)、实验室用高锰酸钾制取氧气,应选用的发生装置是(填字母序号,下同),若要收集一瓶干燥的氧气,应选择的收集装置是 .(3)、实验室用H2O2溶液和MnO2混合制氧气,其中MnO2起作用,该反应的化学方程式为 . 同学们利用B和F装置,通过排水量来测定生成氧气的体积,反应结束后,发现量筒内收集到的水的体积总是比理论值偏大(水的体积测量标准),其主要原因是 .33. 如图是小华配制NaCl溶液的实验操作示意图: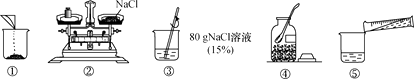 (1)、图中的玻璃仪器分别是、玻璃棒、广口瓶和量筒,其中玻璃棒在此操作中的作用是。(2)、指出图②中的一处错误操作。(3)、通过计算确定托盘天平左盘中固体氯化钠的质量为 , 需要水的质量是 , 配制时应选择(填“10”“50”或“100”)mL的量筒量取所需要的水。(4)、用图中的序号表示配制溶液的操作顺序。(5)、上述溶液取10 g加水40 g进行稀释,所得氯化钠溶液的溶质质量分数是。
(1)、图中的玻璃仪器分别是、玻璃棒、广口瓶和量筒,其中玻璃棒在此操作中的作用是。(2)、指出图②中的一处错误操作。(3)、通过计算确定托盘天平左盘中固体氯化钠的质量为 , 需要水的质量是 , 配制时应选择(填“10”“50”或“100”)mL的量筒量取所需要的水。(4)、用图中的序号表示配制溶液的操作顺序。(5)、上述溶液取10 g加水40 g进行稀释,所得氯化钠溶液的溶质质量分数是。六、计算题
-
34. 向147克稀硫酸中加入锌粉(仅含不容于酸的杂质),所加锌粉的质量与产生气体的质量关系如图所示。求:
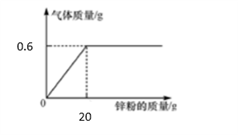 (1)、此过程中产生气体的最大质量是g。(2)、原稀硫酸中溶质的质量分数。(写出计算过程)
(1)、此过程中产生气体的最大质量是g。(2)、原稀硫酸中溶质的质量分数。(写出计算过程)
-