贵州省遵义市汇川区2018-2019学年中考化学一模考试试卷
试卷更新日期:2019-05-06 类型:中考模拟
一、单选题
-
1. 2018年世界环境日,中国的主题是“美丽中国,我是行动者”。下列做法符合主题的是()A、提倡焚烧秸秆增加土壤肥力 B、提倡开小车上班 C、提倡纸张两面使用 D、工厂废水直接排放2. 下列利用物质化学性质的是()A、金刚石用于切割玻璃 B、氢气做燃料 C、用水灭火 D、铁常用来制作炊具3. 某同学为探究氯化钠固体是否能与稀硫酸反应,以下有关操作错误的是()A、
 取氯化钠
B、
取氯化钠
B、 加入氯化钠颗粒
C、
加入氯化钠颗粒
C、 滴加稀硫酸
D、
滴加稀硫酸
D、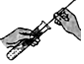 清洗试管
4. 关于硫酸和盐酸的说法错误的是()A、都属于酸类 B、两者的溶液都具有导电性 C、都可用于除铁锈 D、两者的pH一定相等5. 下列化学方程式书写正确,并与事实相符的是()A、甲烷 作燃料: B、铝的自我保护: C、酸雨的形成: D、铁桶不能盛放硫酸铜溶液的原因:6. 小金在做硫燃烧实验时,进行了如下操作:①在铺有细沙的燃烧匙里放入少量硫;②将燃烧匙在酒精灯火焰上加热,直至硫燃烧;③将燃烧匙伸入盛有氧气的集气瓶中(集气瓶内盛有滴加紫色石蕊试液的少量水)。实验中可观察到的现象与结论不符合的是()A、对比①和②可说明硫燃烧需要达到一定的温度 B、对比②和③中硫的燃烧现象说明氧气具有助燃性 C、在③中观察到紫色石蕊试液变红,说明硫燃烧是化学变化 D、在③中观察到紫色石蕊试液变红,说明硫燃烧产物是一种酸7. 如图是某种“加碘食盐”包装袋上的部分说明,下列说法正确的是()
清洗试管
4. 关于硫酸和盐酸的说法错误的是()A、都属于酸类 B、两者的溶液都具有导电性 C、都可用于除铁锈 D、两者的pH一定相等5. 下列化学方程式书写正确,并与事实相符的是()A、甲烷 作燃料: B、铝的自我保护: C、酸雨的形成: D、铁桶不能盛放硫酸铜溶液的原因:6. 小金在做硫燃烧实验时,进行了如下操作:①在铺有细沙的燃烧匙里放入少量硫;②将燃烧匙在酒精灯火焰上加热,直至硫燃烧;③将燃烧匙伸入盛有氧气的集气瓶中(集气瓶内盛有滴加紫色石蕊试液的少量水)。实验中可观察到的现象与结论不符合的是()A、对比①和②可说明硫燃烧需要达到一定的温度 B、对比②和③中硫的燃烧现象说明氧气具有助燃性 C、在③中观察到紫色石蕊试液变红,说明硫燃烧是化学变化 D、在③中观察到紫色石蕊试液变红,说明硫燃烧产物是一种酸7. 如图是某种“加碘食盐”包装袋上的部分说明,下列说法正确的是() A、“碘盐”属于化合物 B、人体缺“碘”是指缺碘分子 C、根据标签可预测 或氯化钠性质不稳定 D、1kg该碘盐中最多含 的氯化钠8. 15%的H2O2溶液在二氧化锰催化作用下会剧烈反应产生O2 . 实验室欲利用15%的H2O2溶液制取O2 , 则下列装置中,仪器选择和药品放置最合理的是( )
A、“碘盐”属于化合物 B、人体缺“碘”是指缺碘分子 C、根据标签可预测 或氯化钠性质不稳定 D、1kg该碘盐中最多含 的氯化钠8. 15%的H2O2溶液在二氧化锰催化作用下会剧烈反应产生O2 . 实验室欲利用15%的H2O2溶液制取O2 , 则下列装置中,仪器选择和药品放置最合理的是( )
A、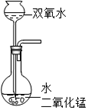 B、
B、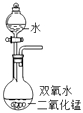 C、
C、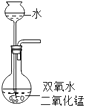 D、
D、 9. 下列实验方法展示了化学的学科价值,各组物质的鉴别方法与结论均正确的是()
9. 下列实验方法展示了化学的学科价值,各组物质的鉴别方法与结论均正确的是()选项
物质
方法与结论
A
硬水和软水
观察,若水中有不溶物即为硬水
B
氮气和二氧化碳
将燃着的木条伸入集气瓶中,熄灭的是二氧化碳
C
碳粉和氧化铜粉末
取样,分别滴加足量的稀硫酸,固体溶解的是氧化铜
D
食盐水与澄清石灰水
取样滴加无色酚酞,酚酞变红的是食盐水
A、A B、B C、C D、D10. 对大量的数据通过绘制分布图或曲线图进行处理,可发现其中的变化规律。下列图象正确的是()A、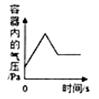 镁条在空气中燃烧
B、
镁条在空气中燃烧
B、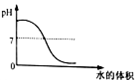 向一定量的氨水 能使紫石蕊试液变蓝 中不断加水
C、
向一定量的氨水 能使紫石蕊试液变蓝 中不断加水
C、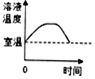 硝酸铵溶于水时溶液的温度变化
D、
硝酸铵溶于水时溶液的温度变化
D、 发生的反应为:
发生的反应为:
二、简答题
-
11. 遵义山清水秀、景色迷人,特色美食也遍布各地。(1)、虾子羊肉粉风味独特,清香扑鼻。从分子角度解释“清香扑鼻”的原因是。(2)、山盆柑橘汁多味美,齿颊生津。橘子皮还可以吸附室内异味,写出一种具有同样性质的化学物质的名称。(3)、湘江河中有许多鱼类,夏天鱼儿会跳出水面呼吸,原因是。(4)、绥阳红果树景区,形态各异的钟乳石、石笋令人惊叹,这是因为溶解在水中的碳酸氢钙 分解生成碳酸钙、二氧化碳、水的缘故,该反应的化学方程式为。12. 多角度对物质进行认识和研究,有利于合理使用物质。 对人类的生命活动非常重要:(1)、天然降水会遇到空气中的二氧化碳。因此正常雨水呈性 填“酸”、“碱”、“中” 。(2)、煤气的主要成分一氧化碳燃烧时会转化为二氧化碳,若用“
 ”表示碳原子,“ ”表示氧原子,请用模型表示该反应的微观过程。 (3)、大气中 含量的增加会加剧温室效应。下列反应中,对维持大气中 气体总量平衡至关重要的是 填序号 。(4)、科学家将 和 以一定比例混合,在一定条件下反应生成一种重要的化工原料和水,化学方程式: ,则X的化学式为。13. 空气是一种宝贵的自然资源。
”表示碳原子,“ ”表示氧原子,请用模型表示该反应的微观过程。 (3)、大气中 含量的增加会加剧温室效应。下列反应中,对维持大气中 气体总量平衡至关重要的是 填序号 。(4)、科学家将 和 以一定比例混合,在一定条件下反应生成一种重要的化工原料和水,化学方程式: ,则X的化学式为。13. 空气是一种宝贵的自然资源。图1
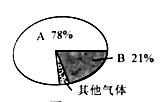 图2
图2 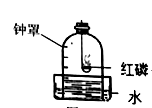 (1)、图1表示了空气的组成情况。保持A气体化学性质的微粒是 填化学符号 ;(2)、将浓硫酸敞口放置在空气中,溶液的溶质质量分数会变小,原因是。(3)、图2装置可以粗略地测定空气的组成。能作为氧气约占空气体积的 的实验证据是。(4)、工业上可利用分离液态空气的方法获得液氧,控制温度的范围在。 已知液氮的沸点为 ,液氧的沸点为 。(5)、下列有关空气污染的说法正确的是。
(1)、图1表示了空气的组成情况。保持A气体化学性质的微粒是 填化学符号 ;(2)、将浓硫酸敞口放置在空气中,溶液的溶质质量分数会变小,原因是。(3)、图2装置可以粗略地测定空气的组成。能作为氧气约占空气体积的 的实验证据是。(4)、工业上可利用分离液态空气的方法获得液氧,控制温度的范围在。 已知液氮的沸点为 ,液氧的沸点为 。(5)、下列有关空气污染的说法正确的是。A 防治大气污染应从污染源着手
B 二氧化碳也是空气污染物之一
C 煤燃烧产生的二氧化硫进入空气后可形成硫酸型酸雨
D 德国将自2030年起,在全欧停止使用以汽油等为燃料的汽车,这将减少空气污染
14. 宏观辨识和微观探析是认识物质及其变化的两种角度。据图回答下列问题。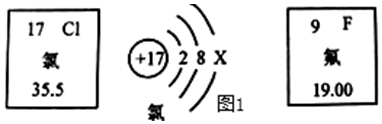 (1)、氯原子的相对原子质量为;通过计算可得 ,计算的理论依据是。(2)、可用浓盐酸和二氧化锰混合加热制取氯气,发生反应的化学方程式为 ,该变化中化合价降低的元素是 填符号 。(3)、氯气和氢气混合时,遇强光可能会发生爆炸,请写出该化合反应的化学方程式;研究发现,氟气也能和氢气剧烈反应生成氟化氢。氯气和氟气具有相似化学性质的原因是。(4)、氯气常用于自来水消毒,它溶于水发生反应的微观过程如图2:
(1)、氯原子的相对原子质量为;通过计算可得 ,计算的理论依据是。(2)、可用浓盐酸和二氧化锰混合加热制取氯气,发生反应的化学方程式为 ,该变化中化合价降低的元素是 填符号 。(3)、氯气和氢气混合时,遇强光可能会发生爆炸,请写出该化合反应的化学方程式;研究发现,氟气也能和氢气剧烈反应生成氟化氢。氯气和氟气具有相似化学性质的原因是。(4)、氯气常用于自来水消毒,它溶于水发生反应的微观过程如图2: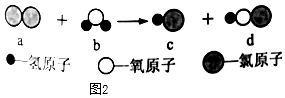
通过该变化获得的d物质具有强氧化性,有杀菌消毒的作用。变化中物质a和b的质量比为;分别向c和d的溶液中加入少量铁粉,均可观察到有气泡产生,请写出c溶液中发生反应的化学方程式 , 并从微粒的角度分析两种溶液中出现相同现象的本质原因。
15. 金属是一类重要的材料,在生产生活中有着广泛的用途。 (1)、地壳中含量最多的金属元素是 填元素名称 。(2)、金属铜常用来制导线,利用铜的延展性和性。铜制品长时间使用会生锈,铜锈的主要成分是 ,有同学认为铜生锈可能与 、 、 有关。他猜测的依据是。(3)、金属锰的性质与锌相似,利用如图装置探究Mn、Cu、Ag三种金属的活动性强弱时,装置中金属片和溶液中的溶质分别是______ 填字母序号 。A、Mn、Cu、 B、 、Ag、 C、Cu、Ag、(4)、《自然 杂志刊载“绿色炼铁”技术:电解熔融的氧化铁能得到铁和氧气,该反应与工业炼铁相比,具有的优点是。
(1)、地壳中含量最多的金属元素是 填元素名称 。(2)、金属铜常用来制导线,利用铜的延展性和性。铜制品长时间使用会生锈,铜锈的主要成分是 ,有同学认为铜生锈可能与 、 、 有关。他猜测的依据是。(3)、金属锰的性质与锌相似,利用如图装置探究Mn、Cu、Ag三种金属的活动性强弱时,装置中金属片和溶液中的溶质分别是______ 填字母序号 。A、Mn、Cu、 B、 、Ag、 C、Cu、Ag、(4)、《自然 杂志刊载“绿色炼铁”技术:电解熔融的氧化铁能得到铁和氧气,该反应与工业炼铁相比,具有的优点是。三、实验题
-
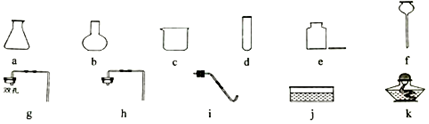
16. 如图中仪器j的名称是。实验室常用大理石和稀盐酸制取二氧化碳,制备并收集二氧化碳的装置应从如图选取的仪器是a、 填字母编号 。若利用足量的大理石和 的稀盐酸制取 的二氧化碳,至少取g的稀盐酸。有同学认为,用稀盐酸制得的二氧化碳可能会不纯净,她做出该猜想的依据是。
四、科学探究题
-
17. 小明取酸性锌锰干电池进行探究,他发现电池内部结构如图所示。
图1
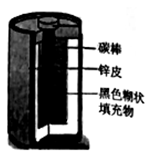
图2
(查阅资料)
①锌皮为金属锌 含有少量的铁 ;
②黑色糊状填充物由炭黑、 、 和 等组成;
③有关数据见表:
温度
0
20
40
60
80
100
溶解度
343
395
452
488
541
614
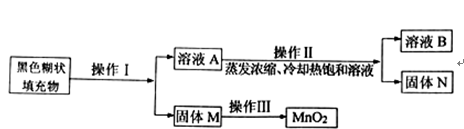
(1)、(实验探究一)小明取适量黑色糊状填充物,按如图2所示实验流程进行探究。操作I除溶解外,还需进行的操作是 , 操作Ⅱ中采用冷却热饱和溶液的方法提取N的原理是。
(2)、欲从固体M中得到较纯的 ,操作Ⅲ可采用的简便方法是。(3)、(实验探究二)小明取电池外壳锌皮,用砂纸打磨干净,剪成小块,进行实验。取一块锌皮放入盛有适量稀盐酸的烧杯中,有 生成。写出能生成氯化锌的另一个反应的化学方程式 必须与前一个反应有一种相同的反应物,写一个即可 。
(4)、若将 锌皮与足量稀硫酸完全反应,则生成氢气的质量 选填“ ”、“ ”或“ ”18. 是初中常用的一种试剂,它可以和很多物质反应。(1)、I. 中的阳离子是 , 高锰酸钾受热发生反应的化学方程式为。(2)、Ⅱ 经硫酸酸化的高锰酸钾溶液和草酸 溶液混合,发现刚开始反应时溶液褪色不明显,但不久后褪色速度突然加快。为了探究反应过程中褪色速度加快的原因,小明查到了如下资料:资料1:
资料2:通常情况下,反应物浓度变大,反应加快;温度升高,反应加快。
根据这些资料,小明提出了两个假设。
假设一:褪色速度突然加快是由反应物浓度变大引起的;
假设二:褪色速度突然加快是由反应过程中温度升高引起的。
小明经过分析,否定了假设一,理由是。
(3)、小丽针对假设二进行实验探究后,经过思考,又做了如下实验:把经硫酸酸化的高锰酸钾溶液等分为两份,分装A、B两试管,同时向两支试管中加入等量等浓度的草酸溶液,并置于同一水浴中。迅速向A试管中加入一定量的 发现A试管中溶液褪色明显快于B试管。上述实验中,把2支试管置于同一水浴中的目的是。这一实验基于的假设是。
-