安徽省安庆市2018-2019学年中考化学模拟考试试卷
试卷更新日期:2019-05-06 类型:中考模拟
一、单选题
-
1. 在安庆市人民路历史文化街区改造的过程中,一部分建筑修复用上了仿古砖。下列仿古砖制作工艺流程中发生化学变化的是()A、
 和泥
B、
和泥
B、 印坯
C、
印坯
C、 晒坯
D、
晒坯
D、 炉烧
2. “绿水青山就是金山银山”是建设生态文明的重要理念。下列说法不符合这一理念的是()A、乘电动公交车,提倡低碳出行 B、实施绿化工程,防治扬尘污染 C、增加烟囱高度,防止废气污染 D、回收废旧金属,节约金属资源3. 据报道,清华大学合成了原子级钴催化剂。钴元素的相关信息如图所示。下列有关钴的说法正确的是()
炉烧
2. “绿水青山就是金山银山”是建设生态文明的重要理念。下列说法不符合这一理念的是()A、乘电动公交车,提倡低碳出行 B、实施绿化工程,防治扬尘污染 C、增加烟囱高度,防止废气污染 D、回收废旧金属,节约金属资源3. 据报道,清华大学合成了原子级钴催化剂。钴元素的相关信息如图所示。下列有关钴的说法正确的是() A、相对原子质量为58.93g B、钴的元素符号为CO C、钴原子的核电荷数为27 D、钴原子的最外层电子数为274. 实验室用锌和稀硫酸制取氢气,下列操作正确的是()A、
A、相对原子质量为58.93g B、钴的元素符号为CO C、钴原子的核电荷数为27 D、钴原子的最外层电子数为274. 实验室用锌和稀硫酸制取氢气,下列操作正确的是()A、 稀释浓硫酸
B、
稀释浓硫酸
B、 加入锌粒
C、
加入锌粒
C、 产生的氢气
D、
产生的氢气
D、 收集氢气
5. 下列有关人体营养与健康的认识,错误的是()A、瘦肉和蛋清中都富含蛋白质 B、糖类和维生素都是为人体提供能量的主要物质 C、食用适量海带可预防缺碘性疾病 D、食用甲醛浸泡过的海产品,会危害人体健康6. 将知识归纳是学习化学的重要方法,下列归纳正确的是()A、
收集氢气
5. 下列有关人体营养与健康的认识,错误的是()A、瘦肉和蛋清中都富含蛋白质 B、糖类和维生素都是为人体提供能量的主要物质 C、食用适量海带可预防缺碘性疾病 D、食用甲醛浸泡过的海产品,会危害人体健康6. 将知识归纳是学习化学的重要方法,下列归纳正确的是()A、 溶液的特征
B、
溶液的特征
B、 含钙物质的转化
C、
含钙物质的转化
C、 物质的分类
D、
物质的分类
D、 盐的化学性质
7. 某化工企业生产钛的主要原料为钛酸亚铁(FeTiO3),下列说法正确的是()A、钛酸亚铁由两种金属和一种非金属组成 B、钛酸亚铁是有机化合物 C、钛酸亚铁由铁、钛、氧三种原子构成 D、钛酸亚铁中钛、氧元素质量比为 1:18. 为制得太阳能燃料(合成气),科学家用镍基催化剂设计了如下转化过程。下列有关说法错误的是()
盐的化学性质
7. 某化工企业生产钛的主要原料为钛酸亚铁(FeTiO3),下列说法正确的是()A、钛酸亚铁由两种金属和一种非金属组成 B、钛酸亚铁是有机化合物 C、钛酸亚铁由铁、钛、氧三种原子构成 D、钛酸亚铁中钛、氧元素质量比为 1:18. 为制得太阳能燃料(合成气),科学家用镍基催化剂设计了如下转化过程。下列有关说法错误的是() A、反应①的化学方程式为 CH4+O2=CO2+H2O B、镍基催化剂在反应前后化学性质不变 C、太阳能燃料主要成分是CO和H2 D、上述反应前后元素种类不变9. 对比实验是初中化学重要的实验方法,下列实验设计不合理的是()A、
A、反应①的化学方程式为 CH4+O2=CO2+H2O B、镍基催化剂在反应前后化学性质不变 C、太阳能燃料主要成分是CO和H2 D、上述反应前后元素种类不变9. 对比实验是初中化学重要的实验方法,下列实验设计不合理的是()A、 探究温度对分子运动快慢的影响
B、
探究温度对分子运动快慢的影响
B、 探究人呼出气体与空气中 CO2 的含量
C、
探究人呼出气体与空气中 CO2 的含量
C、 探究影响物质溶解性的因素
D、
探究影响物质溶解性的因素
D、 探究铁、银的活动性强弱
10. 小明将未经砂纸打磨的铝条放入盛有稀盐酸的密闭容器中,用压强传感器测得容器内压强和反应时间的变化曲线如图所示,下列分析正确的是()
探究铁、银的活动性强弱
10. 小明将未经砂纸打磨的铝条放入盛有稀盐酸的密闭容器中,用压强传感器测得容器内压强和反应时间的变化曲线如图所示,下列分析正确的是()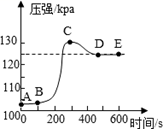 A、AB段表示铝与盐酸反应 B、CD段压强变化的主要影响因素是温度 C、C点生成的氢气质量大于D点 D、D点处反应刚好结束
A、AB段表示铝与盐酸反应 B、CD段压强变化的主要影响因素是温度 C、C点生成的氢气质量大于D点 D、D点处反应刚好结束二、填空题
-
11. 我国高铁、航空航天、手机制造等都已经跻身世界一流水平,根据下列材料的应用回答问题。
应用
“复兴号”高铁车轮
“鲲龙”水陆两栖飞机零部件
华为折叠手机屏幕
用到的材料
高速钢
钛合金、铝合金
聚酰亚胺塑料
(1)、上述材料中属于有机合成材料的是 , 属于金属材料的是(写一种即可)。(2)、飞机外壳用钛合金、铝合金的优点是。(3)、在对高铁钢轨中的缝隙进行焊接时,常用铝和氧化铁在高温条件下反应生成熔融状态下的铁和另一种氧化物。该反应的化学方程式为 , 反应基本类型是。三、实验题
-
12. 请根据下列装置回答问题。
 (1)、写出图中标号①的仪器名称。(2)、实验室用高锰酸钾制氧气的化学方程式为 , 选择的发生装置是(填装置序号,下同),若要收集一瓶供铁丝燃烧实验用的氧气,最适宜选择收集装置是。(3)、小组同学为了研究用向上排空气法和排水法收集的氧气浓度是否有差异,做了如下实验:加热高锰酸钾固体,分别用两种方法各收集三瓶氧气,并使用传感器测定收集到的氧气浓度,数据见表。
(1)、写出图中标号①的仪器名称。(2)、实验室用高锰酸钾制氧气的化学方程式为 , 选择的发生装置是(填装置序号,下同),若要收集一瓶供铁丝燃烧实验用的氧气,最适宜选择收集装置是。(3)、小组同学为了研究用向上排空气法和排水法收集的氧气浓度是否有差异,做了如下实验:加热高锰酸钾固体,分别用两种方法各收集三瓶氧气,并使用传感器测定收集到的氧气浓度,数据见表。收集方法
向上排空气法
排水法
氧气浓度/%
79.6
79.7
79.9
90.0
89.8
89.3
氧气平均浓度/%
79.7
89.7
①用向上排空气法收集氧气时,以能使放置在集气瓶瓶口的带火星木条复燃为氧气集满的标准;用排水法收集氧气时,以观察到为氧气集满的标准;
②向上排空气法收集到的氧气浓度只有80%左右,下列说法错误的是填字母序号)。
a.氧气的密度略大于空气的密度,无法将空气排尽
b.加热高锰酸钾固体产生氧气的浓度只有80%左右
c.当观察到带火星木条复燃时,集气瓶内还有剩余空气
四、流程题
-
13. 中国芯彰显中国“智”造,芯片的基材主要是高纯硅(Si),下图是某种制备高纯硅的工艺流程图:
 (1)、地壳中硅元素的含量比铝(填“高”或“低”),二氧化硅中硅元素化合价为。(2)、反应Ⅱ的化学方程式为 , 该反应要在无氧环境中进行,原因是(答出一种即可)。(3)、操作Ⅰ的名称是 , 所得粗硅应充分洗涤,以除去表面可能含有的盐酸、(填化学式)。
(1)、地壳中硅元素的含量比铝(填“高”或“低”),二氧化硅中硅元素化合价为。(2)、反应Ⅱ的化学方程式为 , 该反应要在无氧环境中进行,原因是(答出一种即可)。(3)、操作Ⅰ的名称是 , 所得粗硅应充分洗涤,以除去表面可能含有的盐酸、(填化学式)。五、简答题
-
14. 在学完酸碱盐的知识后,某兴趣小组开展了如下的探究,请回答相关问题。(1)、向石灰乳中加入一定量的稀盐酸,得到了澄清溶液,写出发生反应的化学方程式:。已知氯化钙溶液显中性,现用pH计测得反应后的溶液的pH=4.3,则此时溶液里的粒子示意图正确的是(填字母序号)。
 (2)、已知常温下氢氧化钙的溶解度为0.17g。若将石灰乳静置一段时间,则得到的上层澄清液体的溶质质量分数为(精确到0.01%)。(3)、向石灰石中加入稀硫酸,发现反应缓慢,如何提高该反应速率呢?
(2)、已知常温下氢氧化钙的溶解度为0.17g。若将石灰乳静置一段时间,则得到的上层澄清液体的溶质质量分数为(精确到0.01%)。(3)、向石灰石中加入稀硫酸,发现反应缓慢,如何提高该反应速率呢?查阅资料:石灰石与稀硫酸反应生成CaSO4 , 同时产生CO2气体;且CaSO4微溶于水。
Ⅰ.甲同学认为可以用增大稀硫酸浓度的方法来提高该反应速率。取相同质量相同规格的石灰石进行了如下实验:
实验
①10%硫酸溶液
②20%硫酸溶液
③40%硫酸溶液
观察1分钟内石灰石表面的气泡放出快慢
缓慢
明显加快
开始很快、又迅速变慢
由上述实验现象可知,增大稀硫酸的浓度(填“一定”或“不一定”)能提高该反应速率。请推测出现实验③中现象的原因:
Ⅱ.写出另外一种提高该反应速率方法:。
六、科学探究题
-
15. 化学兴趣小组用如下装置,进行有关碳及其氧化物的实验(图中夹持仪器已略去)。在完成气密性检查后加入药品,并已设法在玻璃管及试管中充满二氧化碳。
 (1)、完成实验,填好表格
(1)、完成实验,填好表格实验步骤
实验现象
实验分析
缓缓通入CO2 , 点燃A处酒精喷灯加热一段时间。
木炭粉减少,D中有气泡、石灰水变浑浊且。
A中发生反应的化学方程式为
。
点燃B处酒精灯加热一段时间。
B处玻璃管内固体变红。
说明一氧化碳具有。
(2)、C装置的作用是。(3)、小明同学又将木炭与氧化铜混合加热得到红色固体,为弄清这种红色固体的成分,进行了如下的探究:(查阅资料)Cu和Cu2O均为红色固体,且Cu2O+H2SO4=Cu+CuSO4+H2O。
(提出猜想)红色固体是:Ⅰ.Cu Ⅱ.Cu2O Ⅲ.。
(进行实验)
操作
现象
结论
取灼烧后的红色固体2.88g于试管中,加入足量稀硫酸充分反应
红色固体一定有Cu2O
(4)、(思考与分析)小林同学认为猜想Ⅱ正确,同学们分析后认为他的结论不准确,理由是。要得出正确结论,还需要测定的数据是 , 若用 a 表示该数据,则a的取值范围为 , 可以得出猜想Ⅲ正确。
七、计算题
-
16. 碳酸氢钠俗称小苏打,是食品工业中一种应用最广泛的疏松剂,它在 270℃时能分解(2NaHCO3 Na2CO3+H2O+CO2↑)现取一定质量的碳酸氢钠,加热至完全分解时,产生二氧化碳气体的质量为2.2g。请计算(结果保留到小数点后一位小数):(1)、碳酸氢钠中钠元素的质量分数。(2)、所取碳酸氢钠的质量。
-
-
-
-
-