广东省深圳市2019年中考化学预测卷(一)
试卷更新日期:2019-04-19 类型:中考模拟
一、单选题
-
1. 陶瓷是中华民族在人类科技史上的伟大发明。下列陶瓷制作工艺中发生化学变化的是()A、
 混合
B、
混合
B、 成型
C、
成型
C、 晾干
D、
晾干
D、 烧结
2. 下列化学用语所表达的意义正确的是()A、Al3+——铝离子 B、2K——2个钾元素 C、F2——个氟原子 D、2SO3——3个二氧化硫分子3. 在燃气中加入少量有特殊气味的乙硫醇(C2H5SH),可在燃气泄漏时及时发现,其燃烧的化学方程式为2C2H5SH+9O2 4CO2+2X+6H2O,则X的化学式为( )A、SO2 B、CO C、H2S D、SO34. 下列有关元素、微粒以及物质的描述正确的是()A、金刚石、石墨、C60都是由碳元素形成的结构不同、但性质相同的单质 B、“富硒大米”中的硒指的是元素 C、电解水可以制取氢气,说明水中含有氢气 D、O2-、Na+质子数和电子数都不同5. 甲、乙、丙、丁四种金属,只有丙在自然界中主要以单质形式存在,用甲制的容器不能盛放丁盐的水溶液,用乙制的容器却可以盛放丁盐的水溶液。由此推断四种金属的活动性由强到弱的顺序是( )
烧结
2. 下列化学用语所表达的意义正确的是()A、Al3+——铝离子 B、2K——2个钾元素 C、F2——个氟原子 D、2SO3——3个二氧化硫分子3. 在燃气中加入少量有特殊气味的乙硫醇(C2H5SH),可在燃气泄漏时及时发现,其燃烧的化学方程式为2C2H5SH+9O2 4CO2+2X+6H2O,则X的化学式为( )A、SO2 B、CO C、H2S D、SO34. 下列有关元素、微粒以及物质的描述正确的是()A、金刚石、石墨、C60都是由碳元素形成的结构不同、但性质相同的单质 B、“富硒大米”中的硒指的是元素 C、电解水可以制取氢气,说明水中含有氢气 D、O2-、Na+质子数和电子数都不同5. 甲、乙、丙、丁四种金属,只有丙在自然界中主要以单质形式存在,用甲制的容器不能盛放丁盐的水溶液,用乙制的容器却可以盛放丁盐的水溶液。由此推断四种金属的活动性由强到弱的顺序是( )
A、丙>乙>甲>丁 B、甲>丁>乙>丙 C、丁>甲>乙>丙 D、甲>乙>丁>丙6. 甲、乙、丙三种固体物质的溶解度曲线如右图所示。下列说法错误的是( ) A、T2℃时,取等质量的甲、乙分别配制成饱和溶液,所需水的质量:甲>乙 B、T2℃时,将甲、乙的饱和溶液均降温到T1℃,得到的溶液仍饱和 C、若甲中混有少量的丙,可采用降温结晶的方法提纯甲 D、T2℃时,甲、乙各30g分别加入100g水中,均形成饱和溶液7. 下列实验现象叙述错误的是()A、硝酸铵溶于水,溶液温度升高 B、红磷在空气中燃烧,产生大量白烟 C、浓硫酸涂在木棒上,木棒变黑 D、点燃羊毛纤维,闻到烧焦羽毛气味8. 下列图像符合题意反映对应变化关系的是()A、常温下,相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸反应
A、T2℃时,取等质量的甲、乙分别配制成饱和溶液,所需水的质量:甲>乙 B、T2℃时,将甲、乙的饱和溶液均降温到T1℃,得到的溶液仍饱和 C、若甲中混有少量的丙,可采用降温结晶的方法提纯甲 D、T2℃时,甲、乙各30g分别加入100g水中,均形成饱和溶液7. 下列实验现象叙述错误的是()A、硝酸铵溶于水,溶液温度升高 B、红磷在空气中燃烧,产生大量白烟 C、浓硫酸涂在木棒上,木棒变黑 D、点燃羊毛纤维,闻到烧焦羽毛气味8. 下列图像符合题意反映对应变化关系的是()A、常温下,相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸反应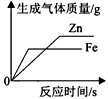 B、向一定量的氢氧化钠溶液中滴加pH=3的稀盐酸
B、向一定量的氢氧化钠溶液中滴加pH=3的稀盐酸  C、加热一定质量的高锰酸钾
C、加热一定质量的高锰酸钾  D、氢气还原一定质量的氧化铜
D、氢气还原一定质量的氧化铜  9. 氨催化氧化是制笑气的主要反应之一,该反应前后分子种类变化的微观示意图如图。下列说法错误的是()
9. 氨催化氧化是制笑气的主要反应之一,该反应前后分子种类变化的微观示意图如图。下列说法错误的是()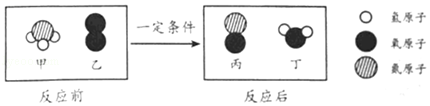 A、甲中氮、氢原子个数比为1:3 B、乙的相对分子质量为32 C、两种生成物均为化合物 D、生成的丙与丁的分子个数比为1:210. 除去下列物质中混有的少量杂质所选用的操作方法,正确的是( )
A、甲中氮、氢原子个数比为1:3 B、乙的相对分子质量为32 C、两种生成物均为化合物 D、生成的丙与丁的分子个数比为1:210. 除去下列物质中混有的少量杂质所选用的操作方法,正确的是( )选项
物质
操作方法
A
CO2混有HCl气体
将气体通过足量NaOH溶液
B
CuO混有碳粉
加入适量稀HCl,过滤、洗涤、干燥
C
NaCl溶液混有CaCl2
加入过量Na2CO3溶液、过滤
D
Cu(NO3)2溶液混有CuCl2
加入适量AgNO3溶液、过滤
A、A B、B C、C D、D二、非选择题
-
11. A,B,C,D,E是九年级化学中常见的五种物质。已知C是人体胃液中可以帮助清化的物质,D是大理石的主要成分,其相互反应及转化关系如下图所示,“﹣“表示示相连的两物质之间能发生反应,“→”表示一种物质能转化为另一种物质,部分反应条件、反应物、生成物已略去。
 (1)、写出下列反应的化学方程式。
(1)、写出下列反应的化学方程式。C与D的反应:;
(2)、B转化为A的反应:;(3)、①C转化为A的反应: , 该反应属于置换反应(填基本反应类型)。②B与E的反应是(填“吸热”或“放热”)反应。
③写出E物质的一种用途;
12. 结合图1化学实验装置,回答有关问题。 (1)、写出图中标有宇母的仪器的名称:a b。(2)、实验室用氯酸钾制取氧气应选择的发生装置是(填代号),可用法收集氧气。制得的氧气用来做如图2所示的实验,发现H中铁丝不燃烧,其原因是。写出G中反应的化学方程式(3)、实验室制取二氧化碳常用的药品是 , 若用装置E收集二氧化碳,则气体应从填“①”或“②“)端进入;若要获得干燥的二氧化碳,可将装置B和装置D用胶皮管连接,并在装置D中盛放(填物质名称)试剂。(4)、实验室常用装置C代替装置B制取气体,装置C的优点是。13. 某工厂化验室用10%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸(该产品中其它物质不与NaOH反应),消耗氢氧化钠溶液的质量与反应过程中溶液的pH值关系如图所示。
(1)、写出图中标有宇母的仪器的名称:a b。(2)、实验室用氯酸钾制取氧气应选择的发生装置是(填代号),可用法收集氧气。制得的氧气用来做如图2所示的实验,发现H中铁丝不燃烧,其原因是。写出G中反应的化学方程式(3)、实验室制取二氧化碳常用的药品是 , 若用装置E收集二氧化碳,则气体应从填“①”或“②“)端进入;若要获得干燥的二氧化碳,可将装置B和装置D用胶皮管连接,并在装置D中盛放(填物质名称)试剂。(4)、实验室常用装置C代替装置B制取气体,装置C的优点是。13. 某工厂化验室用10%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸(该产品中其它物质不与NaOH反应),消耗氢氧化钠溶液的质量与反应过程中溶液的pH值关系如图所示。 (1)、图中A点表示的意义是。(2)、A点消耗氢氧化钠溶液的溶质的质量为g。(3)、求石油产品中残余硫酸的质量(写出计算过程)。
(1)、图中A点表示的意义是。(2)、A点消耗氢氧化钠溶液的溶质的质量为g。(3)、求石油产品中残余硫酸的质量(写出计算过程)。