广东省深圳市2019年中考化学预测卷(三)
试卷更新日期:2019-04-19 类型:中考模拟
一、单选题
-
1. 描述物质变化的成语有:①滴水成冰;③死灰复燃;③木已成舟;④火烧赤壁;⑤沙里淘金;⑥火上浇油;⑦百炼成钢;⑧花香四溢;⑨玉石俱焚,其中属于化学变化的是( )A、②③④⑤⑥⑦ B、④⑤⑥⑦⑨ C、①③④⑤⑧⑨ D、②④⑥⑦⑨2. 下图为钠的原子结构示意图。下列说法错误的是( )
 A、钠原子的质子数为11 B、n=8 C、钠原子在反应中容易失电子 D、钠元素位于第二周期3. 水是生命之源,是人类生产生活中不可缺少的物质。下列有关水的说法正确的是( )A、水的天然循环主要是通过化学变化完成的 B、活性炭可以吸附黄泥水中的泥沙 C、通过过滤操作可以把硝酸钾从它的水溶液中分离出来 D、天然水的人工净化过程中,通过蒸馏操作得到的水是纯净物4. 在一密闭容器中放入X、Y、Z、Q四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,则关于此反应的认识正确的是()
A、钠原子的质子数为11 B、n=8 C、钠原子在反应中容易失电子 D、钠元素位于第二周期3. 水是生命之源,是人类生产生活中不可缺少的物质。下列有关水的说法正确的是( )A、水的天然循环主要是通过化学变化完成的 B、活性炭可以吸附黄泥水中的泥沙 C、通过过滤操作可以把硝酸钾从它的水溶液中分离出来 D、天然水的人工净化过程中,通过蒸馏操作得到的水是纯净物4. 在一密闭容器中放入X、Y、Z、Q四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,则关于此反应的认识正确的是()物质
X
Y
Z
Q
反应前质量/g
20
2
1
37
反应后质量/g
15
32
1
未知
A、物质Y一定是单质 B、反应后物质Q的质量为12g C、反应过程中X、Q的质量比为9:4 D、物质Z一定的该反应的催化剂5. 下列有关元素、微粒以及物质的描述正确的是()A、金刚石、石墨、C60都是由碳元素形成的结构不同、但性质相同的单质 B、“富硒大米”中的硒指的是元素 C、电解水可以制取氢气,说明水中含有氢气 D、O2-、Na+质子数和电子数都不同6. 保护金属资源的有效途径,不包括下列的( )A、合理开采矿物 B、寻找金属替代品 C、回收利用金属 D、禁止使用铁制品7. KNO3与KCl的溶解度曲线如右图所示。下列说法正确的是( )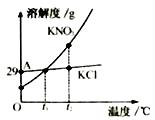 A、KNO3的溶解度比KCl的溶解度大 B、t1温度下的KCl的饱和溶液升温至t2 , 有晶体析出 C、A点所表示的KCl饱和溶液溶质的质量分数为29% D、冷却热的KNO3饱和溶液可获得KNO3晶体8. 根据你的化学知识和生活经验判断,下列说法错误的是( )A、打开浓盐酸试剂瓶瓶塞,能闻到刺激性气味,是因为分子在不断地运动 B、滴加洗涤剂能将餐具上的油污洗掉,因为洗涤剂能溶解油污 C、吃松花蛋时可加入少量食醋,因为食醋能消除蛋中所含碱性物质的涩味 D、稀盐酸能用来除去铁制品表面的铁锈,因为稀盐酸能与某些金属氧化物反应9. 下列物质属于氧化物的是( )A、KMnO4 B、KOH C、O3 D、CO10. 下表中除去物质中少量杂质的方法正确的是( )
A、KNO3的溶解度比KCl的溶解度大 B、t1温度下的KCl的饱和溶液升温至t2 , 有晶体析出 C、A点所表示的KCl饱和溶液溶质的质量分数为29% D、冷却热的KNO3饱和溶液可获得KNO3晶体8. 根据你的化学知识和生活经验判断,下列说法错误的是( )A、打开浓盐酸试剂瓶瓶塞,能闻到刺激性气味,是因为分子在不断地运动 B、滴加洗涤剂能将餐具上的油污洗掉,因为洗涤剂能溶解油污 C、吃松花蛋时可加入少量食醋,因为食醋能消除蛋中所含碱性物质的涩味 D、稀盐酸能用来除去铁制品表面的铁锈,因为稀盐酸能与某些金属氧化物反应9. 下列物质属于氧化物的是( )A、KMnO4 B、KOH C、O3 D、CO10. 下表中除去物质中少量杂质的方法正确的是( )选项
物质
所含杂质
除去杂质的方法
A
氯化钠
泥沙
加入适量水溶解、过滤、洗涤、干燥
B
氮气
氧气
将混合气体通过灼热的铜网
C
木炭
四氧化三铁
将混合物在空气中灼烧
D
氢氧化钠溶液
氢氧化钙
加入过量的碳酸钠溶液,充分反应后,过滤
A、A B、B C、C D、D二、非选择题
-
11. 下图中A,B,C,D,E,F分别表示初中化学常见的六种物质,B、C、D、E分别属于酸、碱、盐、氧化物四种类别中的一种,A是目前提取量最大的金属,B由两种元素组成,C是大理石的主要成分。(图中用“—”表示两种物质之间能发生化学反应,用“→”或“
 ”表示一种物质能转化为另一种物质,部分反应物和生成物及反应条件已略去,图中部分反应需要在溶液中进行,物质是溶液的只考虑溶质)。
”表示一种物质能转化为另一种物质,部分反应物和生成物及反应条件已略去,图中部分反应需要在溶液中进行,物质是溶液的只考虑溶质)。 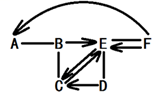
请回答下列问题。
(1)、分别写出A、C、E、F物质的化学式 ACEF。(2)、写出B与C发生反应的化学方程式。(3)、写出过量A的粉末与B发生反应的实验现象。12. 请回答下列实验问题:(1)、现提供下列装置
①上图C装置中,甲仪器的名称是。
②实验室将双氧水加入二氧化锰粉末制取氧气,发生装置是(填序号),反应的化学方程式为 , 若用E装置收集氧气,当有时,开始收集气体。
③实验室可以按照“B→F→F→真空气囊”的装置顺序制取纯净的CO2气体,B装置中发生反应的化学方程式为 , 第一个F装置盛放试剂的作用是 , 第二个F装置盛放的试剂为。
(2)、实验室用氯化钠固体配制50g15%的氯化钠溶液的步骤有:计算、称取氯化钠、量取水、溶解、转移。①在溶解过程中,玻璃棒的作用是。
②下列操作中,可能导致配制氯化钠溶液的溶质质量分数偏大的是(填序号)。
a.称取时,将氯化钠置于托盘天平的右盘
b.量取水时俯视读数
c.用已有少量水的烧杯溶解氯化钠
d.转移时,有少量溶液溅出
13. 将20.0g稀盐酸逐滴加入到10.0g溶质质量分数为40%的氢氧化钠溶液中,边滴加边搅拌,随着稀盐酸的滴加,溶液的pH变化情况如图所示,溶液的温度变化如表所示(不考虑反应过程中热量散失)
反应时间(s)
0
10
20
30
40
50
60
溶液温度(℃)
20.5
20.6
20.7
20.8
20.9
20.8
20.7
(1)、当稀盐酸与氢氧化钠溶液恰好完全反应时,溶液的温度是℃(2)、计算稀盐酸中溶质的质量分数(精确到0.1%)