内蒙古自治区赤峰市宁城县2018-2019学年九年级上学期化学期末考试试卷
试卷更新日期:2019-04-17 类型:期末考试
一、单选题
-
1. 下列现象一定涉及化学变化的是( )A、木已成舟 B、积土成山 C、滴水成冰 D、百炼成钢2. 下列实验操作中,正确的是( )
A、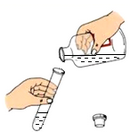 倾倒液体
B、
倾倒液体
B、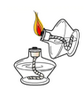 点燃酒精灯
C、
点燃酒精灯
C、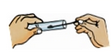 取用固体粉末
D、
取用固体粉末
D、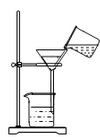 过滤
3. 分类是研究物质的常用方法。下图是纯净物、单质、化合物、氧化物之间关系的形象表示,若整个大圆圈表示纯净物,则下列物质属于Z范围的是( )
过滤
3. 分类是研究物质的常用方法。下图是纯净物、单质、化合物、氧化物之间关系的形象表示,若整个大圆圈表示纯净物,则下列物质属于Z范围的是( )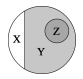 A、红磷 B、干冰 C、氯酸钾 D、食盐水4. 下列实验现象描述正确的是( )A、硫在氧气中燃烧发出淡蓝色火焰 B、磷在空气中燃烧产生大量白烟 C、木炭在空气中燃烧发出白光 D、铁丝在氧气中燃烧,火星四射,生成四氧化三铁5. LiCoO2(钴锂酸)主要用于制造飞机、笔记本电脑及其它便携式电子设备锂离子电池的正极材料。已知LiCoO2中Li元素的化合价为+1价,则Co元素的化合价为( )A、+1 B、+2 C、+3 D、+46. 在反应2Mg + O2 2MgO中镁、氧气、氧化镁的质量比为( )A、48:32:80 B、24:32:40 C、24:32:64 D、24:32:807. 葡萄糖在人体组织中缓慢氧化,放出热量,供给人们所需能量,是人类生命活动所需能量的重要来源之一.若R代表葡萄糖,所发生的氧化反应为R+6O2=6CO2+6H2O,则葡萄糖的分子式为( )A、C6H12 B、C6H10O C、C5H6O2 D、C6H12O68. 下列说法正确的是( )A、计算机房失火只能用泡沫灭火器灭火 B、二氧化碳有毒,空气中含量过高,会使人中毒死亡 C、在煤矿的矿井里,通风并严禁烟火,可以有效地防止发生爆炸事故 D、某物质完全燃烧后生成二氧化碳和水,则该物质一定由碳、氢、氧三种元素组成9. 在化学实验室内外一般不会张贴的标志是( )A、
A、红磷 B、干冰 C、氯酸钾 D、食盐水4. 下列实验现象描述正确的是( )A、硫在氧气中燃烧发出淡蓝色火焰 B、磷在空气中燃烧产生大量白烟 C、木炭在空气中燃烧发出白光 D、铁丝在氧气中燃烧,火星四射,生成四氧化三铁5. LiCoO2(钴锂酸)主要用于制造飞机、笔记本电脑及其它便携式电子设备锂离子电池的正极材料。已知LiCoO2中Li元素的化合价为+1价,则Co元素的化合价为( )A、+1 B、+2 C、+3 D、+46. 在反应2Mg + O2 2MgO中镁、氧气、氧化镁的质量比为( )A、48:32:80 B、24:32:40 C、24:32:64 D、24:32:807. 葡萄糖在人体组织中缓慢氧化,放出热量,供给人们所需能量,是人类生命活动所需能量的重要来源之一.若R代表葡萄糖,所发生的氧化反应为R+6O2=6CO2+6H2O,则葡萄糖的分子式为( )A、C6H12 B、C6H10O C、C5H6O2 D、C6H12O68. 下列说法正确的是( )A、计算机房失火只能用泡沫灭火器灭火 B、二氧化碳有毒,空气中含量过高,会使人中毒死亡 C、在煤矿的矿井里,通风并严禁烟火,可以有效地防止发生爆炸事故 D、某物质完全燃烧后生成二氧化碳和水,则该物质一定由碳、氢、氧三种元素组成9. 在化学实验室内外一般不会张贴的标志是( )A、 B、
B、 C、
C、 D、
D、 10. 绿色化学有助于解决环境污染问题,下列做法不符合绿色化学理念的是( )A、大力发展公共交通,提倡绿色出行 B、使用可降解塑料,减少白色污染 C、加速石油的开采,可以快速提高人类生活质量 D、为了防止水污染,农业上要合理使用化肥、农药11. 康康同学在探究燃烧条件时,进行了如图所示的实验.下列关该实验的说法错误的是( )
10. 绿色化学有助于解决环境污染问题,下列做法不符合绿色化学理念的是( )A、大力发展公共交通,提倡绿色出行 B、使用可降解塑料,减少白色污染 C、加速石油的开采,可以快速提高人类生活质量 D、为了防止水污染,农业上要合理使用化肥、农药11. 康康同学在探究燃烧条件时,进行了如图所示的实验.下列关该实验的说法错误的是( ) A、铜片上的白磷燃烧而红磷不燃烧,说明燃烧需要达到可燃物的着火点 B、铜片上的白磷燃烧而热水中的白磷不燃烧,说明燃烧需要空气(或氧气) C、即使向热水中的白磷通入氧气,白磷也不可能燃烧 D、由本实验推知,消除可燃物燃烧的任何一个条件,都可达到灭火的目的12. 将宏观、微观及化学符号联系在一起是化学学科的特点。某化学反应微观示意图如图所示,下列叙述正确的是( )
A、铜片上的白磷燃烧而红磷不燃烧,说明燃烧需要达到可燃物的着火点 B、铜片上的白磷燃烧而热水中的白磷不燃烧,说明燃烧需要空气(或氧气) C、即使向热水中的白磷通入氧气,白磷也不可能燃烧 D、由本实验推知,消除可燃物燃烧的任何一个条件,都可达到灭火的目的12. 将宏观、微观及化学符号联系在一起是化学学科的特点。某化学反应微观示意图如图所示,下列叙述正确的是( )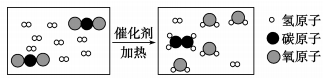 A、反应前后各元素化合价不变 B、该化学变化中发生改变的微粒是原子 C、该反应不符合质量守恒定律 D、参加反应的CO2和H2分子个数比为1:313. 砷化镓(GaAs)是一种“LED”绿色节能光源材料,镓元素的相关信息如图.下列有关镓的说法错误的是( )
A、反应前后各元素化合价不变 B、该化学变化中发生改变的微粒是原子 C、该反应不符合质量守恒定律 D、参加反应的CO2和H2分子个数比为1:313. 砷化镓(GaAs)是一种“LED”绿色节能光源材料,镓元素的相关信息如图.下列有关镓的说法错误的是( )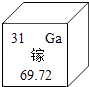 A、原子的核电荷数是31 B、元素符号是Ga C、属于金属元素 D、相对原子质量为69.72g14. 水是由氢元素和氧元素组成的,下列有关说法正确的是( )A、氧离子的结构示意图
A、原子的核电荷数是31 B、元素符号是Ga C、属于金属元素 D、相对原子质量为69.72g14. 水是由氢元素和氧元素组成的,下列有关说法正确的是( )A、氧离子的结构示意图 B、H2O和H2O2中氢元素的化合价相同
C、电解水实验中氢气和氧气的质量比为2:1
D、水沸腾时可冲起壶盖,说明温度升高水分子变大
15. 以下是根据一些实验事实推理出的影响化学反应的因素,其中推理错误的是( )
B、H2O和H2O2中氢元素的化合价相同
C、电解水实验中氢气和氧气的质量比为2:1
D、水沸腾时可冲起壶盖,说明温度升高水分子变大
15. 以下是根据一些实验事实推理出的影响化学反应的因素,其中推理错误的是( )序号
实验事实
影响化学反应的因素
A
铁丝在空气中很难燃烧,而在氧气中能剧烈燃烧
反应物浓度
B
碳在常温下不与氧气反应,而在点燃时能与氧气反应
反应温度
C
大块木头不易点燃,而刨成非常薄的片状却易点燃
反应物的种类
D
双氧水在常温下缓慢分解,而在加入二氧化锰后迅速分解
有、无催化剂
A、A B、B C、C D、D16. 下列物质的性质与所对应的用途没有直接关系的是( )A、石墨能导电﹣可作电极 B、干冰升华吸热﹣用于人工降雨 C、稀有气体的性质稳定﹣可作保护气 D、氧气的密度比空气略大﹣用于急救病人17. 化学反应前后肯定没有变化的是( )①原子数目 ②分子数目 ③元素种类
④物质种类 ⑤原子种类 ⑥物质的总质量
A、①④⑥ B、②③⑤ C、①②⑥ D、①③⑤⑥18. 下列关于分子、原子、离子的说法错误的是( )A、铜、汞等金属单质都是由原子构成的物质 B、氯化钠、硫酸铜均是由阴、阳离子构成的物质 C、氧气、金刚石等非金属单质都是由分子构成的物质 D、水、氨气的化学性质分别是由水分子和氨分子保持的二、填空题
-
19. 依据所给内容:①2SO42﹣②氢气③二氧化硫④氢氧根离子⑤一氧化碳⑥N2 ⑦化石燃料之天然气的主要成分。按要求完成下列问题(1)、形成酸雨的主要气体;(用序号填空,下同)(2)、将成为一种重要的无污染新型燃料的是;(3)、其中的“2”表示离子个数的是;(4)、与血红蛋白结合引起中毒的气体;(5)、其中的“2”表示一个分子中的原子个数的是;(6)、写出氢氧化钠溶液中阴离子的符号(填写相应的化学用语,下同)(7)、天然气的主要成分的化学式。20. 美国普渡大学研究出一种利用铝镓合金制备氢气的新工艺,流程如图所示:
 (1)、氧化铝(Al2O3)制取铝的反应中。铝元素的化合价(填“升高”“降低”“不变”);(2)、此流程生成的氧化铝中氧元素来自于;(3)、上述过程中,涉及到的氧化物有(填化学式)(4)、氧化铝可以借助太阳能电池重新变成氧气与金属铝,该反应的化学方程式为 , 反应类型是(填“化合反应”或“分解反应”)。21. 阅读下列短文,运用你所学的知识将正确的编号填入题后的空格里.
(1)、氧化铝(Al2O3)制取铝的反应中。铝元素的化合价(填“升高”“降低”“不变”);(2)、此流程生成的氧化铝中氧元素来自于;(3)、上述过程中,涉及到的氧化物有(填化学式)(4)、氧化铝可以借助太阳能电池重新变成氧气与金属铝,该反应的化学方程式为 , 反应类型是(填“化合反应”或“分解反应”)。21. 阅读下列短文,运用你所学的知识将正确的编号填入题后的空格里.①氧气在通常情况下是无色无味的气体;
②氧气不易溶于水;
③在标准状况下氧气的密度是1.429g/L比空气重;
④将纯氧吹入炼钢炉中,可以提高炉温,用于炼钢;
⑤氧气在一定条件下能与铁丝、木炭等物质发生化学反应;
⑥氧气具有氧化性.其中属于物理性质的是 , 属于化学性质的是 , 属于用途的是 .
22. 已知A、E、F是单质,B、C、D是化合物,它们分别是由碳、氢、氧三种元素中的一种或者几种组成。其中B是相对分子质量最小的氧化物,D物质很不稳定,容易分解生成B和C,它们之间的转化关系如右图所示。 (1)、则A、F的化学式为A: , F:(2)、请你写出下列变化的化学方程式:
(1)、则A、F的化学式为A: , F:(2)、请你写出下列变化的化学方程式:A+E→B
D→B+C
三、简答题
-
23. 利用化学知识,可以解释与解决生活中一些常见的问题,请你完成下列空白:(1)、水与双氧水的化学性质不同,是因为它们的不同。(2)、用活性炭净水器可净化饮用水是利用活性炭的作用。(3)、天然水中含有许多杂质,将天然水变成纯水的方法是。日常生活中软化硬水的方法。(4)、下列生活中的做法 不利于节约用水的是_____A、洗菜的水用来浇花 B、未喝完的矿泉水随手倒掉 C、用不间断的流水冲洗碗筷 D、洗手使用洗手液时暂时关闭水龙头(5)、6.5世界环境日中国主题为“共建生态文明,共享绿色未来”。请你参与下列问题:内蒙古大草原,过去是“天苍苍,野茫茫,风吹草地现牛羊”,现在则是“天苍苍,野茫茫,老鼠跑过露脊梁”,其原因可能是_____。A、温室效应引起长期干旱 B、乱砍乱伐森林 C、过度放牧、盲目开垦 D、酸雨的影响
四、实验题
-
24. 通过一学期的化学学习,相信你已掌握了实验室制取气体的有关知识。请结合图示回答下列问题:
 (1)、请写出图中标号a、b仪器的名称:a;b。(2)、装置A与D或E组合制取气体的条件:反应物必须是 , 生成的气体;实验室收集气体前应对产生的气体进行检验,请你用化学方程式表示CO2气体的检验方法:。(3)、加热某紫黑色固体制取氧气,发生装置应该选择A,同时需要在试管口放 , 其作用是 , 写出该反应的化学方程式。(4)、检查装置B气密性的方法是 , 该装置的优点是。(5)、装置B与D组合,可以制取一种温室气体是 , 该反应的化学方程式为。(6)、F装置可用来测量生成CO2气体的体积,在水面上放一层植物油的目的是。(7)、在以后的化学学习中你将会学到,实验室可以通过加热氯化铵(NH4Cl)和熟石灰Ca(OH)2来制取氨气(NH3),同时生成氯化钙,发生装置应选择 , 化学方程式为。
(1)、请写出图中标号a、b仪器的名称:a;b。(2)、装置A与D或E组合制取气体的条件:反应物必须是 , 生成的气体;实验室收集气体前应对产生的气体进行检验,请你用化学方程式表示CO2气体的检验方法:。(3)、加热某紫黑色固体制取氧气,发生装置应该选择A,同时需要在试管口放 , 其作用是 , 写出该反应的化学方程式。(4)、检查装置B气密性的方法是 , 该装置的优点是。(5)、装置B与D组合,可以制取一种温室气体是 , 该反应的化学方程式为。(6)、F装置可用来测量生成CO2气体的体积,在水面上放一层植物油的目的是。(7)、在以后的化学学习中你将会学到,实验室可以通过加热氯化铵(NH4Cl)和熟石灰Ca(OH)2来制取氨气(NH3),同时生成氯化钙,发生装置应选择 , 化学方程式为。五、科学探究题
-
25. 实验探究:小林同学在体育课上腿部擦伤,医务室的大夫在她伤口上涂了医用过氧化氢溶液,小林看到伤口处产生了小气泡,很好奇。为什么瓶中的过氧化氢溶液涂到伤口上,分解就加快了呢?
 (1)、I.小林准备用如图2所示装置测定过氧化氢分解的快慢,实验前在注射器中吸入过氧化氢溶液,量筒内装满水。实验开始时,向试管中注入过氧化氢溶液,并用排水法收集氧气,记录2分钟收集的气体体积。
(1)、I.小林准备用如图2所示装置测定过氧化氢分解的快慢,实验前在注射器中吸入过氧化氢溶液,量筒内装满水。实验开始时,向试管中注入过氧化氢溶液,并用排水法收集氧气,记录2分钟收集的气体体积。请写出过氧化氢分解的化学方程式:,
(2)、若要检验生成的气体是否为氧气,可将导气管从水中取出, , 说明生成的气体是氧气。(3)、Ⅱ.小林查阅了相关资料,并进行了探究实验(查阅资料)①.过氧化氢是人体代谢废物之一,它能够对机体造成损害,人体存在过氧化氢酶,可以催化过氧化氢分解。
②.温度对化学反应的快慢有影响,人体正常体温是37℃。
(提出猜想)
猜想1:过氧化氢分解加快是因为体温比瓶中的温度高。
猜想2:过氧化氢分解加快是因为伤口中有过氧化氢酶。
(进行实验)
序号
实验步骤
实验现象
实验结论
①
分两次进行实验,均注入5mL过氧化氢溶液
第一次在常温下进行
第二次将试管浸在37℃的温水中
量筒中2分钟收集到的气体体积均为5mL
猜想不成立
②
分两次进行实验
第一次将装有一小粒过氧化氢酶的试管浸在37℃的温水中,注入5mL过氧化氢溶液
第二次
第一次,量筒中2分钟收集到的气体体积为56mL
第二次,量筒中2分钟收集到的气体体积为5mL
猜想成立
(4)、(实验反思)小林反思了实验过程,认为人体中过氧化氢酶是在体温条件下发挥作用的,实验得出的结论可能存在不足。因此又补充进行了几组实验,数据记录如下表所示。
加入过氧化氢酶
不加过氧化氢酶
反应温度/℃
25
37
42
25
37
42
收集到气体体积/mL
39
56
60
5
5
5
通过这些数据,你能得出的新结论是。
要证明某物质是催化剂,还需要证明的是。
六、计算题
-
26. 如图是诺氟沙星胶囊的说明书,某患者遵医嘱,每次服用诺氟沙星胶囊400mg,一段时间后病情有了好转。(诺氟沙星的化学式为C16H18FN3O3)
请回答以下问题:
 (1)、诺氟沙星分子中碳、氢的原子个数比为;(最简整数比)(2)、诺氟沙星中氮元素的质量分数是;(精确到0.1%)(3)、从组成上可知诺氟沙星属于;(填“单质”或“化合物”)(4)、31.9g诺氟沙星含氧元素的质量为g。27. 某化学兴趣小组为了粗略测定一批石灰石样品中CaCO3的质量分数,设计并进行如下实验。实验装置如图所示:称取研细的2.50g石灰石样品,分4次加入稀盐酸,充分反应至不再产生气体为止。测得反应前后的有关质量如表:
(1)、诺氟沙星分子中碳、氢的原子个数比为;(最简整数比)(2)、诺氟沙星中氮元素的质量分数是;(精确到0.1%)(3)、从组成上可知诺氟沙星属于;(填“单质”或“化合物”)(4)、31.9g诺氟沙星含氧元素的质量为g。27. 某化学兴趣小组为了粗略测定一批石灰石样品中CaCO3的质量分数,设计并进行如下实验。实验装置如图所示:称取研细的2.50g石灰石样品,分4次加入稀盐酸,充分反应至不再产生气体为止。测得反应前后的有关质量如表: (1)、反应生成二氧化碳的质量为。(2)、计算石灰石样品中CaCO3的质量分数。(3)、若在上述实验过程中石灰石样品和所加酸液均无抛洒,根据图中装置判断,该实验结果可能(填“偏大”、“偏小”或“准确”)。
(1)、反应生成二氧化碳的质量为。(2)、计算石灰石样品中CaCO3的质量分数。(3)、若在上述实验过程中石灰石样品和所加酸液均无抛洒,根据图中装置判断,该实验结果可能(填“偏大”、“偏小”或“准确”)。反应前,整套装置+样品的质量/g
共加入:稀盐
酸的质量/g
反应后,整套装置+锥
形瓶中剩余物的质量/g
104.60
20.00
123.72
-
-
-