湖北省荆州市洪湖市2018-2019学年中考化学一模考试试卷
试卷更新日期:2019-04-08 类型:中考模拟
一、单选题
-
1. 我国有着悠久的历史和灿烂的文化。下列工艺中一定发生化学变化的是( )A、刺绣 B、织布 C、剪纸 D、酿酒2. 下列实验基本操作中,正确的是( )A、氧气验满
 B、加热液体
B、加热液体  C、滴加液体
C、滴加液体  D、收集二氧化碳
D、收集二氧化碳  3. 下列关于宏观事实的微观解释,错误的是( )A、浓氨水挥发——氨分子不断运动 B、温度计内汞柱液面上升——汞原子体积变大 C、干冰升华——二氧化碳分子间的间隔变大 D、一滴水中大约有1.67×1021个水分子——水分子的质量和体积都很小4. 下列做法符合安全要求的是( )A、火灾逃生时弯腰前行 B、煤火取暖时紧闭门窗 C、燃气泄漏时点火检查 D、森林游玩时乱扔烟头5. 水与人们的生活息息相关,下列有关水的说法错误的是( )A、长期饮用蒸馏水不利于人体的健康 B、将水加热煮沸能降低水的硬度 C、用肥皂水鉴别硬水和软水 D、过滤可除去水中所有杂质6. 食醋是厨房中常用的调味品,它的主要成分是乙酸(CH3COOH)。下列有关乙酸的说法中,正确的是( )A、乙酸是一种化合物 B、乙酸中碳元素的质量分数最大 C、乙酸中共含有8个原子 D、乙酸中碳、氢,氧三种元素的质量比为1:2:17. 纳米铁粉在空气中能自燃并生成一种红色氧化物。对比铁丝在空气中不能燃烧,而在氧气中能剧烈燃烧的事实,某同学得出的下列结论错误的是( )A、纳米铁粉在空气中自燃的产物不是四氧化三铁 B、相同的反应物在不同条件下生成物可能不同 C、有些物质燃烧时温度不需要达到着火点 D、反应物间的接触面积大小是反应能否发生的因素之一8. 空气是一种宝贵的自然资源。下列有关空气的说法错误的是( )A、氮气的化学性质不活泼,可用于食品的防腐 B、空气的成分按体积计算,稀有气体大约占0.03% C、燃烧法测定空气中氧气的含量,不能用硫代替红磷 D、禁止燃放烟花爆竹,可以减少空气污染9. 煤炭燃烧排出的尾气中,能形成酸雨的是( )A、N2 B、CO2 C、SO2 D、H2O10. 下列物质由离子构成的是( )A、二氧化碳 B、水 C、金刚石 D、氯化钠11. 下列有关碳和碳的化合物说法错误的是( )A、金刚石、石墨、C60都是碳元素组成的单质 B、在加热或高温的条件下,CO能与许多金属氧化物反应 C、二氧化碳能使紫色石蕊溶液变红,说明二氧化碳具有酸性 D、水墨画可长久保存不变色是因为在常温下碳的化学性质不活泼12. 在光照条件下,AgNO3可分解为Ag、O2和某种氮的氧化物X,取34gAgNO3固体充分光照,测得完全反应后生成Ag、O2、X的质量分别为21.6g、mg、9.2g。下列说法正确的是( )A、AgNO3固体应密封保存在无色细口瓶中 B、m=3.3 C、该反应方程式中Ag与O2的化学计量数之比为3∶2 D、X的化学式为NO2
3. 下列关于宏观事实的微观解释,错误的是( )A、浓氨水挥发——氨分子不断运动 B、温度计内汞柱液面上升——汞原子体积变大 C、干冰升华——二氧化碳分子间的间隔变大 D、一滴水中大约有1.67×1021个水分子——水分子的质量和体积都很小4. 下列做法符合安全要求的是( )A、火灾逃生时弯腰前行 B、煤火取暖时紧闭门窗 C、燃气泄漏时点火检查 D、森林游玩时乱扔烟头5. 水与人们的生活息息相关,下列有关水的说法错误的是( )A、长期饮用蒸馏水不利于人体的健康 B、将水加热煮沸能降低水的硬度 C、用肥皂水鉴别硬水和软水 D、过滤可除去水中所有杂质6. 食醋是厨房中常用的调味品,它的主要成分是乙酸(CH3COOH)。下列有关乙酸的说法中,正确的是( )A、乙酸是一种化合物 B、乙酸中碳元素的质量分数最大 C、乙酸中共含有8个原子 D、乙酸中碳、氢,氧三种元素的质量比为1:2:17. 纳米铁粉在空气中能自燃并生成一种红色氧化物。对比铁丝在空气中不能燃烧,而在氧气中能剧烈燃烧的事实,某同学得出的下列结论错误的是( )A、纳米铁粉在空气中自燃的产物不是四氧化三铁 B、相同的反应物在不同条件下生成物可能不同 C、有些物质燃烧时温度不需要达到着火点 D、反应物间的接触面积大小是反应能否发生的因素之一8. 空气是一种宝贵的自然资源。下列有关空气的说法错误的是( )A、氮气的化学性质不活泼,可用于食品的防腐 B、空气的成分按体积计算,稀有气体大约占0.03% C、燃烧法测定空气中氧气的含量,不能用硫代替红磷 D、禁止燃放烟花爆竹,可以减少空气污染9. 煤炭燃烧排出的尾气中,能形成酸雨的是( )A、N2 B、CO2 C、SO2 D、H2O10. 下列物质由离子构成的是( )A、二氧化碳 B、水 C、金刚石 D、氯化钠11. 下列有关碳和碳的化合物说法错误的是( )A、金刚石、石墨、C60都是碳元素组成的单质 B、在加热或高温的条件下,CO能与许多金属氧化物反应 C、二氧化碳能使紫色石蕊溶液变红,说明二氧化碳具有酸性 D、水墨画可长久保存不变色是因为在常温下碳的化学性质不活泼12. 在光照条件下,AgNO3可分解为Ag、O2和某种氮的氧化物X,取34gAgNO3固体充分光照,测得完全反应后生成Ag、O2、X的质量分别为21.6g、mg、9.2g。下列说法正确的是( )A、AgNO3固体应密封保存在无色细口瓶中 B、m=3.3 C、该反应方程式中Ag与O2的化学计量数之比为3∶2 D、X的化学式为NO2二、填空题
-
13. 通过学习化学,我们认识了许多物质。请从:①一氧化碳;②活性炭;③二氧化碳;④氢气;⑤氦气;⑥氧气中,选取相应物质的序号填空(每种物质限选一次)。(1)、用于急救病人的气体是;(2)、最清洁的燃料是;(3)、可用于冰箱除异味的是;(4)、充入灯泡内通电能发出有色光的是。14. 汽车尾气催化转换器可减少有害气体的排放,其中某一反应过程的微观变化如图所示。请回答下列问题:
 (1)、化学反应前后种类没有发生改变的微粒是(填“分子”或“原子”)。(2)、丙中碳元素的化合价为。(3)、已知丁是一种单质,则丁的化学式是。(4)、该反应的化学方程式为。15. 以1-18号元素为研究对象,请回答下列问题:(1)、1~18号元素中最外层有2个电子的原子有、Be、Mg(填元素符号)。(2)、氮化钠是科学家制备的一种重要的化合物,在室温时为晶体,在低于室温时会变成非晶体,高于87℃时会分解为钠单质及氮气,氮化钠的化学式是。(3)、某粒子的结构示意图为
(1)、化学反应前后种类没有发生改变的微粒是(填“分子”或“原子”)。(2)、丙中碳元素的化合价为。(3)、已知丁是一种单质,则丁的化学式是。(4)、该反应的化学方程式为。15. 以1-18号元素为研究对象,请回答下列问题:(1)、1~18号元素中最外层有2个电子的原子有、Be、Mg(填元素符号)。(2)、氮化钠是科学家制备的一种重要的化合物,在室温时为晶体,在低于室温时会变成非晶体,高于87℃时会分解为钠单质及氮气,氮化钠的化学式是。(3)、某粒子的结构示意图为 (y≠0),当x-y=8时该粒子的符号为。
(4)、具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有相似的结构和性质。与N2O互为等电子体的粒子符号为。16. A~F 是初中化学常见的5种物质,分别由C、H、O、Ca中的一种或几种元素组成。已知A的固体可用于人工降雨;B是可燃性气体,燃烧能生成A;化合物D、E、F中含有相同的金属元素,且存在如下转化关系:D→E→F→A。
(y≠0),当x-y=8时该粒子的符号为。
(4)、具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有相似的结构和性质。与N2O互为等电子体的粒子符号为。16. A~F 是初中化学常见的5种物质,分别由C、H、O、Ca中的一种或几种元素组成。已知A的固体可用于人工降雨;B是可燃性气体,燃烧能生成A;化合物D、E、F中含有相同的金属元素,且存在如下转化关系:D→E→F→A。请回答下列问题:
(1)、A的另一种用途是。(2)、B中一定含有的元素是。(3)、D→E的化学方程式是。(4)、F→A的化学方程式是。三、实验题
-
17. 观察是学习化学的重要方法。研究小组进行如下实验,发现均有红棕色二氧化氮气体产生。

查阅资料:4HNO3 O2↑+4NO2↑+2H2O;C+4HNO3(浓) CO2↑+4NO2↑+2H2O
(1)、浓HNO3(浓硝酸)易挥发出HNO3 , 浓硝酸的挥发性是浓硝酸的(填“物理”或“化学”)性质。(2)、(实验1)中所用碎玻璃与浓硝酸不发生化学反应,灼热的碎玻璃在实验中起到的作用是。(3)、(实验2)中有红棕色气体产生,并不能证明(实验2)中木炭与浓硝酸发生了反应,理由是:。(4)、(实验3)发现生成的气体产物中检测出二氧化碳(体积分数大于0.03%),但也不能证明(实验3)中木炭与浓硝酸发生了反应,请用化学方程式说明理由:18. 在实验室中利用下列仪器进行制取气体的实验,请回答下列问题: (1)、利用图中仪器可以制取并收集二氧化碳,你选择的仪器是(填字母,按字母顺序排列),所用药品是。(2)、若补充一种仪器(填仪器名称),再利用高锰酸钾以及图中仪器还可以制取氧气,其反应的化学方程式为 。19. 兴趣小组对“一氧化碳还原氧化铜”的实验进行拓展研究。
(1)、利用图中仪器可以制取并收集二氧化碳,你选择的仪器是(填字母,按字母顺序排列),所用药品是。(2)、若补充一种仪器(填仪器名称),再利用高锰酸钾以及图中仪器还可以制取氧气,其反应的化学方程式为 。19. 兴趣小组对“一氧化碳还原氧化铜”的实验进行拓展研究。(查阅资料)
Ⅰ.制取CO的方法:加热碳酸镁和锌粉的混合物,反应原理为:MgCO3+Zn=MgO+ZnO+CO↑
Ⅱ.处理尾气的方法:用氯化亚铜的氨水溶液吸收一氧化碳,溶液中会出现红色固体。
(设计方案)根据上述资料设计如下实验装置(固定装置略,装置气密性良好):

(实验步骤)
第一步:打开弹簧夹,通入一会儿氮气;
第二步:关闭弹簧夹,点燃两个酒精灯;
第三步:一段时间后,熄灭两个酒精灯;
第四步:……
(实验分析)
(1)、实验过程中,观察到B处的实验现象是 , C处发生反应的化学方程式是;D处发生反应的化学方程式为:2CuCl+2CO+2X═Cu2Cl2(CO)2·2H2O↓,其中X的化学式为。(2)、上述实验步骤中,第一步操作的目的是;第四步操作是:打开弹簧夹,再通入氮气至。
(3)、若A处有mgMgCO3参加反应,C处生成ngCaCO3 , 能证明25m>21n的一个实验现象是。四、计算题
-
20. 已知:Cu与稀硫酸(H2SO4)不反应,Zn+H2SO4=ZnSO4+H2↑。某同学将20g黄铜(铜和锌的混合物)放入烧杯中,向烧杯中滴加稀硫酸至过量,实验测得加入稀硫酸的质量与产生氢气质量的关系如下图所示。请计算:
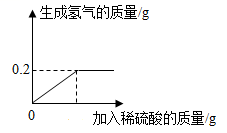 (1)、恰好完全反应时生成氢气的质量是多少g;(2)、该黄铜中锌的质量分数是多少?(3)、若恰好完全反应时加入稀硫酸的质量为100g,则恰好完全反应时烧杯内物质的质量为多少g。
(1)、恰好完全反应时生成氢气的质量是多少g;(2)、该黄铜中锌的质量分数是多少?(3)、若恰好完全反应时加入稀硫酸的质量为100g,则恰好完全反应时烧杯内物质的质量为多少g。