2016-2017学年山东省日照市五莲县九年级上学期期末化学试卷
试卷更新日期:2017-05-02 类型:期末考试
一、选择题
-
1. 下列现象中属于化学变化的是( )A、水结冰 B、酒精挥发 C、水杯破碎 D、葡萄酿酒2. 长征七号运载火箭于2016年6月在海南文昌发射,火箭采用了液氧煤油发动机等新技术,下列说法不正确的是( )A、液氧是助燃剂 B、煤油是不可再生能源 C、液氧是混合物 D、煤油是化石燃料3. 2016年“世界地球日”活动主题为“节约集约利用资源,倡导绿色简约生活”,下列说法不符合主题要求的是( )A、大力发展新能源,禁止使用化石燃料 B、采用“绿色化学”生产工艺,提高原料运用率 C、回收废旧电池,节约金属资源、减少环境污染 D、生活垃圾分类回收,合理利用,减少污染4. 下列有关水或溶液的说法正确的是( )A、用直流电电解水,发现负极与正极上得到的气体体积比约为1:2 B、自来水厂的净水过程中,加入明矾的作用是吸附杂质 C、为了节约用水,可以用工业废水直接浇灌农田 D、均一、稳定的液体一定是溶液5. 下列说法错误的是( )A、稀有气体有广泛的用途,在通电时能发出不同颜色的光,可制成多种用途的电光源 B、自带布袋购物有利于减少“白色污染” C、燃烧和缓慢氧化都属于氧化反应 D、厨房内燃气泄漏时应立即打开排气扇6. 下列化学用语书写正确的是( )A、氢氧根离子:OH B、硫酸铁的化学式:Fe2(SO4)3 C、钠离子: D、3个二氧化硫分子:SO27. 采取正确的措施,能够避免火灾发生或减少灾害损失,下列灭火方法不恰当的是( )A、某档案室着火﹣用水基型灭火器 B、酒精灯着火﹣用湿抹布盖灭 C、森林起火﹣砍伐树木形成隔离带 D、油锅起火﹣用锅盖盖灭8. 如图所示的实验操作,正确的是( )A、
 过滤
B、
过滤
B、 塞紧橡胶塞
C、
塞紧橡胶塞
C、 向试管中加入固体
D、
向试管中加入固体
D、 用滴管滴加液体
9. 下列化学方程式与事实相符且正确的是( )A、碳在氧气中完全燃烧2C+O2 2CO B、用足量澄清石灰水检验二氧化碳:CO2+Ca(OH)2═CaCO3↓+H2O C、铝在空气中发生反应,其表面生成一层致密的氧化铝薄膜:2Al+3O2=Al2O3 D、铁与稀盐酸反应:2Fe+6HCl=2FeCl3+3H2↑10. 下列关于催化剂的说法正确的是( )A、在酿造工业和制药工业,一般都要用酶作催化剂 B、反应前后催化剂的化学性质通常会发生改变 C、在化学反应中二氧化锰是催化剂 D、用氯酸钾制取氧气时,加入催化剂可使生成氧气的质量增加11. 用分子的知识解释生活中的现象,其中合理的是( )A、酒香不怕巷子深,说明分子总是在不断运动 B、水结成冰,是因为温度降低,分子停止运动 C、酒精挥发说明酒精分子的体积增大 D、碳单质在不同条件下燃烧可生成一氧化碳,也可生成二氧化碳,说明同种分子化学性质不同12. 下列物质中,氯元素的化合价最高的是( )A、ClO2 B、HClO C、KClO3 D、Cl213. 在一定条件下,甲和乙反应生成丙的微观示意图如下,则下列说法中错误的是( )
用滴管滴加液体
9. 下列化学方程式与事实相符且正确的是( )A、碳在氧气中完全燃烧2C+O2 2CO B、用足量澄清石灰水检验二氧化碳:CO2+Ca(OH)2═CaCO3↓+H2O C、铝在空气中发生反应,其表面生成一层致密的氧化铝薄膜:2Al+3O2=Al2O3 D、铁与稀盐酸反应:2Fe+6HCl=2FeCl3+3H2↑10. 下列关于催化剂的说法正确的是( )A、在酿造工业和制药工业,一般都要用酶作催化剂 B、反应前后催化剂的化学性质通常会发生改变 C、在化学反应中二氧化锰是催化剂 D、用氯酸钾制取氧气时,加入催化剂可使生成氧气的质量增加11. 用分子的知识解释生活中的现象,其中合理的是( )A、酒香不怕巷子深,说明分子总是在不断运动 B、水结成冰,是因为温度降低,分子停止运动 C、酒精挥发说明酒精分子的体积增大 D、碳单质在不同条件下燃烧可生成一氧化碳,也可生成二氧化碳,说明同种分子化学性质不同12. 下列物质中,氯元素的化合价最高的是( )A、ClO2 B、HClO C、KClO3 D、Cl213. 在一定条件下,甲和乙反应生成丙的微观示意图如下,则下列说法中错误的是( ) A、该反应属于化合反应 B、.反应前后分子的个数没有改变 C、一个X分子中含有三个原子 D、参加反应的甲、乙两种物质质量比为7:414. 如图为A、B、C三种固体物质的溶解度曲线图(A、B、C析出晶体时均不含结晶水),根据曲线图所示,下列说法正确的是( )
A、该反应属于化合反应 B、.反应前后分子的个数没有改变 C、一个X分子中含有三个原子 D、参加反应的甲、乙两种物质质量比为7:414. 如图为A、B、C三种固体物质的溶解度曲线图(A、B、C析出晶体时均不含结晶水),根据曲线图所示,下列说法正确的是( ) A、t2℃ 时,溶解度最大的物质是A B、若将M点处C的不饱和溶液变为饱和溶液,可以选择的方法是降低温度 C、t2℃时,将等质量的A、B、C的饱和溶液都升温到t3℃,溶液中溶剂质量的大小关系是(忽略水的挥发)B>A=C D、t1℃时,将A、B、C三种固体物质分别溶于水所得溶液的溶质质量分数C>A=B15. 食醋是厨房中常用的调味品,它的主要成分是乙酸,乙酸分子的模型如图所示,其中
A、t2℃ 时,溶解度最大的物质是A B、若将M点处C的不饱和溶液变为饱和溶液,可以选择的方法是降低温度 C、t2℃时,将等质量的A、B、C的饱和溶液都升温到t3℃,溶液中溶剂质量的大小关系是(忽略水的挥发)B>A=C D、t1℃时,将A、B、C三种固体物质分别溶于水所得溶液的溶质质量分数C>A=B15. 食醋是厨房中常用的调味品,它的主要成分是乙酸,乙酸分子的模型如图所示,其中 代表一个碳原子,○代表一个氢原子,
代表一个碳原子,○代表一个氢原子,  代表一个氧原子,下列说法不正确的是( )
代表一个氧原子,下列说法不正确的是( )  A、乙酸是一种化合物 B、乙酸的相对分子质量为60 C、乙酸中碳元素的质量分数为60% D、乙酸分子中的碳原子、氢原子、氧原子的个数比为1:2:116. 在配制一定溶质质量分数的氯化钠溶液时,导致溶液中氯化钠的质量分数偏大的可能原因有( )A、用量筒量取水时俯视读数 B、用来配制溶液的烧杯刚用少量蒸馏水润洗过 C、用托盘天平称取氯化钠时,将氯化钠放在右盘,且称量时使用了游码 D、用了含少量杂质的氯化钠配制溶液17. 某化学兴趣小组向一定量AgNO3和Cu(NO3)2混合溶液中加入一定量的Zn粉,充分反应后过滤得溶液A和固体B,滤液A中所含的溶质不可能的情况是( )A、Zn(NO3)2 B、Zn(NO3)2、Cu(NO3)2、AgNO3 C、Zn(NO3)2、Cu(NO3)2 D、Zn(NO3)2、AgNO318. 分子数相同的二氧化硫和三氧化硫,它们的质量比为( )A、1:2 B、2:1 C、4:5 D、5:4
A、乙酸是一种化合物 B、乙酸的相对分子质量为60 C、乙酸中碳元素的质量分数为60% D、乙酸分子中的碳原子、氢原子、氧原子的个数比为1:2:116. 在配制一定溶质质量分数的氯化钠溶液时,导致溶液中氯化钠的质量分数偏大的可能原因有( )A、用量筒量取水时俯视读数 B、用来配制溶液的烧杯刚用少量蒸馏水润洗过 C、用托盘天平称取氯化钠时,将氯化钠放在右盘,且称量时使用了游码 D、用了含少量杂质的氯化钠配制溶液17. 某化学兴趣小组向一定量AgNO3和Cu(NO3)2混合溶液中加入一定量的Zn粉,充分反应后过滤得溶液A和固体B,滤液A中所含的溶质不可能的情况是( )A、Zn(NO3)2 B、Zn(NO3)2、Cu(NO3)2、AgNO3 C、Zn(NO3)2、Cu(NO3)2 D、Zn(NO3)2、AgNO318. 分子数相同的二氧化硫和三氧化硫,它们的质量比为( )A、1:2 B、2:1 C、4:5 D、5:4二、填空题
-
19. 化学就在我们身边,化学与生活息息相关.通过一学期的学习,请你回答下列问题.(1)、在日常生活中饮用水硬度过大的水不利于人体健康,日常生活中常用来区分硬水和软水,可用的方法降低水的硬度,实验室中常用的方法除去不溶于水的杂质.(2)、防毒面具中使用了活性炭,这时利用了活性炭的作用.(3)、天然气的主要成分为(填化学式),其燃烧的化学方程式是 .(4)、煤燃烧生成CO2、SO2、CO等气体,其中会引起温室效应的是;溶于水会形成酸雨的是;能与人体血红蛋白结合的是 .(5)、交警通过酒精检测仪显示的颜色变化,可快速检测出司机是否酒后驾车,其反应原理为2CrO3(红色)+3C2H5OH+3H2SO4═Cr2(SO4)3(绿色)+3CH3CHO+6X,X的化学式为 .(6)、查阅资料可知,米酒味道变酸是因为米酒中产生的醋酸杆菌使乙醇(C2H5OH)和氧气发生反应生成了醋酸(CH3COOH)和另一种常见的液体.食物变质是一种氧化反应(填“剧烈”、“缓慢”).米酒味道变酸的化学反应方程式为;可用验证米酒味道变酸是生成了醋酸.20. 根据下列四种粒子的结构示意图,回答下列问题:
 (1)、以上四种微粒结构示意图共表示种元素.(2)、以上四种微粒中达到稳定结构的是(填序号).(3)、②的单质在③的单质中燃烧时的化学方程式为21. 根据如表回答问题.
(1)、以上四种微粒结构示意图共表示种元素.(2)、以上四种微粒中达到稳定结构的是(填序号).(3)、②的单质在③的单质中燃烧时的化学方程式为21. 根据如表回答问题.温度(℃)
20
40
50
60
80
溶解度(g/100g水)
NaCl
36.0
36.6
37.0
37.3
38.4
NH4Cl
37.2
45.8
50.4
55.2
65.6
KNO3
31.6
63.9
85.5
110
169
①20℃时,溶解度最大的物质是
②50℃时,100g水中最多溶解NaClg
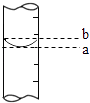
③量筒的局部示意见图,量取水时应沿视线(选填“a”或“b”)进行读数,视线(选填“a”或“b”)对应的读数较大.
④A是80℃含有120g水的KNO3溶液,经过如下操作,得到102gKNO3固体.

Ⅰ.A溶液为(选填“饱和”或“不饱和”)溶液
Ⅱ.对以上过程的分析,正确的是(选填编号)
a.A到B的过程中,溶质质量没有改变
b.B中溶质与溶剂的质量比为169:100
c.开始析出KNO3固体的温度在60℃至80℃之间
d.A溶液的质量等于222g.
三、解答题
-
22. 实验室常用下列装置来制取、收集气体.仪器b是分液漏斗,可通过旋转活塞分次滴加液体.请回答以下问题.
 (1)、仪器a、c的名称是:a , c .(2)、实验室用KMnO4制取O2 , 应选用的发生装置和收集装置(收集一瓶纯净的氧气)的组合为(填字母序号),该发生装置的不足之处是 , 该反应的化学方程式是 . 用排水法收集气体时判断气体满的方法是 .(3)、实验室要制取CO2可选择的发生装置(填字母序号);要制取少量CO2应选择的较简单的发生装置是(填字母序号);该反应的化学方程式是 .(4)、化学反应可控制才能更好地为人类造福,我们可以通过改变反应的条件、药品用量、改进装置等途径来达到控制反应的目的.常温下块状电石(CaC2)与水反应生成乙炔 (C2H2)气体和氢氧化钙,该反应的化学方程式是 , 实验室制取乙炔时,须严格控制加水速度,以免剧烈反应放热引起装置炸裂.图中适合制取乙炔气体的发生装置有(填装置序号).23. 利用表中装置进行下列实验,已知:白磷的着火点为40℃.
(1)、仪器a、c的名称是:a , c .(2)、实验室用KMnO4制取O2 , 应选用的发生装置和收集装置(收集一瓶纯净的氧气)的组合为(填字母序号),该发生装置的不足之处是 , 该反应的化学方程式是 . 用排水法收集气体时判断气体满的方法是 .(3)、实验室要制取CO2可选择的发生装置(填字母序号);要制取少量CO2应选择的较简单的发生装置是(填字母序号);该反应的化学方程式是 .(4)、化学反应可控制才能更好地为人类造福,我们可以通过改变反应的条件、药品用量、改进装置等途径来达到控制反应的目的.常温下块状电石(CaC2)与水反应生成乙炔 (C2H2)气体和氢氧化钙,该反应的化学方程式是 , 实验室制取乙炔时,须严格控制加水速度,以免剧烈反应放热引起装置炸裂.图中适合制取乙炔气体的发生装置有(填装置序号).23. 利用表中装置进行下列实验,已知:白磷的着火点为40℃.实验装置
实验1
实验2

Ⅰ.将盛有足量锌粒的燃烧匙伸入瓶中,塞紧瓶塞
Ⅱ.打开K,从长颈漏斗向瓶内加入稀盐酸,至浸没锌粒
Ⅲ.当瓶中产生大量气泡时,关闭K
Ⅰ.将盛有白磷的燃烧匙伸入瓶内,塞紧瓶塞
Ⅱ.打开K,从长颈漏斗向瓶内加入约80℃的热水,至浸没白磷
Ⅲ.从a口向瓶中鼓入空气,使瓶中液面低于燃烧匙底部,关闭K
(1)、连接仪器后,关闭K,加水至长颈漏斗内液面高于瓶中液面,一段时间后,液面高度保持不变,该现象说明 .(2)、实验Ⅰ中,瓶内发生反应的化学方程式为 , 步骤Ⅲ中,关闭K后的现象是 .(3)、实验2中,仅对比步骤Ⅱ和Ⅲ可知,欲探究的燃烧条件是 .四、解答题
-
24. 现有含氧化铁80%(其他成分不含铁)的赤铁矿400t,能炼出含铁98%的生铁多少吨?(计算结果保留1位小数)