2015-2016学年北京市海淀区普通中学高三下学期开学化学试卷(2月份)
试卷更新日期:2017-04-28 类型:开学考试
一、选择题
-
1. 已知KH和H2O反应生成H2和KOH,反应中1mol KH( )A、失去1mol电子 B、得到1mol电子 C、失去2mol电子 D、没有电子得失2. 如表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )
 A、常压下五种元素的单质中,Z单质的沸点最高 B、Y、Z的阴离子电子层结构都与R原子的相同 C、Y的氢化物的沸点比H2O的沸点高 D、Y元素的非金属性比W元素的非金属性强3. 下列关于浓硫酸的叙述,正确的是( )A、浓硫酸具有吸水性,因而能使蔗糖炭化 B、浓硫酸在常温下可迅速与铜片反应放出二氧化硫气体 C、浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体 D、浓硫酸在常温下能够使铁、铝等金属钝化4. 下列分子式中,所有原子不可能共处在同一平面上的是( )A、C2H2 B、CS2 C、NH3 D、C6H65. 绿色化学对于化学反应提出了“原子经济性”的新概念及要求.理想的原子经济性反应是原料分子中的原子全部转变成所需产物,不产生副产物,实现零排放.下列几种生产乙苯的方法中,原子经济性最好的是( )A、
A、常压下五种元素的单质中,Z单质的沸点最高 B、Y、Z的阴离子电子层结构都与R原子的相同 C、Y的氢化物的沸点比H2O的沸点高 D、Y元素的非金属性比W元素的非金属性强3. 下列关于浓硫酸的叙述,正确的是( )A、浓硫酸具有吸水性,因而能使蔗糖炭化 B、浓硫酸在常温下可迅速与铜片反应放出二氧化硫气体 C、浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体 D、浓硫酸在常温下能够使铁、铝等金属钝化4. 下列分子式中,所有原子不可能共处在同一平面上的是( )A、C2H2 B、CS2 C、NH3 D、C6H65. 绿色化学对于化学反应提出了“原子经济性”的新概念及要求.理想的原子经济性反应是原料分子中的原子全部转变成所需产物,不产生副产物,实现零排放.下列几种生产乙苯的方法中,原子经济性最好的是( )A、 +C2H5Cl→
+C2H5Cl→  +HCl
B、
+HCl
B、 +C2H5OH→
+C2H5OH→  +H2O
C、
+H2O
C、 +CH2=CH2→
+CH2=CH2→  D、
D、 →
→  +HBr
+HBr
二、解答题
-
6. 芳香化合物A、B互为同分异构体,B的结构筒式是
 .A经①、②两步反应得C、D和E.B经①、②两步反应得E、F和H.上述反应过程、产物性质及相互关系如图所示.
.A经①、②两步反应得C、D和E.B经①、②两步反应得E、F和H.上述反应过程、产物性质及相互关系如图所示. (提示:
 )
) (1)、写出E的结构简式 .(2)、A有2种可能的结构,写出相应的结构简式 .(3)、F和小粒金属钠反应的化学方程式是 , 实验现象是 , 反应类型是 .(4)、写出F在浓H2SO4作用下在170℃发生反应的化学方程式:实验现象是 , 反应类型是 .(5)、写出F与H在加热和浓H2SO4催化作用下发生反应的化学方程式 , 实验现象是 , 反应类型是 .(6)、在B、C、D、F、G、I化合物中,互为同系物的是 .7. 在一定条件下,烯烃可发生臭氧化还原水解反应,生成羰基化合物,该反应可表示为:
(1)、写出E的结构简式 .(2)、A有2种可能的结构,写出相应的结构简式 .(3)、F和小粒金属钠反应的化学方程式是 , 实验现象是 , 反应类型是 .(4)、写出F在浓H2SO4作用下在170℃发生反应的化学方程式:实验现象是 , 反应类型是 .(5)、写出F与H在加热和浓H2SO4催化作用下发生反应的化学方程式 , 实验现象是 , 反应类型是 .(6)、在B、C、D、F、G、I化合物中,互为同系物的是 .7. 在一定条件下,烯烃可发生臭氧化还原水解反应,生成羰基化合物,该反应可表示为: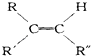
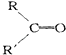 +
+ 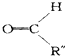 .
.已知:
①化合物A,其分子式为C9H10O,它既能使溴的四氯化碳溶液褪色,又能与FeCl3溶液发生显色反应,且能与金属钠或氢氧化钠溶液反应生成B;
②B发生臭氧化还原水解反应生成C,C能发生银镜反应;
③C催化加氢生成D,D在浓硫酸存在下加热生成E;
④E既能使溴的四氯化碳溶液褪色,又能与FeCl3溶液发生显色反应,且能与氢氧化钠溶液反应生成F;
⑤F发生臭氧化还原水解反应生成G,G能发生银镜反应,遇酸转化为H(C7H6O2).
请根据上述信息,完成下列填空:
(1)、写出下列化合物的结构简式(如有多组化合物符合题意,只要写出其中的一组)A , C , E .
(2)、写出分子式为C7H6O2的含有苯环的所有同分异构体的结构简式 .8. 某有机化合物A的相对分子质量(分子量)大于110,小于150.经分析得知,其中碳和氢的质量分数之和为52.24%,其余为氧.请回答:(1)、该化合物分子中含有个氧原子,为什么?(2)、该化合物的相对分子质量(分子量)是 .(3)、该化合物的化学式(分子式)是 .(4)、该化合物分子中最多含个 官能团. 9. 有A、B、C、D、E、F、G七瓶不同物质的溶液,它们各是:Na2CO3、Na2SO4、KCl、AgNO3、MgCl2、Ca(NO3)2和Ba(OH)2溶液中的一种.为了鉴别,各取少量溶液进行两两混合,实验结果如下表所示.表中“↓”表示生成沉淀或微溶化合物,“﹣”表示观察不到明显变化.试回答下面问题:(1)、A的化学式是 , G的化学式是 , 判断的理由是 .(2)、写出其余几种物质的化学式.B:C:D:E:F: .
官能团. 9. 有A、B、C、D、E、F、G七瓶不同物质的溶液,它们各是:Na2CO3、Na2SO4、KCl、AgNO3、MgCl2、Ca(NO3)2和Ba(OH)2溶液中的一种.为了鉴别,各取少量溶液进行两两混合,实验结果如下表所示.表中“↓”表示生成沉淀或微溶化合物,“﹣”表示观察不到明显变化.试回答下面问题:(1)、A的化学式是 , G的化学式是 , 判断的理由是 .(2)、写出其余几种物质的化学式.B:C:D:E:F: .A
B
C
D
E
F
G
A
﹣
﹣
﹣
﹣
﹣
﹣
↓
B
﹣
﹣
﹣
﹣
↓
↓
↓
C
﹣
﹣
﹣
↓
﹣
↓
↓
D
﹣
﹣
↓
﹣
↓
↓
↓
E
﹣
↓
﹣
↓
﹣
↓
﹣
F
﹣
↓
↓
↓
↓
﹣
↓
G
↓
↓
↓
↓
﹣
↓
﹣
10. A、B、C、D是4种可溶的化合物,分别由阳离子K+、Ba2+、Al3+、Fe3+和阴离子OH﹣、CO32﹣、NO3﹣、SO42﹣两两组合而成,它们的溶液发生如下反应:A与B反应生成白色沉淀,再加过量A,沉淀量减少,但不会完全消失;C与D反应生成有色沉淀;B与C 反应生成白色沉淀.写出它们的化学式:A , B , C , D .11. 有三种不同质量比的氧化铜与炭粉的混合物样品①、②、③.甲、乙、丙三同学各取一种样品,加强热充分反应,测定各样品中氧化铜的量.(1)、甲取样品①强热,若所得固体为金属铜,将其置于足量的稀硝酸中微热,产生1.12L气体(标准状况),则样品①中氧化铜的质量为g.(2)、乙取样品②ag强热,生成的气体不能使澄清的石灰水变浑浊.再将反应后的固体与足量的稀硝酸微热,充分反应后,有bg固体剩余,该剩余固体的化学式为 . 样品②中氧化铜质量为g(以含a、b的代数式表示).
(3)、丙称量样品③强热后剩余的固体,质量比原样品减小了cg,若该固体为金属铜,则样品③中氧化铜物质的量(n)的取值范围为 .12. 根据下图及描述,回答下列问题:
(1)、关闭图A装置中的止水夹a后,从长颈漏斗向试管中注入一定量的水,静置后如图所示.试判断:A装置是否漏气?(填“漏气”、“不漏气”或“无法确定”) , 判断理由: .(2)、关闭图B装置中的止水夹a后,开启活塞b,水不断往下滴,直至全部流入烧瓶.试判断:B装置是否漏气?(填“漏气”、“不漏气”或“无法确定”) , 判断理由: .