广东省深圳市罗湖区2018-2019学年九年级上学期化学期末考试试卷
试卷更新日期:2019-03-15 类型:期末考试
一、单选题
-
1. 下列标志表示“节约用水”的是( )A、
 B、
B、 C、
C、 D、
D、 2. 空气被称为“生命气体”,有关空气的说法中错误的是( )A、酸雨与空气污染有关 B、焊接金属时,可用氮气作保护气 C、空气中稀有气体的质量分数为0.94% D、人体呼出的气体中CO2含量比吸入时的高3. 实验室中用量筒量取7mL水时,读数时视线仰视(视线和刻度线在同一侧),所量的实际体积( )A、等于7mL B、小于7mL C、大于7mL D、无法确定4. 关于“蜡烛及其燃烧”,以下说法正确的是( )
2. 空气被称为“生命气体”,有关空气的说法中错误的是( )A、酸雨与空气污染有关 B、焊接金属时,可用氮气作保护气 C、空气中稀有气体的质量分数为0.94% D、人体呼出的气体中CO2含量比吸入时的高3. 实验室中用量筒量取7mL水时,读数时视线仰视(视线和刻度线在同一侧),所量的实际体积( )A、等于7mL B、小于7mL C、大于7mL D、无法确定4. 关于“蜡烛及其燃烧”,以下说法正确的是( ) A、“蜡炬成灰泪始干”只发生了物理变化 B、蜡烛中含有的碳元素属于非金属元素 C、燃烧产物中只有水属于氧化物 D、石蜡和太阳能都属于化石能源5. 下列原子具有相对稳定结构的是( )A、
A、“蜡炬成灰泪始干”只发生了物理变化 B、蜡烛中含有的碳元素属于非金属元素 C、燃烧产物中只有水属于氧化物 D、石蜡和太阳能都属于化石能源5. 下列原子具有相对稳定结构的是( )A、 B、
B、 C、
C、 D、
D、 6. 关于物质“K2MnO4”的说法,正确的是( )
6. 关于物质“K2MnO4”的说法,正确的是( ) A、该物质名称是高锰酸钾 B、K2MnO4中含2个O2 C、其中Mn的化合价是+6 D、据图可知,氧原子核内有16个质子7. 分类法是化学学习中常用的方法。下列分类正确的是( )A、大气污染物:CO、SO2 B、化学性质:沸点、可燃性 C、可加热仪器:试管、集气瓶 D、单质:干冰、氧气8. 实验室中制取、收集CO2 , 并验满,以下各步操作中正确的是( )A、
A、该物质名称是高锰酸钾 B、K2MnO4中含2个O2 C、其中Mn的化合价是+6 D、据图可知,氧原子核内有16个质子7. 分类法是化学学习中常用的方法。下列分类正确的是( )A、大气污染物:CO、SO2 B、化学性质:沸点、可燃性 C、可加热仪器:试管、集气瓶 D、单质:干冰、氧气8. 实验室中制取、收集CO2 , 并验满,以下各步操作中正确的是( )A、 检査气密性
B、
检査气密性
B、 添加大理石
C、
添加大理石
C、 收集
D、
收集
D、 验满
9. 下列反应,既不属于分解反应,也不属于化合反应的是( )A、C+O2
验满
9. 下列反应,既不属于分解反应,也不属于化合反应的是( )A、C+O2 CO2
B、Cl2+2 NaOH=NaClO+NaCl+H2O
C、2HgO
CO2
B、Cl2+2 NaOH=NaClO+NaCl+H2O
C、2HgO 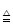 2Hg+O2↑
D、CuSO4+5H2O=CuSO4•5H2O
10. 有关“水”的说法正确的是( )A、由于热胀冷缩的缘故,水沸腾时分子会变大 B、水电解所生成氢气和氧气的质量比为2:1 C、湖水经沉淀、吸附处理后,即可得纯水 D、任意排放工业和生活废水,会导致水体污染11. 乘坐高铁时,易燃易爆品不许携带上车,以防爆炸造成危害,其中包括( )
2Hg+O2↑
D、CuSO4+5H2O=CuSO4•5H2O
10. 有关“水”的说法正确的是( )A、由于热胀冷缩的缘故,水沸腾时分子会变大 B、水电解所生成氢气和氧气的质量比为2:1 C、湖水经沉淀、吸附处理后,即可得纯水 D、任意排放工业和生活废水,会导致水体污染11. 乘坐高铁时,易燃易爆品不许携带上车,以防爆炸造成危害,其中包括( )①蔗糖;②饮料;③爆竹;④汽油;⑤香烟
A、①② B、③⑤ C、④⑤ D、③④12. 干粉灭火器的灭火原理是利用压缩的CO2吹出干粉(主要成分是碳酸氢钠和磷酸铵盐)。以下有关说法正确的是( )A、灭火时要朝向火焰的最上方喷射 B、灭火时降低了可燃物的着火点 C、(NH4)3PO4中N:H:O的原子个数比为1:4:4 D、NaHCO3中氧元素的质量分数表达式为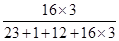 ×100%
13. 下列说法中错误的是( )A、把秸秆、杂草在密闭池中发酵可产生甲烷 B、不锈钢比纯铁抗腐蚀,但硬度不如纯铁 C、铁制品在潮湿的空气因发生缓慢氧化而生锈 D、煤制成蜂窝状后燃烧更旺是因为增大了煤与空气的接触面积14. 甲、乙、丙、丁是四种不同的物质,它们在反应前后的质量变化如图所示。下列有关说法错误的是( )
×100%
13. 下列说法中错误的是( )A、把秸秆、杂草在密闭池中发酵可产生甲烷 B、不锈钢比纯铁抗腐蚀,但硬度不如纯铁 C、铁制品在潮湿的空气因发生缓慢氧化而生锈 D、煤制成蜂窝状后燃烧更旺是因为增大了煤与空气的接触面积14. 甲、乙、丙、丁是四种不同的物质,它们在反应前后的质量变化如图所示。下列有关说法错误的是( ) A、x的值是7 B、丁一定是化合物 C、甲和丁质量变化比为4:11 D、丙可能是不参加反应的杂质15. 下列物质在给定条件下的转化均能一步实现的是( )A、CuCl2溶液
A、x的值是7 B、丁一定是化合物 C、甲和丁质量变化比为4:11 D、丙可能是不参加反应的杂质15. 下列物质在给定条件下的转化均能一步实现的是( )A、CuCl2溶液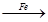 Cu
Cu 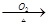 CuO
B、H2O2
CuO
B、H2O2 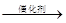 H2
H2 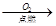 H2O
C、CaCl2溶液
H2O
C、CaCl2溶液 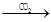 CaCO3
CaCO3  CO2
D、Fe3O4
CO2
D、Fe3O4 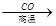 Fe
Fe  FeCl3
16. 以下实验方案不能达到目的是( )
FeCl3
16. 以下实验方案不能达到目的是( )选项
实验目的
实验方案
A
除杂:N2中混有O2
通过灼热的铜网
B
分离:水和泥沙
用活性炭吸附
C
检验:CO2中含有的水蒸气
通过无水硫酸铜
D
区别:硬水和软水
用肥皂水区分
A、A B、B C、C D、D17. 利用催化剂可有效消除有害气体甲醛(CH2O),其反应的微观示意图如图。下列说法中错误的是( )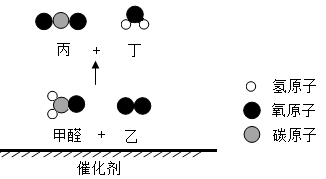 A、乙的化学式是O2 B、丙的相对分子质量是44 C、该反应类型属于置换反应 D、该反应可用来减少甲醛的危害18. 以下转化关系中均是初中化学常见物质,有关说法正确的是( )
A、乙的化学式是O2 B、丙的相对分子质量是44 C、该反应类型属于置换反应 D、该反应可用来减少甲醛的危害18. 以下转化关系中均是初中化学常见物质,有关说法正确的是( ) A、反应①的化学方程式为C+CuO
A、反应①的化学方程式为C+CuO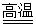 CO2+Cu
B、反应②中物质A表现了还原性
C、反应③的现象为红棕色固体变为银白色
D、溶液D一定是CuSO4溶液
19. 下列排序正确的是( )A、最外层电子数:
CO2+Cu
B、反应②中物质A表现了还原性
C、反应③的现象为红棕色固体变为银白色
D、溶液D一定是CuSO4溶液
19. 下列排序正确的是( )A、最外层电子数: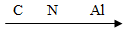 渐多
B、地壳中的元素含量:
渐多
B、地壳中的元素含量: 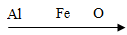 渐多
C、金属活动性顺序:
渐多
C、金属活动性顺序:  渐强
D、物质颜色:
渐强
D、物质颜色: 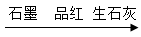 渐深
20. 下列实验能达到实验目的是( )
渐深
20. 下列实验能达到实验目的是( )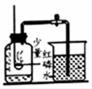

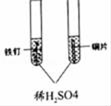

A.探究空气中氧气含量
B.验证甲烷(CH4)燃烧生成二氧化碳和水
C.探究铁、铜的金属活动性强弱
D.称量固体药品
A、A B、B C、C D、D二、综合题
-
21. 图示为“铁丝在O2中燃烧”的实验改进装置(浓硫酸具有吸水性,可干燥氧气)。
 (1)、图一甲装置:固体是二氧化锰,其作用是;发生反应的化学方程式为;图一丙装置:铁丝在O2中燃烧,观察到的实验现象是;用塑料瓶代替集气瓶的优点之一是;
(1)、图一甲装置:固体是二氧化锰,其作用是;发生反应的化学方程式为;图一丙装置:铁丝在O2中燃烧,观察到的实验现象是;用塑料瓶代替集气瓶的优点之一是;请在图二中作出随着时间的变化甲中生成O2质量的关系曲线(在答题卡中画出)。
(2)、实验室用氯酸钾和二氧化锰制取O2 , 正确的操作顺序是(选填序号);①点燃酒精灯,给试管加热;②熄灭酒精灯;③检查装置的气密性;
④将氯酸钾和二氧化锰的混合物装入试管中,并连好导管,将试管固定在铁架台上;
⑤用排水集气法收集氧气;⑥将导管从水槽中取出。
(3)、在潜水艇中提供氧气的反应原理之一是:2Na2O2(固体)+2H2O═4NaOH+O2↑(如图三所示),实验室中可用装置来模拟其制取过程(选填字母序号)。
22. 铜是人类最早利用的金属之一。
(1)、
用“﹣”连接金属铜的性质与用途(要求:性质不重复选择)。(2)、利用废旧电池铜帽(含Cu、Zn)制取海绵铜(Cu),并得到硫酸锌溶液,主要流程如下(反应条件和部分产物已略去):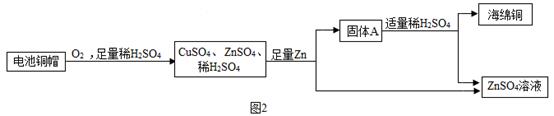 已知:2Cu+2H2SO4+O2 2CuSO4+2H2O
已知:2Cu+2H2SO4+O2 2CuSO4+2H2O根据上述信息,可推得:固体A的成分是(写化学式);它属于(选填“纯净物”或者“混合物”),过程①②③中发生了相同化学反应,其化学方程式为 , 过程②中分离操作的名称是;实验室中进行该操作,常用的玻璃仪器除了烧杯和漏斗,还有。
三、科学探究题
-
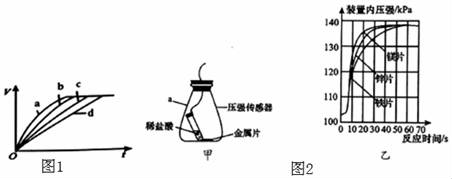
23. 控制变量法是科学探究中常用的方法。化学反应的快慢常与外界条件有关,如温度、压强、催化剂、固体表面积等因素。以下实验设计的目的是探究化学反应快慢与外界条件的关系。(1)、Ⅰ.现有四份等质量的铁分别与足量的盐酸进行反应,图1为随着反应时间的变化产生气体体积V的关系曲线。四组实验条件分别是:
a.50℃、铁粉
b.30℃、铁粉
c.30℃、铁丝
d.20℃、铁丝
请写出铁与盐酸反应的化学方程式: , 该反应进行时会放出热量。
(2)、通过实验a和b对比,得出的结论是;若要比较金属铁的表面积对反应快慢的影响,应选择的实验组别是。实验中观察到产生气体“逐渐变快又变慢”,请解释“逐渐变快”的原因是。(3)、Ⅱ.常温时,用足量的铁、锌、镁三种金属片分别与等量盐酸反应,图2中,甲图为实验发生装置,乙图为测得的产生氢气的量(图中压强越大,表示产生氢气的量越多)。①该实验中,你认为还需要控制的变量是;
②根据乙图,得出反应物的量与生成H2体积的关系是。
(4)、若足量的镁片与盐酸反应,测得产生H2的实际值比理论值偏大,请分析可能的原因(写出一条即可):。
 24. 取四份大理石样品分别和稀盐酸反应,实验数据记录如下表。(杂质既不溶于水也不跟酸反应)
24. 取四份大理石样品分别和稀盐酸反应,实验数据记录如下表。(杂质既不溶于水也不跟酸反应)第1份
第2份
第3份
第4份
大理石样品质量(g)
3.0
3.0
3.0
3.0
稀盐酸质量(g)
5.0
10.0
15.0
20.0
产生气体质量(g)
0.44
0.88
0.99
X
回答下列有关问题:
(1)、仔细观察第1份和第2份实验数据,会发现生成气体的质量不相同。据此判断,在第1份样品的实验中,(填“大理石”或者“稀盐酸”)完全反应;生成的气体通入澄清石灰水中,发生反应的化学方程式为;(2)、同理,比较第2份和第3份实验数据,可以判断其中第份大理石样品反应完全。那么,第4份数据中的x值应该为;(3)、计算:该大理石样品中碳酸钙的质量分数。(依据化学方程式,写出计算过程)