吉林省四平市伊通县2018-2019学年九年级上学期化学期末考试试卷
试卷更新日期:2019-02-26 类型:期末考试
一、单选题
-
1. 物质的下列性质中,属于化学性质的是( )A、可燃性 B、状态 C、气味 D、硬度2. 空气是一种宝贵的资源,空气中体积分数最大的气体是( )A、稀有气体 B、二氧化碳 C、氧气 D、氮气3. 生活中可以使硬水软化成软水的常用方法是( )A、沉降 B、消毒 C、煮沸 D、过滤4. 下列实验操作正确的是( )A、
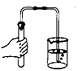 检查装置气密性
B、
检查装置气密性
B、 熄灭酒精灯
C、
熄灭酒精灯
C、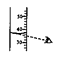 量取液体
D、
量取液体
D、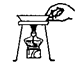 移走蒸发皿
5. 下列物质在点燃前不需验纯的是( )A、氢气 B、硫磺 C、一氧化碳 D、甲烷6. 化学方程式_____+3CO 2Fe+3CO2中,所缺物质的化学式为( )A、FeO B、Fe2O3 C、Fe3O4 D、FeCO37. “保护好我们的环境”是每位公民应尽的义务。下列说法正确的是( )A、农药本身有毒,应该禁止施用农药 B、有害气体和烟尘会对空气造成污染 C、煤燃烧产生的二氧化碳会造成酸雨 D、工业废水不经处理就可以排放到江河里8. 关于电解水实验的下列说法中正确的是( )A、从现象上判断:正极产生的是氢气 B、从变化上分类:该变化属于物理变化 C、从宏观上分析:水是由氢气和氧气组成的 D、从微观上分析:水分子是由氢原子和氧原子构成的9. 下列实验设计能够实现其对应实验目的的是( )A、
移走蒸发皿
5. 下列物质在点燃前不需验纯的是( )A、氢气 B、硫磺 C、一氧化碳 D、甲烷6. 化学方程式_____+3CO 2Fe+3CO2中,所缺物质的化学式为( )A、FeO B、Fe2O3 C、Fe3O4 D、FeCO37. “保护好我们的环境”是每位公民应尽的义务。下列说法正确的是( )A、农药本身有毒,应该禁止施用农药 B、有害气体和烟尘会对空气造成污染 C、煤燃烧产生的二氧化碳会造成酸雨 D、工业废水不经处理就可以排放到江河里8. 关于电解水实验的下列说法中正确的是( )A、从现象上判断:正极产生的是氢气 B、从变化上分类:该变化属于物理变化 C、从宏观上分析:水是由氢气和氧气组成的 D、从微观上分析:水分子是由氢原子和氧原子构成的9. 下列实验设计能够实现其对应实验目的的是( )A、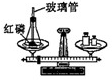 验证质量守恒定律
B、
验证质量守恒定律
B、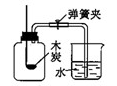 测定空气中氧气的含量
C、
测定空气中氧气的含量
C、 探究铁钉锈蚀的条件
D、
探究铁钉锈蚀的条件
D、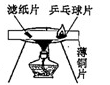 探究燃烧的条件之一:温度达到着火点
10. 推理是化学学习中常用的思维方法,下列推理正确的是( )A、化合物是由不同种元素组成的,所以由不同种元素组成的纯净物一定是化合物 B、原子是不带电的微粒,所以不带电的微粒一定是原子 C、燃烧需要氧气,所以物质与氧气的反应都属于燃烧 D、铝的化学性质比较活泼,所以在空气中铝比铁更容易被腐蚀
探究燃烧的条件之一:温度达到着火点
10. 推理是化学学习中常用的思维方法,下列推理正确的是( )A、化合物是由不同种元素组成的,所以由不同种元素组成的纯净物一定是化合物 B、原子是不带电的微粒,所以不带电的微粒一定是原子 C、燃烧需要氧气,所以物质与氧气的反应都属于燃烧 D、铝的化学性质比较活泼,所以在空气中铝比铁更容易被腐蚀二、填空题
-
11. 用化学用语填空。(1)、两个氮分子;(2)、三个硫酸根离子;(3)、铁丝在氧气中燃烧产物的化学式。12. 高纯硅是制造“芯片”的重要材料。根据右图回答下列问题。
 (1)、硅原子的相对原子质量是;(2)、硅原子的最外层电子数n=;(3)、沙子的主要成分是SiO2 , SiO2中硅元素的化合价为价。
(1)、硅原子的相对原子质量是;(2)、硅原子的最外层电子数n=;(3)、沙子的主要成分是SiO2 , SiO2中硅元素的化合价为价。三、简答题
-
13. 能源在人们的生产生活中起着及其重要的作用,请回答下列问题。(1)、煤燃烧时会产生多种危害,请你举出一例;(2)、玉米等发酵可得到酒精,酒精是的俗称;(3)、天然气的主要成分是(写化学式) , 这种物质燃烧的化学方程式是。14. 结合化学知识回答下列问题。(1)、试举一个能说明分子之间有间隔的例子:;(2)、CO2与CO的化学性质有很大不同的原因是。15. 水是一种宝贵的资源,请回答下列问题。(1)、请举出你在生活中节约用水的一种做法;(2)、电解水实验和实验都能得出水是由氢氧两种元素组成的结论;(3)、做硫在氧气中燃烧实验时,在集气瓶底部放入一些水,其作用是。16. 用铝丝、洁净的铜丝、稀盐酸、AgNO3溶液,验证Al、Cu Ag的活动性顺序。(1)、把打磨过的铝丝和洁净的铜丝分别浸入稀盐酸中,观察到铝丝表面有气泡产生,铜丝表面无明显现象,由此判断出Al和Cu的活动性强弱顺序为>(H)>;发生反应的基本反应类型是 ;铝丝使用前需用砂纸打磨的原因是;(2)、为了达到实验目的,除(1)中实验外,还需要进行的实验是。
四、实验题
-
17. 如图是老师在化学课上学习二氧化碳的性质时做的实验。
 (1)、实验前,检验瓶中二氧化碳已集满的方法;(2)、该实验的现象是;(3)、实验后,老师在瓶中液体里滴加了几滴紫色石蕊溶液,发现石蕊溶液变成红色,写出瓶中发生反应的化学方程式。18. 如图是实验室制取气体的常用装置。
(1)、实验前,检验瓶中二氧化碳已集满的方法;(2)、该实验的现象是;(3)、实验后,老师在瓶中液体里滴加了几滴紫色石蕊溶液,发现石蕊溶液变成红色,写出瓶中发生反应的化学方程式。18. 如图是实验室制取气体的常用装置。 (1)、仪器a的名称是。(2)、选择恰当的装置可用来加热高锰酸钾制取氧气,发生反应的化学方程式为:。用E装置收集氧气时,待集气瓶里的水排完后, , 正放在桌面上。(3)、若选择上述装置制取二氧化碳气体时,连接装置,在加入药品前应进行的操作步骤是;应选择的发生装置和最佳收集装置是。(填写字母代号)
(1)、仪器a的名称是。(2)、选择恰当的装置可用来加热高锰酸钾制取氧气,发生反应的化学方程式为:。用E装置收集氧气时,待集气瓶里的水排完后, , 正放在桌面上。(3)、若选择上述装置制取二氧化碳气体时,连接装置,在加入药品前应进行的操作步骤是;应选择的发生装置和最佳收集装置是。(填写字母代号)五、科学探究题
-
19. 我们的日常生活离不开金属。
 (1)、如图是生活中常见“暖贴”的部分标签。暖贴可以贴于身体的某个部位,自行发热,其发热的反应原理与铁生锈原理相似。
(1)、如图是生活中常见“暖贴”的部分标签。暖贴可以贴于身体的某个部位,自行发热,其发热的反应原理与铁生锈原理相似。①暖贴中活性炭具有作用,使用时空气进入暖贴,空气中的氧气与暖贴中的发生反应而使暖贴放热。
②使用后,发现暖贴内有的物质变为红色,该红色固体主要成分的化学式为。
(2)、目前常用的1元硬币为钢芯镀镍合金,5角硬币为铜锌合金或钢芯镀铜合金,1角硬币为铝锌合金或不锈钢,请回答下列问题。①铸造币的合金不需考虑的是。
A.耐磨性 B.抗腐蚀性 C.色泽 D.导电性 E.价格
②硬币涉及的金属有Al、Ni(镍)、Zn、Cu、Fe,已知Ni能发生如下反应:
Ni+H2 SO4=NiSO4+H2↑ Fe+NiSO4═Ni+FeSO4
以上5种金属活动性由强到弱的顺序是。
③Ni与AgNO3溶液(填“能”或“不能”)反应。
④将一枚以铜锌合金为材质的5角硬币投入稀硫酸中,发生反应的化学方程式为。
六、计算题
-
20. 为测定石灰石中碳酸钙的含量,取2.5g石灰石样品,逐渐加入足量稀盐酸,充分反应后测得剩余固体与加入稀盐酸的质量关系如图所示(杂质不参与反应,也不溶于水)。
 (1)、石灰石样品中碳酸钙的质量为g。(2)、碳酸钙中钙元素的质量分数是。(3)、反应中生成二氧化碳的质量是多少?(写出计算过程)
(1)、石灰石样品中碳酸钙的质量为g。(2)、碳酸钙中钙元素的质量分数是。(3)、反应中生成二氧化碳的质量是多少?(写出计算过程)
-