吉林省吉林市丰满区2018-2019学年九年级上学期化学期末考试试卷
试卷更新日期:2019-02-26 类型:期末考试
一、单选题
-
1. 空气中能供给呼吸、支持燃烧的气体( )A、氮气 B、氧气 C、稀有气体 D、二氧化碳2. 下列物质的性质中,属于物理性质的是( )A、石蜡能熔化 B、纸张能燃烧 C、食物易变质 D、一氧化碳有毒3. 在我们生活的物质世界里,存在着形形色色的物质。下列物质中属于纯净物的是( )A、白酒 B、食醋 C、干冰 D、空气4. 走过花圃会闻到花香,是因为分子( )A、不断运动 B、质量小 C、体积小 D、有间隔5. “水是生命之源”。下列有关净化水的单一操作中,净化程度最高的是( )A、沉降 B、沉淀 C、过滤 D、蒸馏6. 如图所示实验操作规范的是( )A、将铁钉放入试管
 B、氢气验纯
B、氢气验纯  C、移走蒸发皿
C、移走蒸发皿  D、合作滴加液体
D、合作滴加液体  7. 某物质 R 在氧气中燃烧的化学方程式为:R + 3O2 2CO2 + 3H2O,则 R 的化学式为( )A、C2H6O B、C2H4 C、CH4 D、CO8. 下列鉴别物质的方法,能够达到目的的是( )A、用品尝的方法鉴别硬水、软水和食盐水 B、用燃着的木条鉴别二氧化碳、氧气和氮气 C、用点燃的方法鉴别氢气、一氧化碳和甲烷 D、用观察颜色的方法鉴别氧化铁、氧化镁和二氧化锰9. 推理是化学学习中常用的思维方法,下列推理正确的是( )A、混合物中至少含有两种物质,则混合物中至少含有两种元素 B、氧化物中一定含有氧元素,则含有氧元素的纯净物一定是氧化物 C、化学变化伴随有能量变化,则有能量变化的变化一定是化学变化 D、原子得失电子后转变成离子,则离子得失电子后也能转变成原子10. 下列实验设计能够实现其对应实验目的的是( )A、
7. 某物质 R 在氧气中燃烧的化学方程式为:R + 3O2 2CO2 + 3H2O,则 R 的化学式为( )A、C2H6O B、C2H4 C、CH4 D、CO8. 下列鉴别物质的方法,能够达到目的的是( )A、用品尝的方法鉴别硬水、软水和食盐水 B、用燃着的木条鉴别二氧化碳、氧气和氮气 C、用点燃的方法鉴别氢气、一氧化碳和甲烷 D、用观察颜色的方法鉴别氧化铁、氧化镁和二氧化锰9. 推理是化学学习中常用的思维方法,下列推理正确的是( )A、混合物中至少含有两种物质,则混合物中至少含有两种元素 B、氧化物中一定含有氧元素,则含有氧元素的纯净物一定是氧化物 C、化学变化伴随有能量变化,则有能量变化的变化一定是化学变化 D、原子得失电子后转变成离子,则离子得失电子后也能转变成原子10. 下列实验设计能够实现其对应实验目的的是( )A、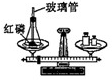 验证质量守恒定律
B、
验证质量守恒定律
B、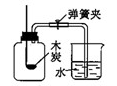 测定空气中氧气的含量
C、
测定空气中氧气的含量
C、 探究铁钉锈蚀的条件
D、
探究铁钉锈蚀的条件
D、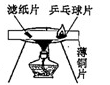 探究燃烧的条件之一:温度达到着火点
探究燃烧的条件之一:温度达到着火点
二、填空题
-
11. 用化学用语填空:(1)、3个氮原子;(2)、硝酸铵;(3)、请标出氯酸钾中氯元素的化合价;12. 根据下图回答问题。
 (1)、钙原子的相对原子质量是;(2)、图中 D的符号是;(3)、图中属于同种元素的粒子是(填字母);(4)、图中A和C两种元素形成化合物的化学式为。13. 结合微观示意图回答下列问题。(“●”和“○”分别表示两种不同元素的原子)
(1)、钙原子的相对原子质量是;(2)、图中 D的符号是;(3)、图中属于同种元素的粒子是(填字母);(4)、图中A和C两种元素形成化合物的化学式为。13. 结合微观示意图回答下列问题。(“●”和“○”分别表示两种不同元素的原子) (1)、参加化学反应的各物质的微观粒子个数比
(1)、参加化学反应的各物质的微观粒子个数比 :
:  :
:  =; (2)、该反应的基本反应类型是;(3)、化学反应前后不变的粒子是。14. 如图是电解水的实验装置图。
=; (2)、该反应的基本反应类型是;(3)、化学反应前后不变的粒子是。14. 如图是电解水的实验装置图。 (1)、气体a为;(2)、该实验可分析出水是由组成的(3)、根据精确的实验测定,每个水分子是由构成的。
(1)、气体a为;(2)、该实验可分析出水是由组成的(3)、根据精确的实验测定,每个水分子是由构成的。三、简答题
-
15. 木炭与氧化铜反应的化学反应方程式如下:2CuO+C 2Cu+CO2↑(1)、该反应中,具有还原性的物质是;(2)、实验过程中,观察固体发生的现象是;(3)、该实验如何检验有二氧化碳生成。16. 根据如图实验回答问题:
 (1)、石蕊小花放入集气瓶后观察到的现象是;(2)、该实验发生反应的化学方程式为:。17. 用有关化学知识回答下列事实。(1)、炒菜的油锅不慎着火,可用锅盖盖灭,灭火的原理是;(2)、金刚石与石墨物理性质有很大差异的原因是;(3)、稀有气体化学性质稳定的原因是。
(1)、石蕊小花放入集气瓶后观察到的现象是;(2)、该实验发生反应的化学方程式为:。17. 用有关化学知识回答下列事实。(1)、炒菜的油锅不慎着火,可用锅盖盖灭,灭火的原理是;(2)、金刚石与石墨物理性质有很大差异的原因是;(3)、稀有气体化学性质稳定的原因是。四、实验题
-
18. 实验室使用下列装置制取氧气
 (1)、如果使用高锰酸钾制取氧气,还必需使用的用品是;(2)、加热固体,没有气泡产生的原因是;(3)、以上使用的仪器重新组装,还能进行用过氧化氢溶液和二氧化锰制取氧气的实验, 这些仪器中,一定不需要使用的仪器是;(4)、实验室用过氧化氢溶液制取氧气的化学反应方程式为:;
(1)、如果使用高锰酸钾制取氧气,还必需使用的用品是;(2)、加热固体,没有气泡产生的原因是;(3)、以上使用的仪器重新组装,还能进行用过氧化氢溶液和二氧化锰制取氧气的实验, 这些仪器中,一定不需要使用的仪器是;(4)、实验室用过氧化氢溶液制取氧气的化学反应方程式为:;五、科学探究题
-
19. 比较镁、铝、锌、铁、铜、银、金的金属活动性。(1)、金属与氧气的反应:镁、铝在常温下就能与氧气反应,铁、铜在常温下几乎不与氧气反应,但在高温时能与氧气反应,金即使在高温时也不与氧气反应。
①镁、铝、铁、铜、金五种金属中最不活泼的金属是;
②铝具有很好的抗腐蚀性能,原因是;
(2)、金属与盐酸的反应: 把镁、铝、锌、铁、铜、银分别放入稀盐酸中,铜和银不能发生反应,其它几种金属都能产生大量气泡,反应后产生浅绿色溶液的化学反应方程式为:。(3)、金属活动性顺序:①设计实验比较铜、银、金的活动性: 最简单的实验操作,可以把两根不同的金属丝,同时放入一种金属化合物的溶液中,观察是否反应,即可比较出这三种金属的活动性铜>银>金。 这种金属化合物的溶液是:;
②进行实验比较镁、铝、锌、铁的活动性:
实验操作
现象
实验一
将镁条插入硫酸锌溶液
镁条表面有固体析出
实验二
将铝丝插入硫酸锌溶液
铝丝表面有固体析出
实验三
将铁丝插入硫酸锌溶液
无明显现象
为了能够完成比较这四种金属活动性的实验,还应进行的一个实验操作是:;
③某同学把实验一、二、三中反应结束后的溶液混合在一起装入烧杯中,向混合溶液中 插入一根镁条,充分反应结束后,镁条仍有剩余,过滤后的溶液中一定有水和 。
六、计算题
-