沪教版初中化学九年级下册第6章《溶解现象》单元测试题
试卷更新日期:2019-02-13 类型:单元试卷
一、单选题
-
1. 将2.5g硼酸在20℃时溶于50g水中即达到饱和,则一般把这种物质的溶解性划分为()A、易溶物质 B、可溶物质 C、微溶物质 D、难溶物质2. 硝酸钾、氯化钾的溶解度曲线如图所示。下列说法正确的是( )
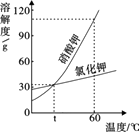 A、硝酸钾的溶解度比氯化钾的溶解度大 B、氯化钾的溶解度随温度升高而减小 C、升温能使硝酸钾的不饱和溶液变成饱和溶液 D、t℃时,两种物质的饱和溶液的质量分数相等3. 如图是A,B,C三种固体物质的溶解度曲线,下列叙述错误的是()
A、硝酸钾的溶解度比氯化钾的溶解度大 B、氯化钾的溶解度随温度升高而减小 C、升温能使硝酸钾的不饱和溶液变成饱和溶液 D、t℃时,两种物质的饱和溶液的质量分数相等3. 如图是A,B,C三种固体物质的溶解度曲线,下列叙述错误的是()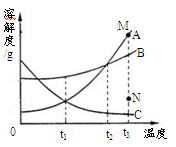 A、t1时,三物质的溶解度B的最大 B、欲使t2时分置于两个容器中的A,B的饱和溶液在升温至t3时仍为饱和溶液,所需加入溶质的质量A大于B C、将t3时C的饱和溶液降温到t1时,溶质的质量分数不变 D、欲使组成在N点的A溶液转变为M点的A溶液,可采取加A的方法4. 甲乙两种固体的溶解度曲线如下图所示。有一个大烧杯中装着含有甲和乙的两种饱和溶液,而且杯中还有少量甲和乙的固体存在。现将温度由80℃降到20℃。下列说法错误的是()
A、t1时,三物质的溶解度B的最大 B、欲使t2时分置于两个容器中的A,B的饱和溶液在升温至t3时仍为饱和溶液,所需加入溶质的质量A大于B C、将t3时C的饱和溶液降温到t1时,溶质的质量分数不变 D、欲使组成在N点的A溶液转变为M点的A溶液,可采取加A的方法4. 甲乙两种固体的溶解度曲线如下图所示。有一个大烧杯中装着含有甲和乙的两种饱和溶液,而且杯中还有少量甲和乙的固体存在。现将温度由80℃降到20℃。下列说法错误的是()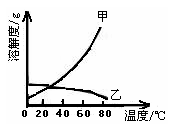 A、杯中固体甲增多、固体乙减少 B、杯中一定有固体甲而不一定有固体乙 C、溶液中溶质甲减少、溶质乙增多 D、甲和乙的两种溶液仍然是饱和溶液5. 下列物质中,属于溶液的是( )
A、杯中固体甲增多、固体乙减少 B、杯中一定有固体甲而不一定有固体乙 C、溶液中溶质甲减少、溶质乙增多 D、甲和乙的两种溶液仍然是饱和溶液5. 下列物质中,属于溶液的是( )
A、蔗糖水 B、牛奶 C、米粥 D、豆浆6. 甲、乙两物质的溶解度曲线如下图所示。下列叙述中正确的是()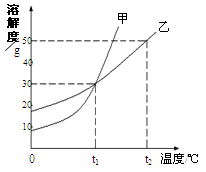 A、t1℃时,甲和乙的溶解度均为30 B、t1℃时,甲和乙的饱和溶液中溶质质量一定相等 C、t2℃时,分别在100g水中各溶解20g甲、乙,降温后,乙溶液的溶质质量分数可能会大于甲溶液的溶质质量分数 D、t2℃时,在100g水中放入60g乙,其溶质的质量分数为37.5%7. 对“16%的硝酸钾溶液”含义的解释错误的是()A、100g水中溶解了16g硝酸钾 B、100g硝酸钾溶液溶解有16g硝酸钾 C、将16g硝酸钾溶解于84g水中所得的溶液 D、将硝酸钾与水按4:21的质量比配成的溶液8. 推理和归纳是化学学习和研究中常用的思维方法,下列推理正确的是()A、离子是带电的原子或原子团,所以带电的粒子一定是离子 B、化合物是由不同元素组成的纯净物,所以由不同元素组成的纯净物一定是化合物 C、氧化物中含有氧元素,所以含有氧元素的化合物一定是氧化物 D、溶液是均一、稳定的,所以均一、稳定的液体一定是溶液9. 某同学在煮鸡蛋汤多加了食盐,汤太“咸”了,要使汤变“淡”,下列措施可行的是()A、将汤倒去一半 B、继续加热 C、向汤里再加鸡蛋 D、向汤里加盐10. t1℃时,将等质量的硝酸钾和氯化钾分别加入到各盛有100g水的两个烧杯中,充分搅拌后现象如图1所示,硝酸钾和氯化钾的溶解度曲线如图2所示。则下列说法正确的是()
A、t1℃时,甲和乙的溶解度均为30 B、t1℃时,甲和乙的饱和溶液中溶质质量一定相等 C、t2℃时,分别在100g水中各溶解20g甲、乙,降温后,乙溶液的溶质质量分数可能会大于甲溶液的溶质质量分数 D、t2℃时,在100g水中放入60g乙,其溶质的质量分数为37.5%7. 对“16%的硝酸钾溶液”含义的解释错误的是()A、100g水中溶解了16g硝酸钾 B、100g硝酸钾溶液溶解有16g硝酸钾 C、将16g硝酸钾溶解于84g水中所得的溶液 D、将硝酸钾与水按4:21的质量比配成的溶液8. 推理和归纳是化学学习和研究中常用的思维方法,下列推理正确的是()A、离子是带电的原子或原子团,所以带电的粒子一定是离子 B、化合物是由不同元素组成的纯净物,所以由不同元素组成的纯净物一定是化合物 C、氧化物中含有氧元素,所以含有氧元素的化合物一定是氧化物 D、溶液是均一、稳定的,所以均一、稳定的液体一定是溶液9. 某同学在煮鸡蛋汤多加了食盐,汤太“咸”了,要使汤变“淡”,下列措施可行的是()A、将汤倒去一半 B、继续加热 C、向汤里再加鸡蛋 D、向汤里加盐10. t1℃时,将等质量的硝酸钾和氯化钾分别加入到各盛有100g水的两个烧杯中,充分搅拌后现象如图1所示,硝酸钾和氯化钾的溶解度曲线如图2所示。则下列说法正确的是()图1
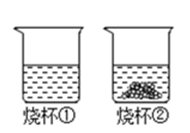
图2
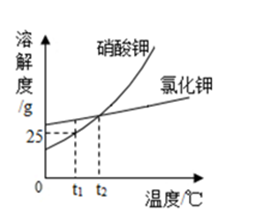 A、烧杯①的溶液一定是不饱和溶液 B、烧杯①的溶液是硝酸钾溶液 C、t1℃时烧杯②的溶液的溶质质量分数为25% D、若烧杯①和烧杯②的溶液都升温到t2℃时,两种溶液的溶质质量分数相等11. 下列四个图象能正确反映实验变化关系的有()
A、烧杯①的溶液一定是不饱和溶液 B、烧杯①的溶液是硝酸钾溶液 C、t1℃时烧杯②的溶液的溶质质量分数为25% D、若烧杯①和烧杯②的溶液都升温到t2℃时,两种溶液的溶质质量分数相等11. 下列四个图象能正确反映实验变化关系的有()
A、常温下,足量的镁、铁分别同时放入少量等质量、等质量分数的稀盐酸中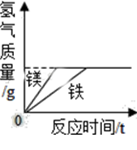 B、敞口放置于空气中的浓硫酸或稀盐酸
B、敞口放置于空气中的浓硫酸或稀盐酸 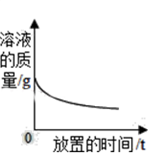 C、加热KNO3、Ca(OH)2的饱和溶液(不考虑溶剂的蒸发)
C、加热KNO3、Ca(OH)2的饱和溶液(不考虑溶剂的蒸发) 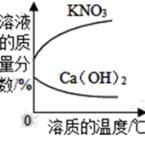 D、少量碳在密闭集气瓶中与氧气完全燃烧
D、少量碳在密闭集气瓶中与氧气完全燃烧  12. 某硫酸溶液中氢离子与水分子个数比为1:5,则该溶液中溶质质量分数略为()A、20% B、35% C、52% D、29%13. 把下列物质混合,能得到溶液的是()A、冰加到水中 B、植物油加到水中 C、碘加入酒精中 D、面粉加到水中14. 下列对应曲线正确的是( )A、 在水中不断加入氯化钠
12. 某硫酸溶液中氢离子与水分子个数比为1:5,则该溶液中溶质质量分数略为()A、20% B、35% C、52% D、29%13. 把下列物质混合,能得到溶液的是()A、冰加到水中 B、植物油加到水中 C、碘加入酒精中 D、面粉加到水中14. 下列对应曲线正确的是( )A、 在水中不断加入氯化钠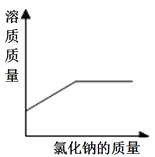 B、某温度下,将饱和的硝酸钾溶液恒温蒸发溶剂
B、某温度下,将饱和的硝酸钾溶液恒温蒸发溶剂 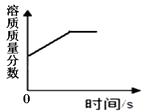 C、加热氯酸钾和二氧化锰
C、加热氯酸钾和二氧化锰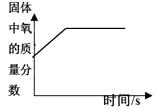 D、等质量、等质量分数的双氧水完全分解
D、等质量、等质量分数的双氧水完全分解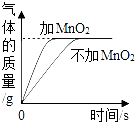 15. 某化学兴趣小组设计四种实验方案来证明炭粉中是否含有氧化铜.其中可行的是:()A、将固体高温加热,看是否有红色固体生成 B、在样品中加稀硫酸,充分反应后,观察是否有固体剩余 C、在样品中加水,是否有蓝色沉淀 D、在样品中加硫酸,充分反应后,溶液是否呈蓝色
15. 某化学兴趣小组设计四种实验方案来证明炭粉中是否含有氧化铜.其中可行的是:()A、将固体高温加热,看是否有红色固体生成 B、在样品中加稀硫酸,充分反应后,观察是否有固体剩余 C、在样品中加水,是否有蓝色沉淀 D、在样品中加硫酸,充分反应后,溶液是否呈蓝色二、填空题
-
16. 水和溶液在生命活动和生产、生活中起着十分重要的作用。
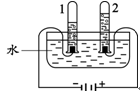 (1)、电解水实验揭示了水的组成。右图实验中得到氢气的试管是(填“1”或“2”);电解水的微观示意图如下,请在方框中补全相应微粒的图示 。
(1)、电解水实验揭示了水的组成。右图实验中得到氢气的试管是(填“1”或“2”);电解水的微观示意图如下,请在方框中补全相应微粒的图示 。 (2)、农业生产常用溶质的质量分数为10%~20%的NaCl溶液来选种。现将600g25%的NaCl溶液稀释为15%的NaCl溶液,需要加水的质量为g。(3)、根据下表回答问题。
(2)、农业生产常用溶质的质量分数为10%~20%的NaCl溶液来选种。现将600g25%的NaCl溶液稀释为15%的NaCl溶液,需要加水的质量为g。(3)、根据下表回答问题。温度/℃
0
20
40
60
80
100
溶解度
/g
NaCl
35.7
36.0
36.6
37.3
38.4
39.8
NH4Cl
29.4
37.2
45.8
55.2
65.6
77.3
①40℃时,向两个分别盛有40gNaCl和NH4Cl的烧杯中,各加入100g的水,充分溶解后,为饱和溶液的是溶液。
②采用一种操作方法,将上述烧杯中的剩余固体全部溶解,变为不饱和溶液。下列说法错误的是(填字母序号)。
A.溶质的质量不变
B.溶液质量一定增大
C.可升高温度或增加溶剂
D.溶液中溶质的质量分数一定减小
17. 我们生活在一个丰富多彩的物质世界中,人类的生产、生活和化学密不可分。(1)、C,H,O是初中化学常见的几种元素,请选用适当的化学符号按要求填空:①酒精溶液中含有的一种有机物是;②相对分子质量最小的氧化物是;
③最清洁的燃料是。④酸的溶液中都含有的一种离子是。
(2)、请用化学知识解释下列问题①喝了汽水后常常会打嗝,原因是升温使气体溶解度。②食物保存在冰箱中不易变质,是因为化学反应速率与有关。③生活中将硬水转化为软水的常用方法是。④食品厂薯条袋内充氮气,是因为氮气。
(3)、小玥一家与朋友们决定使用“共享汽车”出行。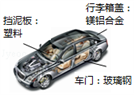
①“共享汽车”中属于金属材料的是(填材料名称,下同), 属于复合材料的是。②将镁铝合金与铝片相互刻画,在铝片表面留下明显划痕,说明镁铝合金的硬度铝的硬度(填“大于”或“小于”)。③使用“共享汽车”出行的好处有(填标号)
a.降低出行成本
b.减少汽车尾气排放
c.节约能源
d.降低交通压力
18. 1mL98%的浓硫酸(密度为1.84g·cm-3)跟5mL水混合,所得稀硫酸溶液溶质的质量分数为 .19. T℃时,氯化钠的溶解度是n克,将m克氯化钠投入到n克水中,充分搅拌,若得到不饱和溶液,则溶液的溶质质量分数为 , 如果m克氯化钠不能完全溶解在n克水中,则溶液的溶质质量分数为 .20. 根据如图所示的溶解度曲线,回答下列问题。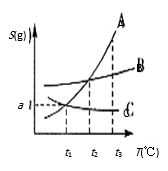 (1)、若A代表的是熟石灰、氯化钠、硝酸钾三种物质中的一种,则A物质是。(2)、在t2℃时,A、B、C三种物质饱和溶液的溶质质量分数由大到小的顺序是。(3)、若保持原溶液溶质质量分数不变,把t3℃时C物质的饱和溶液变成不饱和溶液,应采用的方法。
(1)、若A代表的是熟石灰、氯化钠、硝酸钾三种物质中的一种,则A物质是。(2)、在t2℃时,A、B、C三种物质饱和溶液的溶质质量分数由大到小的顺序是。(3)、若保持原溶液溶质质量分数不变,把t3℃时C物质的饱和溶液变成不饱和溶液,应采用的方法。三、推断题
-
21. 某食盐样品中含有少量泥沙、CaCl2和Na2SO4 , 按图方案提纯得到NaCl晶体。
 (1)、试剂A为。(2)、固体丙的主要成分是。22. 某粗盐样品中含有杂质氯化镁、氯化钙。康康设计了以下提纯方案:
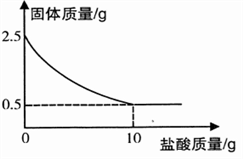
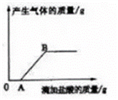
(1)、试剂A为。(2)、固体丙的主要成分是。22. 某粗盐样品中含有杂质氯化镁、氯化钙。康康设计了以下提纯方案: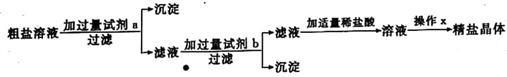 (1)、过滤和操作x中都用到的玻璃仪器是 , 其在操作x中的作用是。(2)、加入试剂b后,必须过滤,否则滴加稀盐酸后沉淀会溶解,沉淀溶解的化学方程式为。(只写1个)。(3)、滴加稀盐酸时产生气体的情况如图所示,OA段发生反应的化学方程式为。
(1)、过滤和操作x中都用到的玻璃仪器是 , 其在操作x中的作用是。(2)、加入试剂b后,必须过滤,否则滴加稀盐酸后沉淀会溶解,沉淀溶解的化学方程式为。(只写1个)。(3)、滴加稀盐酸时产生气体的情况如图所示,OA段发生反应的化学方程式为。
四、实验题
-
23. 下图是康康同学配制一定溶质质量分数的氯化钠溶液的部分操作步骤。
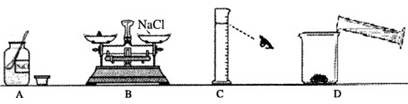 (1)、康康同学的操作中共有(填数字)处错误,请你任选择一处说明其错误的原因。(2)、除了上图所示的仪器外,康康还需要哪些仪器?。(3)、上述不符合题意操作将导致所配制氯化钠溶液的溶质质量分数较理论值(填“偏大”、“不变”、“偏小”或“不能确定”)24. 某同学在实验时发现一瓶装有氢氧化钠溶液的试剂瓶口有白色粉末,他推测该白粉末可能是残留在瓶口的氢氧化钠变质形成的新物质。(1)、为验证自己的推测,他进行了下列实验:取少量白色粉末滴加稀盐酸,有气泡产生。上述实验能否说明氢氧化钠变质了?理由是什么?(2)、为进一步探究该白色粉末中是否含有氢氧化钠,还需做什么实验?请写出简要的实验步骤。
(1)、康康同学的操作中共有(填数字)处错误,请你任选择一处说明其错误的原因。(2)、除了上图所示的仪器外,康康还需要哪些仪器?。(3)、上述不符合题意操作将导致所配制氯化钠溶液的溶质质量分数较理论值(填“偏大”、“不变”、“偏小”或“不能确定”)24. 某同学在实验时发现一瓶装有氢氧化钠溶液的试剂瓶口有白色粉末,他推测该白粉末可能是残留在瓶口的氢氧化钠变质形成的新物质。(1)、为验证自己的推测,他进行了下列实验:取少量白色粉末滴加稀盐酸,有气泡产生。上述实验能否说明氢氧化钠变质了?理由是什么?(2)、为进一步探究该白色粉末中是否含有氢氧化钠,还需做什么实验?请写出简要的实验步骤。五、计算题