鲁教版九年级化学_第九单元_金属_单元检测试卷
试卷更新日期:2019-02-13 类型:单元试卷
一、 选择题
-
1. 利用钨制作灯泡里的灯丝,而不用锡的主要原因是( )A、钨有导电性,而锡没有 B、钨很细,而锡很粗 C、钨熔点高,而锡熔点低 D、钨便宜,而锡很贵2. 下列有关对金属和金属材料的认识错误的是( )A、铜有良好的导电性,常用来制作导线 B、铝表面易形成致密的氧化膜,可阻止铝进一步被所氧化 C、合金的硬度一般小于成分金属的硬度 D、废旧电池的回收,可减少对环境的污染3. 对于一氧化碳还原氧化铁的实验,下列叙述正确的是( )A、 实验开始时先加热,再通一氧化碳气体 B、实验开始时先加热,还是先通一氧化碳气体都可以 C、尾气可以任意排放 D、尾气不可以任意排放,须进行处理4. 在选择铸造硬币的金属材料时,不需要考虑的因素是( )A、 硬度 B、导电性 C、耐腐蚀性 D、与硬币面值相应的价值5. 某化学兴趣小组设计了验证Fe、Cu、Ag的金属活动性顺序的多种方案,每种方案所需的试剂如下:
①Fe、Ag、CuSO4溶液;②Cu、FeCl2溶液、AgNO3溶液;③Fe、Cu、稀盐酸、AgNO3溶液;④Fe、Cu、AgNO3溶液;⑤Cu、Ag、FeSO4溶液,你认为可行的方案是( )
A、①②③④ B、①②③⑤ C、只有①②⑤ D、只有①②③6. 如右图实验,放置 周时间后,装置中能出现的现象是( ) A、 铁丝不变化 B、试管中的液面不变化 C、铁丝逐渐消失 D、试管中的液面上升7. “垃圾是放错了位置的资源”,应该分类回收.生活中废弃的铁锅、铝制易拉罐、铜导线,可归为同一类回收,下列说法错误的是( )A、 铁锅、铝制易拉罐、铜导线放在一筐里称为铁、铝、铜合金 B、废品回收节约了资源,保护了环境 C、回收废品人人有责,人人有利 D、有毒垃圾要进行特殊处理8. 下表中列出几种物质的熔点(在 , 下),判断以下说法中正确的是( )
A、 铁丝不变化 B、试管中的液面不变化 C、铁丝逐渐消失 D、试管中的液面上升7. “垃圾是放错了位置的资源”,应该分类回收.生活中废弃的铁锅、铝制易拉罐、铜导线,可归为同一类回收,下列说法错误的是( )A、 铁锅、铝制易拉罐、铜导线放在一筐里称为铁、铝、铜合金 B、废品回收节约了资源,保护了环境 C、回收废品人人有责,人人有利 D、有毒垃圾要进行特殊处理8. 下表中列出几种物质的熔点(在 , 下),判断以下说法中正确的是( )物质名称
固态水银
金
铜
铁
钨
固态氢
熔点
A、 铜球掉入铁水中不会熔化 B、在零下 时,氢是固体
C、水银温度计可测零下
时,氢是固体
C、水银温度计可测零下  的温度
D、用钨制成的灯丝不易熔化
9. 铁在下列哪种情况下最容易生锈( )A、 在干燥的空气中 B、部分浸入食盐水中 C、在潮湿的空气中 D、浸没在植物油中10. 在下列叙述的短线上,只能填“或”,不能填“和”的是( )A、 在化学反应前后催化剂的质量 化学性质都保持不变 B、要使可燃物燃烧,必须使可燃物跟氧气接触 使可燃物的温度达到着火点 C、复分解反应发生的条件:生成物中要有沉淀生成、有气体放出有水生成 D、工业炼铁用一氧化碳铁矿石在高温下反应生成铁11. 下列关于金属材料的说法错误的是( )A、常温下,铝能与空气中的氧气反应,在其表面生成致密的氧化铝薄膜 B、铁在干燥的空气中容易生锈 C、硬铝(铝合金)的硬度大于纯铝 D、金属资源的回收利用既保护了环境,又节约了金属资源12. 小明同学对所学部分化学知识归纳如下,其中完全正确的一组是( )
的温度
D、用钨制成的灯丝不易熔化
9. 铁在下列哪种情况下最容易生锈( )A、 在干燥的空气中 B、部分浸入食盐水中 C、在潮湿的空气中 D、浸没在植物油中10. 在下列叙述的短线上,只能填“或”,不能填“和”的是( )A、 在化学反应前后催化剂的质量 化学性质都保持不变 B、要使可燃物燃烧,必须使可燃物跟氧气接触 使可燃物的温度达到着火点 C、复分解反应发生的条件:生成物中要有沉淀生成、有气体放出有水生成 D、工业炼铁用一氧化碳铁矿石在高温下反应生成铁11. 下列关于金属材料的说法错误的是( )A、常温下,铝能与空气中的氧气反应,在其表面生成致密的氧化铝薄膜 B、铁在干燥的空气中容易生锈 C、硬铝(铝合金)的硬度大于纯铝 D、金属资源的回收利用既保护了环境,又节约了金属资源12. 小明同学对所学部分化学知识归纳如下,其中完全正确的一组是( )A.物质的分类
B.资源的利用和保护
①合成橡胶、合金都属于合成材料
②氧化物中含有氧元素
③混合物中一定含有多种元素
①保护空气要减少有害气体和烟尘的排放
②爱护水资源要节约用水和防止水体污染
③保护金属资源只能通过防止金属腐蚀实现
C.“低碳经济”的措施
D.用“化学”眼光分析
①改造或淘汰高能耗、高污染产业
②研制和开发新能源替代传统能源
③减少使用一次性塑料方便袋
①洗涤剂去油污是因为起乳化作用
②湿衣服晾干是因为分子之间有间隔
③明矾净水是因为明矾溶于水生成胶状物
A、 A B、B C、C D、D13. 将一定量的锌粉加入 和 的混合溶液中,充分反应后过滤,得到滤渣和滤液。下列关于滤渣和滤液的分析错误的是( )A、 向滤渣中滴加稀盐酸,若无明显现象,则滤液中一定含有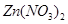 和
和 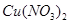 B、向滤渣中滴加稀盐酸,若产生气泡,则滤液中一定没有
B、向滤渣中滴加稀盐酸,若产生气泡,则滤液中一定没有 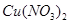 C、向滤液中滴加稀盐酸,若产生白色沉淀,则滤渣中一定没有
C、向滤液中滴加稀盐酸,若产生白色沉淀,则滤渣中一定没有 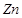 和
和  D、若滤液呈蓝色,则滤渣中一定含有
D、若滤液呈蓝色,则滤渣中一定含有 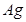 ,可能含有
,可能含有  14. 下列所涉及到的物质中不属于合金的是( )A、 青铜 B、不锈钢 C、氧化铁 D、生铁15. 年我国纪念“世界水日”和开展“中国水周”活动的宣传主题为“水利发展与和谐社会”.下列有关水的知识中,错误的是( )A、 水中
14. 下列所涉及到的物质中不属于合金的是( )A、 青铜 B、不锈钢 C、氧化铁 D、生铁15. 年我国纪念“世界水日”和开展“中国水周”活动的宣传主题为“水利发展与和谐社会”.下列有关水的知识中,错误的是( )A、 水中 、
、  的增多会引起水体的富营养化
B、水是一种最常见的溶剂,自然界中的水都含有杂质
C、工业污水集中处理后排放能大大减少水的污染
D、含汞、镉、铅的电池会造成水体和土壤的污染
的增多会引起水体的富营养化
B、水是一种最常见的溶剂,自然界中的水都含有杂质
C、工业污水集中处理后排放能大大减少水的污染
D、含汞、镉、铅的电池会造成水体和土壤的污染
二、 多选题
-
16. 下列关于金属铝的叙述中,说法错误的是( )A、
 是地壳中含量最多的元素
B、
是地壳中含量最多的元素
B、 是比较活泼的金属,在化学反应中容易失去电子,表现还原性
C、
是比较活泼的金属,在化学反应中容易失去电子,表现还原性
C、 箔在空气中受热可以熔化,且发生剧烈燃烧
D、
箔在空气中受热可以熔化,且发生剧烈燃烧
D、 箔在空气中受热可以熔化,由于氧化膜的存在,熔化的
箔在空气中受热可以熔化,由于氧化膜的存在,熔化的  并不滴落
17. 下列物质属于金属材料的是( )A、 青铜 B、铁矿石 C、焦炭 D、黄金18. 实验室里,用如图所示装置还原氧化铁的过程中,可能生成四氧化三铁、氧化亚铁或铁等固体物质.关于该实验,下列说法错误的是( )
并不滴落
17. 下列物质属于金属材料的是( )A、 青铜 B、铁矿石 C、焦炭 D、黄金18. 实验室里,用如图所示装置还原氧化铁的过程中,可能生成四氧化三铁、氧化亚铁或铁等固体物质.关于该实验,下列说法错误的是( ) A、 实验开始时,应该先点燃酒精灯,一段时间后再通入一氧化碳 B、实验过程中,试管中澄清的石灰水变浑浊,证明该反应有二氧化碳生成 C、实验结束后,玻璃管中红色的氧化铁粉末变成黑色,该产物不一定是铁 D、该反应中,一氧化碳转化为无毒无害的二氧化碳,故不需要尾气处理装置19. 关于一氧化碳还原氧化铜的实验,下列叙述正确的是( )A、 先通入一氧化碳再加热氧化铜 B、先加热氧化铜再通入一氧化碳 C、反应结束,先停止通入CO,再熄灭酒精灯 D、反应尾气要处理20. 同一个化学反应中,在水溶液里能同时生成的是( )A、
A、 实验开始时,应该先点燃酒精灯,一段时间后再通入一氧化碳 B、实验过程中,试管中澄清的石灰水变浑浊,证明该反应有二氧化碳生成 C、实验结束后,玻璃管中红色的氧化铁粉末变成黑色,该产物不一定是铁 D、该反应中,一氧化碳转化为无毒无害的二氧化碳,故不需要尾气处理装置19. 关于一氧化碳还原氧化铜的实验,下列叙述正确的是( )A、 先通入一氧化碳再加热氧化铜 B、先加热氧化铜再通入一氧化碳 C、反应结束,先停止通入CO,再熄灭酒精灯 D、反应尾气要处理20. 同一个化学反应中,在水溶液里能同时生成的是( )A、 、
、  B、
B、 、
、  C、
C、 、
、  D、
D、 、
、 
三、 填空题
-
21. 请回答下列与金属有关的问题.(1)、铜片与黄铜片相互刻画,在片表面会留下划痕;(2)、在Cu、Al、Au三种金属中,常温下因表面形成氧化膜而耐腐蚀的是;(3)、向AgNO3和Cu(NO3)2的混合溶液中加入一定量的Zn粉,充分反应后过滤,得到无色滤液,则滤渣中一定含有的金属是 .22. 将铁粉加入到一定量的硝酸银、硝酸铜及硝酸锌的混合溶液中.待充分反应后过滤,再在滤渣中加入稀盐酸,没有气体产生,则在滤液中
A.只有硝酸锌和水 B.一定有硝酸锌和硝酸亚铁
C.一定没有硝酸银 D.如果没有硝酸铜,则一定没有 .
23. 同学们已经学习了一些金属的有关知识,对金属的活动性顺序也有了一定的认识.请运用所学知识参与以下探究并回答相关问题:(1)、将 枚洁净无锈的铁钉分别放入下面 、 、 、 支试管中.再分别在 中加入少量的蒸馏水, 中加入少量的氯化钠溶液, 中注满迅速冷却的沸水,塞紧橡皮塞, 中加入少量干燥剂,再放入一团棉花球,把铁钉放在干棉花球上,塞紧橡皮塞(如图所示).
上述实验中,试管中的铁钉最易生锈.设计如题图 实验的目的是 .
(2)、某兴趣小组利用仅提供的铁、铜、硝酸银溶液三种药品探究铁、铜、银的金属活动性顺序.甲同学设计了如图 、 所示的两个实验:

通过 实验得出的结论是 , 实验中观察到溶液的颜色由无色变为色.乙同学认为甲同学设计的实验并不能达到实验目的,经过思考,他仍用这三种药品设计实验,并得出符合题意的结论.请你帮他完成实验报告:
操作
现象
结论
将铁片和铜片同时插入同一份硝酸银溶液中.然后将有明显现象的金属取出,继续观察另一金属片对应现象
一会,铁片表面明显变白,而铜片表面无明显现象.当铁片取出后,铜表面也慢慢变白.
三种金属的活动性有强到弱的顺序:铁铜银
列举上述探究结果在生产生活中的一条具体应用 .
四、 解答题
-
24. 钢铁的生产与使用是人类文明和社会进步的一个重要标志.我们每年向自然界索取大量的金属矿物资源.随着金属材料使用量的增大和矿物资源的紧缺,人们对资源保护的意识日趋增强.请你谈谈保护金属资源的四个有效途径.25. 铁是一种化学性质比较活泼的金属,在一定条件下能跟多种物质发生化学反应.回答下列问题:(1)、以铁为研究对象,仿照图中实例在框图处填写物质的化学式(所填写的反应物不属同一类别的物质,生成物必须填写铁的化合物).
 (2)、实验室中要除去细碎铜屑中的少量铁屑,请用物理方法和化学方法除杂.(只用简单的原理描述即可):
(2)、实验室中要除去细碎铜屑中的少量铁屑,请用物理方法和化学方法除杂.(只用简单的原理描述即可):物理方法:;
化学方法: .
五、 实验探究题
-
26. 国务院发布了《关于钢铁行业化解过剩产能,实现脱困发展的意见》,推动钢铁行业升级.钢铁是一种重要的金属材料.
 (1)、我们在日常生活中使用的铁锅,体现的一种主要性质是________.A、延展性 B、导热性 C、抗腐蚀性 D、熔点高(2)、使用铁锅炒菜可补充人体必须的微量元素铁,缺铁元素易患的疾病是 .(3)、据报道,全世界每年被腐蚀损耗的钢铁材料约全年钢铁产量的五分之一,铁生锈是铁与空气中的等发生化学反应;生产生活中常用防止铁制品生锈的方法有什么(两个即可)?(4)、某化学小组利用如图装置(部分装置已略去)进行了将铁锈还原的实验探究:
(1)、我们在日常生活中使用的铁锅,体现的一种主要性质是________.A、延展性 B、导热性 C、抗腐蚀性 D、熔点高(2)、使用铁锅炒菜可补充人体必须的微量元素铁,缺铁元素易患的疾病是 .(3)、据报道,全世界每年被腐蚀损耗的钢铁材料约全年钢铁产量的五分之一,铁生锈是铁与空气中的等发生化学反应;生产生活中常用防止铁制品生锈的方法有什么(两个即可)?(4)、某化学小组利用如图装置(部分装置已略去)进行了将铁锈还原的实验探究:甲中 为铁锈粉末,实验开始时先缓缓通入 ,一段时间后高温加热硬质玻璃管甲,乙中的澄淸石灰水出现了白色浑浊,待反应完全后停止加热,仍继续通入 直到甲冷却.
①甲中发生反应的化学方程式为 .
②实验存在缺陷,请提出改进措施.
③为什么实验开始时先通 ,再进行加热?
(5)、铁锈结构疏松,若不及时除去铁锈会加剧锈蚀,现用盐酸快速除铁锈,但过量的盐酸会腐蚀金属,如果用 的盐酸去除铁锈中 氧化铁,请计算消耗盐酸的质量是多少?27. 为了验证 、 、 的金属活动性顺序,甲、乙、丙三位同学进行下列探究,请你一起参与他们的活动:(1)、提出假设:对于如何选择化学试剂问题,他们各抒己见.①甲同学认为,应选的试剂是: 、 、 ;
②乙同学认为,应选的试剂是: 、 、 ;
③丙同学认为,只要分别将 、 、 投入稀盐酸中,根据它们产生的不同现象,同样也可以验证它们的金属活动性顺序.
你认为,他们选择试剂的方案中,可行的有 . (填以下序号)
.甲同学 .乙同学 .丙同学
(2)、查阅资料:①不同的金属,活动性是不同的;有的金属能与酸起置换反应,有的则不能.②在相同条件下,金属活动性越强,与酸反应的速度越快.
实验探究:他们各自按自己选择的试剂进行探究.
甲同学发现,把 、 分别投入 溶液中,只有的表面才有黑色固体析出.
(3)、乙同学发现,把 分别投入 和 溶液中,只有在溶液中 的表面才有固体析出.(4)、丙同学将 、 、 分别投入稀盐酸中,也得出同样的结论.你认为丙观察到的现象是: 的表面(有、没有)气泡产生;丙同学所说的不同现象是指 .实验结论:他们充分交流后,发现得出的结论相同,即 、 、 的金属活动性由强到弱的顺序是 .
28. 小明对铁的锈蚀进行如下探究.室温时,将包有样品的滤纸包用大头针固定在橡胶塞上,迅速塞紧,装置如图.观察到量筒内水沿导管慢慢进入广口瓶(净容积为146mL).当温度恢复至室温,且量筒内水面高度不变时读数(此时瓶内氧气含量近似为零).记录起始和最终量筒的读数以及所需时间如下表.
序号
样品
量筒起始
读数
量筒最终
读数
所需时间
铁粉、 碳和 滴水
约
铁粉、 碳、 滴水和少量
约
铁粉、 滴水
________
________
________
(1)、实验①和②说明 可以(填“加快”或“减慢”)铁锈蚀的速率.(2)、实验开始后,广口瓶内温度有所上升,说明铁的锈蚀过程是(填“放热”或“吸热”)过程.(3)、实验结束后取出滤纸包,观察到有红棕色物质生成,该物质的化学式是: .(4)、实验①和③是探究碳对铁锈蚀速率的影响,请在表格空白处填写实验③的样品组成.(5)、该装置还可用于测量空气中氧气的含量,根据上述数据计算氧气的体积含量是(6)、现仅提供:量筒、大烧杯、玻璃棒、水、滤纸包(内含 铁粉、 碳、 滴水和少量 ),请你帮助小明再设计一个测量空气中氧气体积含量的实验方案,画出实验装置示意图即可(注明滤纸包的位置).29. 钛 具有硬度大、密度小、熔点高、抗腐蚀性远优于不锈钢等优良性能,被誉为“未来金属”.某化学兴趣小组欲探究 、 、 的金属活动性顺序,进行如下实验:、先用砂纸将金属表面擦光亮.
、将大小厚薄相同的三种金属片分别放入等质量、等溶质质量分数的稀硫酸中,观察到得现象如下:
金属
钛
镁
铜
与稀硫酸反应
缓慢放出气泡
迅速放出气泡
无明显现象
(1)、根据以上现象,将钛、镁、铜的元素符号填入下表的相应位置. (2)、根据金属与盐溶液的反应情况也能判断出金属活动性顺序,小李认为:用钛分别与两种盐溶液反应也可得出以上的金属活动性顺序,请你完成下面实验报告:
(2)、根据金属与盐溶液的反应情况也能判断出金属活动性顺序,小李认为:用钛分别与两种盐溶液反应也可得出以上的金属活动性顺序,请你完成下面实验报告:实验操作
预期实验现象
结论
①把一钛片放入装有溶液的试管中
无明显现象
金属活动性:
②把一钛片放入装有溶液的试管中
金属活动性: