贵州黔南2018-2019学年九年级上学期理综-化学期末考试试卷
试卷更新日期:2019-02-13 类型:期末考试
一、选择题
-
1. 下列变化中, 属于物理变化的是( )A、菜刀生锈 B、酒精燃烧 C、花生榨油 D、粮食酿酒2. 下列物质中,含有氧分子的是( )A、H2O B、O2 C、CO2 D、H2O23. 下列属千纯净物的是( )A、空气 B、自来水 C、酱油 D、干冰4. 在元素周期表中,镁元素的信息如图所示,对图中信息解释不正确的是( )
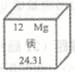 A、原子序数为12 B、核外电子数为24 C、元素符号为Mg D、相对原子质量为24.315. 下列实验操作错误的是( )A、检查气密性
A、原子序数为12 B、核外电子数为24 C、元素符号为Mg D、相对原子质量为24.315. 下列实验操作错误的是( )A、检查气密性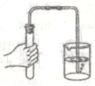 B、取用固体
B、取用固体  C、碗倒液体
C、碗倒液体 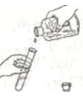 D、加热液体
D、加热液体 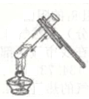 6. 食醋是厨房中常用的调味品,它的主要成分是乙酸,乙酸分子的模型如右图所示.其中
6. 食醋是厨房中常用的调味品,它的主要成分是乙酸,乙酸分子的模型如右图所示.其中 代表一个碳原子,
代表一个碳原子,  代表一个氢原子,
代表一个氢原子,  代表一个氧原子。下列说法不正确的是( )
代表一个氧原子。下列说法不正确的是( )  A、乙酸是一种化合物 B、乙酸的相对分子质量为60 C、乙酸中碳元素的质量分数为60% D、乙酸分子中的碳原子、氢原子、氧原子的个数比为1:2:1
A、乙酸是一种化合物 B、乙酸的相对分子质量为60 C、乙酸中碳元素的质量分数为60% D、乙酸分子中的碳原子、氢原子、氧原子的个数比为1:2:1二、解答题
-
7. 用化学符号表示:
①钾元素:; ②2个氮原子:: ⑨2个氢气分子:;④铵根离子: ⑤标出“Mg0”中镁元素的化合价。
8. 水是生命之源,它与我们的生活密切相关。(1)、净水器常用活性炭,主要是利用活性炭的性。生活中,既能降低水的硬度,又能杀菌消毒的方法是。(2)、电解水的装置如在图所示,试管A中的气体是 , 通过此实验证明水是由组成的.该反应的化学方程式是。实验室除了用电解水制取氧气外-还能用加热氯酸钾和二氧化锰的混合物来制取,反应的化学方程式为 , 在该反应中.二氧化锰的作用是。 9. 目前人们使用的燃料大多来自化石燃料,如 、石油、天然气等。天然
9. 目前人们使用的燃料大多来自化石燃料,如 、石油、天然气等。天然气的主要成分是甲烷(CH4),甲烷完全燃烧的化学方程式是 。氢能是理想的清洁能源。以太阳能为热源,经由铁氧化合物循环分解水的过程如右图所示:
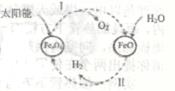 (1)、反应l的基本反应类型为。(2)、写出在一定条件下发生的反应ll的化学方程式。(3)、在上述循环过程中,最终得到的产品是和。10. 下图中表示中学几种常见的物质在一定条件下可以转化,A是石灰石的主要成分,E、G为黑色的粉末,c为无色液体.H为紫红色剧体。(部分条件省略)
(1)、反应l的基本反应类型为。(2)、写出在一定条件下发生的反应ll的化学方程式。(3)、在上述循环过程中,最终得到的产品是和。10. 下图中表示中学几种常见的物质在一定条件下可以转化,A是石灰石的主要成分,E、G为黑色的粉末,c为无色液体.H为紫红色剧体。(部分条件省略)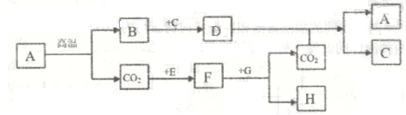 (1)、写出下列物质的化学式:A. . C. , D: , F:。(2)、CO2与E反应的化学反应方程式是: . F与G反应的化学反应方程式
(1)、写出下列物质的化学式:A. . C. , D: , F:。(2)、CO2与E反应的化学反应方程式是: . F与G反应的化学反应方程式为:。
三、实验与探究
-
11. 根据下图回答问题。
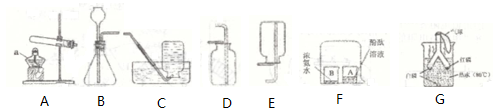 (1)、仪器a的名称是。(2)、用高锰酸钾制取氧气的化学方程式为 , 用c装置收集的气体应具有的性质
(1)、仪器a的名称是。(2)、用高锰酸钾制取氧气的化学方程式为 , 用c装置收集的气体应具有的性质是。
(3)、用大理石和稀盐酸制取二氧化碳时,所选用的发生装置是 , 用D装置收集二氧化碳的验满方法是。(4)、实验F中观察到的实验现象是 , 实验结论是。(5)、实验G中观察到的实验现象是 , 化学方程式为。12. 过氧化氢在生产生活中有广泛应用。实验小组对过氧化氢的某些性质进行研究。(1)、Ⅰ.不稳定性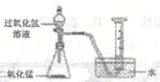
如上图所示进行实验,过氧化氢分解的化学方程式为 , 产生3.2g02时分解的过氧化氢的质量为g。
(2)、能用排水法收集02的原因是。(3)、探究温度对过氧化氢分解速率的影响同学们进行了如下的实验,实验数据如下表:
实验序号
①
②
③
H2O2溶液的浓度%
30
30
30
H2O2溶液的体积/mL
6
6
6
温度/℃
20
35
55
MnO2的用量/g
0
0
0
收集O2的体积/mL
0
1.9
7.8
反应时间
40min
40min
40min
由此得出的结论是。
(4)、Ⅱ.腐蚀性【查阅资料】H2O2溶液有腐蚀性。
【进行实验】
将铜片分别浸泡在3种溶液中进行实验,如下表。
编号
②
②
③
实验
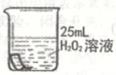

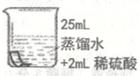
一段时间后的现象
无明显变化
溶液变蓝,缓慢产生细小气泡
无明显变化
【解释与结论】
实验①的作用是。
(5)、铜片被腐蚀的反应如下,补全该反应的化学方程式。Cu+H2O2+H2SO4=CuSO4+2。
(6)、【反思交流】某同学提出,实验②中,除发生(5)的反应外,还发生了一个反应导致有细小气泡产生,该反应的反应物为。
四、计算题
-
13. 把4g硫粉放在给定质量的氧气中燃烧,有关实验数据如下表所示。请回答下列问题:
实验编号
①
②
③
O2的质量(g)
3
4
6
SO2的质量(g)
6
(1)、第一次实验中,参加反应的S的质量为g。(2)、第二次实验中,参加反应的S的质量、O2的质量与生成的SO2的质量比是:。(3)、计算第三次试验中生成SO2的质量。