2018-2019学年粤教版化学九年级下册第七单元测试卷
试卷更新日期:2019-01-15 类型:单元试卷
一、单选题
-
1. 从200mL20%的氢氧化钠溶液中取出10mL,取出溶液的质量分数( )
A、20% B、10% C、2% D、0.2%2. 我们熟悉的物质中,属于溶液的是( )A、牛奶 B、豆浆 C、冰水 D、糖水3. 向两烧杯水中分别加入甲、乙两种物质形成溶液,经测定,甲能使溶液温度升高,而加入乙的溶液温度不发生改变,那么甲、乙分别可能是下列哪种物质( )
A、氢氧化钠;硝酸铵 B、硝酸铵;氯化钠 C、氢氧化钠;浓硫酸 D、生石灰;氯化钠4. 下列物质中属于乳浊液的是( )A、牛奶 B、食盐水 C、碘酒 D、蔗糖5. 20℃时,100g水中不断加入NaCl固体,充分搅拌后过滤,称量所得溶液的质量如表所示,其中属于饱和溶液的是( )选项
①
③
④
加入NaCl质量(g)
5
15
36
40
所得溶液质量(g)
105
115
136
136
A、①② B、②⑨ C、③④ D、都是6. 室温时,有两瓶硝酸钾溶液,一瓶为饱和溶液(溶质的质量分数为40%),另一瓶为10%的溶液。下列实验操作中,无法区分这两种溶液的是 ( )A、加一定量的水 B、加入少量硝酸钾晶体 C、略降低温度 D、室温时,蒸发少量水7. 保持其他条件不变,欲使接近饱和的KNO3溶液变为饱和溶液,下列方法中不可行的是( )A、蒸发溶剂 B、升高温度 C、降低温度 D、加入KNO3固体8. 下列关于溶液的叙述中,错误的是( )A、饱和溶液不一定是浓溶液 B、氢氧化钠固体溶于水时,液体温度升高 C、将室温下接近饱和的硝酸钾溶液变成饱和溶液,可采用加水的方法 D、从100g质量分数 20%的食盐水中倒出10g,剩余溶液的溶质质量分数仍为20%9. 下列说法中正确的是( )A、金属能导电,则能导电的物质都是金属 B、碳单质具有可燃性,则含碳元素的物质都有可燃性 C、点燃氢气前要验纯,则可燃性气体点燃前都需要验纯 D、气体的溶解度随温度的升高而减小,则溶解度随温度的升高而减小的物质一定是气体10. 下图是A、B、C三种固体(均不含结晶水)的溶解性曲线,下列说法错误的是( ) A、t1℃时,A,B,C三种物质的饱和溶液的溶质质量分数B>A=C B、将t2℃时A,B的饱和溶液降温到t1℃,析出晶体的质量一定是A>B C、若B中混有少量A,可用蒸发结晶的方法提纯B D、将t1℃等质量的A,B的饱和溶液升温t2℃时,所得A,B溶液的质量一定相等11. a、b、c三种固体物质的溶解度曲线如图所示,下列有关叙述正确的是( )
A、t1℃时,A,B,C三种物质的饱和溶液的溶质质量分数B>A=C B、将t2℃时A,B的饱和溶液降温到t1℃,析出晶体的质量一定是A>B C、若B中混有少量A,可用蒸发结晶的方法提纯B D、将t1℃等质量的A,B的饱和溶液升温t2℃时,所得A,B溶液的质量一定相等11. a、b、c三种固体物质的溶解度曲线如图所示,下列有关叙述正确的是( ) A、a物质的溶解度大于b物质的溶解度 B、t2℃时,c溶液溶质质量分数最小 C、将t1℃时a的饱和溶液升高温度后,溶质质量分数变大 D、大量b中混入少量a,一般用蒸发溶剂的方法获得较纯净的b12. 把 80℃的饱和硝酸钾溶液降温到 30℃,下列叙述正确的是( )
A、a物质的溶解度大于b物质的溶解度 B、t2℃时,c溶液溶质质量分数最小 C、将t1℃时a的饱和溶液升高温度后,溶质质量分数变大 D、大量b中混入少量a,一般用蒸发溶剂的方法获得较纯净的b12. 把 80℃的饱和硝酸钾溶液降温到 30℃,下列叙述正确的是( )①溶质的质量不变 ②溶液的质量不变 ③溶剂的质量不变 ④仍然是饱和溶液 ⑤溶质的 质量分数减小
A、①②③ B、②③④ C、①④⑤ D、③④⑤13. 将200g溶质质量分数为10%的蔗糖溶液稀释到5%,需加水的质量为( )
A、20g B、100g C、180g D、200g14. 现有100克溶质质量分数为10%的食盐溶液,若使溶液的溶质质量分数增加一倍,下列操作中正确的是 ( )
A、加入食盐10克 B、加入水50克 C、蒸发掉溶剂的一半 D、加入100克溶质质量分数为30%的食盐溶液二、填空题
-
15. 如图1是A、B、C三种物质的溶解度曲线图.请回答:
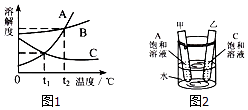
①t1℃时,溶解度相等的两种物质是 .
②B的饱和溶液中混有少量的物质A,要除去A得到较纯的B物质,可采用的结晶方法是 .
③如图2所示,在大烧杯中加入一定量的硝酸铵固体后,甲试管内出现的现象是 , 乙试管内的溶液为溶液(填“饱和”或“不饱和”).
16. 试根据图中信息回答下列问题:⑴

用来铸造硬币的合金需要具有的性质是(答两点)
;
⑵

把水喷向空中的目的是
;
⑶

铁锈主要成分的化学式是;
⑷

厨房洗涤剂除油污的原理是;
17. 某小组同学利用如图2溶解度曲线和图1进行实验,并完成下列问题
①20℃时,氯化钠的溶解度为。
②40℃时,硝酸钾的溶解度氯化钠的溶解度(用“>”“<”“=”填空)
③A中溶液为60℃硝酸钾的溶液(填“饱和”或“不饱和”)
④B中溶液的质量为克
⑤将D过滤,下列有关所得晶体和溶液说法正确的是(填字母)。
Ⅰ.析出的晶体中可能含有氯化钠
Ⅱ.所得溶液中一定含有硝酸钾和氯化钠
Ⅲ.C→D过程可以完全分离硝酸钾和氯化钠
Ⅳ.所得溶液一定是硝酸钾的饱和溶液
18. 如图是甲、乙、丙三种固体物质的溶解度曲线。 (1)、P点的含义。(2)、要使接近饱和的甲溶液变成饱和溶液,可采用的方法有(写出一种)。当甲溶液中含有少量乙时,可采用的方法提纯甲。(3)、t2℃时,将30g甲物质放入50g水的烧杯中,所得溶液溶质的质量分数为(精确到0.1%)。若烧杯内物质升温到t3℃(不考虑水蒸发),溶液中变化的是。
(1)、P点的含义。(2)、要使接近饱和的甲溶液变成饱和溶液,可采用的方法有(写出一种)。当甲溶液中含有少量乙时,可采用的方法提纯甲。(3)、t2℃时,将30g甲物质放入50g水的烧杯中,所得溶液溶质的质量分数为(精确到0.1%)。若烧杯内物质升温到t3℃(不考虑水蒸发),溶液中变化的是。Ⅰ.溶质的质量 Ⅱ.溶剂的质量 Ⅲ.溶质的质量分数
(4)、t3℃时甲、乙、丙三种物质的溶解度按由小到大的顺序是。(5)、将t1℃时甲、乙、丙三种物质饱和溶液的温度升高到t3℃时,三种溶液的溶质质量分数大小关系是______(填写选项序号)。A、丙>甲=乙 B、甲=乙>丙 C、甲>乙>丙 D、乙>甲>丙。三、实验探究题
-
19. 3%的硼酸溶液可用于清洗皮肤的小面积创伤。现配制300g质量分数为3%的硼酸溶液,实验操作如下:
 (1)、量取水的体积:用量筒取mL水(ρ水=1g/cm3)。
(1)、量取水的体积:用量筒取mL水(ρ水=1g/cm3)。
(2)、溶解:用到的玻璃仪器是。(3)、若按照上述质量称量氯化钠时,将氯化钠放在天平的右盘中,砝码放在天平的左盘中,则会使配制的溶液溶质质量分数(填“偏大”“偏小”或“不变”)。在量取水的体积时,小刚同学俯视读数,则所配制溶液中氯化钠的质量分数(填“偏大”“偏小”或“不变”)。
20. 海洋是丰富的化学资源宝库.通过晾晒海水,可以得到含少量泥沙的粗盐.为了得到比较纯净的NaCl(不考虑可溶性杂质),设计了如图所示的实验操作: (1)、写出图示标号对应的名称:②;(2)、操作①②③都用到的仪器是 , 在步骤②中该仪器的作用是;(3)、操作③中看到时,停止加热,以防液体飞溅;(4)、某同学在进行操作①量水时用俯视量取15mL水,则他量得水的实际体积15mL(填> 或=或<)(5)、若粗盐的质量为9. 0克,精盐的质量为3. 6克,则该粗盐含有精盐的产率是 , 所得到的精盐属于(填“纯净物”或“混合物”),下列各组同学对造成产率偏高或偏低的原因分析,正确的是
(1)、写出图示标号对应的名称:②;(2)、操作①②③都用到的仪器是 , 在步骤②中该仪器的作用是;(3)、操作③中看到时,停止加热,以防液体飞溅;(4)、某同学在进行操作①量水时用俯视量取15mL水,则他量得水的实际体积15mL(填> 或=或<)(5)、若粗盐的质量为9. 0克,精盐的质量为3. 6克,则该粗盐含有精盐的产率是 , 所得到的精盐属于(填“纯净物”或“混合物”),下列各组同学对造成产率偏高或偏低的原因分析,正确的是A、烧杯里的食盐未溶解完就开始过滤,造成产率低
B、没有蒸发干,精盐中仍有水分,造成产率偏低
C、滤液浑浊就开始蒸发,造成产率偏高
D、蒸发时晶体飞溅,造成产率偏高
21. 小华同学配制50g溶质质量分数为20%的NaCl溶液,操作流程如图所示: (1)、小华同学应称取氯化钠的质量是g。
(1)、小华同学应称取氯化钠的质量是g。
(2)、指出图中的一处错误:。(3)、在用托盘天平称取食盐的过程中,发现指针已偏向分度盘左侧,他接下来的操作是。
(4)、在用量筒量取水的过程中,当液面接近刻度线时,他的操作如图所示,其中规范的是(填字母)。 (5)、如果小华配制的氯化钠溶液的溶质质量分数小于20%,则造成此误差的可能原因有____(填字母)。A、称量前天平没有调节平衡 B、称量纸上残留少量食盐 C、向烧杯中加水时,有少量水溅出烧杯外
(5)、如果小华配制的氯化钠溶液的溶质质量分数小于20%,则造成此误差的可能原因有____(填字母)。A、称量前天平没有调节平衡 B、称量纸上残留少量食盐 C、向烧杯中加水时,有少量水溅出烧杯外四、计算题
-
22. 鸡蛋壳的主要成分是碳酸钙(其它成分不溶于水也不与酸反应)。化学兴趣小组为了测定鸡蛋壳中碳酸钙的含量,做如下实验。反应①结束后,所加盐酸刚好反应了一半,反应②恰好完全反应。

请回答下列问题:
(1)、反应①的化学方程式为;(2)、根据已知条件列出求解碳酸钙质量(X)的比例式;(3)、该鸡蛋壳中碳酸钙的质量分数为;(4)、溶液b中溶质的质量分数为;(5)、用36.5%的浓盐酸配制80g上述稀盐酸需加水的质量为。