2018-2019学年粤教版化学九年级下册7.4结晶现象 同步训练
试卷更新日期:2019-01-15 类型:同步测试
一、单选题
-
1. 下列关于结晶的说法不正确的是( )A、结晶是指有规则几何形状的晶体从溶液中析出的过程 B、不同物质的晶体从溶液中析出后,其几何形状可能不相同 C、结晶必须在蒸发溶液的时候才能进行 D、把硝酸钾晶体从其溶液中结晶出来最好采用冷却热饱和溶液法2. 海水晒盐属于( )A、蒸发结晶 B、降温结晶 C、化学变化 D、以上都不是3. 把碳酸钙和硝酸钾分离的方法是( )A、溶解、结晶 B、溶解、蒸发 C、溶解、结晶、过滤 D、溶解、过滤、蒸发4. 甲、乙两种不含结晶水的固体物质的溶解度曲线如图所示。下列说法正确的是( )
 A、t1℃时,甲、乙两物质的饱和溶液中溶质的质量分数相等,且都等于 60% B、t2℃时,甲、乙两种物质的饱和溶液,降温至t1℃,析出晶体质量,甲不一定大于乙 C、t1℃时,将甲、乙两种物质的饱和溶液升温至t2℃时,溶质的质量分数甲大于乙 D、t1℃时,将甲、乙两种物质的饱和溶液分别降温到0℃,乙析出晶 体比甲析出晶体多5. 用化学知识解释生活中的一些现象,其中错误的是 ( )
A、t1℃时,甲、乙两物质的饱和溶液中溶质的质量分数相等,且都等于 60% B、t2℃时,甲、乙两种物质的饱和溶液,降温至t1℃,析出晶体质量,甲不一定大于乙 C、t1℃时,将甲、乙两种物质的饱和溶液升温至t2℃时,溶质的质量分数甲大于乙 D、t1℃时,将甲、乙两种物质的饱和溶液分别降温到0℃,乙析出晶 体比甲析出晶体多5. 用化学知识解释生活中的一些现象,其中错误的是 ( )选项
生活现象或实验现象
解释
A
用金属铝做高压线电线,而不用金属银
铝价钱低、密度小、易导电、抗腐蚀性强等
B
咸菜晾晒时,表面有白色食盐析出
溶剂蒸发饱和时有晶体析出
C
铁锈不与氧气反应,但却加快铁生锈速率
铁锈疏松多孔,易吸收水分
D
食盐溶于水不溶于豆油
食盐溶解与加入溶剂多少有关
A、A B、B C、C D、D6. 下表是NaCl和Na2CO3在不同温度下的溶解度,下列说法中错误的是( )温度/℃
0
10
20
30
40
溶解度/g
NaCl
35.0
35.5
36.0
36.5
37.0
Na2CO3
6.0
10.0
18.0
36.5
50.0
A、两种物质溶解度相等的温度在30℃ B、生活在盐碱湖附近的人们习惯“夏天晒盐、冬天捞碱” C、40℃时,5gNaCl中加10g水可得溶质质量分数为26.3%的溶液 D、40℃时,9g Na2CO3中加20g水,充分溶解后再降温到10℃,析出固体的质量为7g7. 在进行过滤操作时,除了使用铁架台、烧杯、玻璃棒以外,还需要的仪器是( )A、石棉网 B、漏斗 C、集气瓶 D、试管8. 关于过滤操作的下列叙述中,正确的是( )A、滤纸的边缘低于漏斗边缘,玻璃棒作用有搅拌、引流 B、液面可以高于滤纸边缘 C、过滤后滤液仍浑浊原因可能是不溶物堵塞滤纸 D、漏斗下端的管口置于烧杯的中间9. 误差分析是定量实验的一个重要内容,下列分析正确的是( )A、用量筒量取10mL水,仰视读数,会导致水的实际体积偏小 B、用托盘天平称取10.5g氯化钠,药品和砝码放反,会导致氯化钠偏多 C、粗盐提纯时,若溶解时加水量不足,会导致得到的精盐质量偏低 D、电解水时,氧气比氢气更易溶于水,会导致负极与正极的气体体积比小于2:1二、填空题
-
10. 人们通常把的过程叫做结晶.结晶的方法主要有和法.法是适用于一切把可溶于水的物质从溶液中分离出来的方法;法则特别适用于溶解度受温度影响大的物质,如等.11. 如图1是A、B、C三种物质的溶解度曲线图.请回答:

①t1℃时,溶解度相等的两种物质是 .
②B的饱和溶液中混有少量的物质A,要除去A得到较纯的B物质,可采用的结晶方法是 .
③如图2所示,在大烧杯中加入一定量的硝酸铵固体后,甲试管内出现的现象是 , 乙试管内的溶液为溶液(填“饱和”或“不饱和”).
12. 如图是甲、乙、丙三种物质的溶解度曲线.回答下列问题: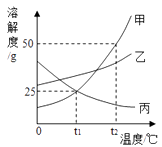
①t1℃时,甲的溶解度为;
②现有甲、乙、丙三种物质的浓溶液,适用海水晒盐原理进行结晶提纯的是;
③t3℃时,甲的饱和溶液中含有少量的丙,现要提纯甲可采用的方法是;
④下列说法正确的是 .
A.t2℃时把50g甲放入50g水中所得到甲的饱和溶液中溶质与溶液的质量比为1:2
B.t2℃时,等质量的甲、乙、丙分别制成饱和溶液,需水的质量最多的是甲
C.t1℃时,甲、乙、丙三种溶液分别升温,其浓度都不可能发生变化
D.t1℃时,向100g20%甲的饱和溶液中加100g水,充分搅拌,溶液的浓度为10%
E.t2℃时,将甲、乙、丙三种物质的饱和溶液降温至t1℃,这三种溶液的溶质质量分数的大小关系是乙>甲=丙
F.t1℃时,甲、乙、丙三种溶液的浓度可能相等.
三、综合题
-
13. 结合下表给出的KNO3、NaCl两种固体物质的溶解度,回答有关问题:
0℃
20℃
40℃
60℃
80℃
100℃
KNO3
13.3g
31.6g
63.9g
110g
169g
246g
NaCl
35.7g
36.0g
36.6g
37.3g
38.4g
39.8g
(1)、20℃时,将40gKNO3放在100水中充分溶解,所得溶液的质量是 g;(2)、20℃时,将接近饱和的KNO3溶液转化为该温度下的KNO3饱和溶液,可使用的方法是(写一种即可);(3)、这两种物质中,溶解度受温度变化影响较小的是;(4)、NaCl中有少量 KNO3杂质,提纯NaCl应使用的方法是(选填“蒸发结晶”或“降温结晶”)。14. 溶液对于自然界中的生命活动和人类生产活动具有重要的意义,多角度认识溶液有助于指导我们的生活。(1)、关于溶液的说法,正确的是(填写标号)A.溶液中各部分的性质相同
B.均一、稳定的液体一定是溶液
C.浓溶液不一定是饱和溶液
D.溶液加水稀释后溶质的质量变小
(2)、表1是部分物质在20℃时的溶解性;表Ⅱ是氯化钠、碳酸钠在不同温度时的溶解度。离子
OH-
Cl-
CO32-
SO42-
K+
溶
溶
溶
溶
Mg2+
不
溶
微
溶
.Ba2+.
溶
溶
不
温度 (℃)
0
10
20
30
40
氯化钠(g)
35
35.5
36
36.5
37
碳酸钠(g)
6
10
18
36.5
50
表1空格中应填写;分析表Ⅱ可知,氯化钠和碳酸钠的饱和溶液溶质质量分数相同时的温度是。
(3)、简单解释“夏天晒盐、冬天捞碱”的科学原理。四、实验探究题
-
15. 物质提纯是生活和科学研究的需要。
某化学兴趣小组的同学做粗盐(含有难溶性杂质)提纯实验,下图是粗盐提纯实验的操作示意图。

请回答下列问题:
① 下列说法错误的是
A.此实验只能除去不溶性的杂质
B.称量粗盐是为了计算产率和计算量取水的体积
C.操作F时若滤纸没有紧贴漏斗内壁,则会影响过滤速度
D.蒸发结晶时,蒸发皿应放在石棉网上加热
② 操作C中用玻璃棒的作用是。
③ 操作F的错误是 , 本操作完成后若发现滤液仍然浑浊,但滤纸未破损,可能的原因是。(写一条)
④ 粗盐提纯实验的操作顺序为(填操作字母)、称量精盐并计算产率。
⑤ 操作D中,当观察到时,停止加热。