2018-2019学年粤教版化学九年级下册第六单元测试卷
试卷更新日期:2019-01-15 类型:单元试卷
一、单选题
-
1. “绿箱子环保计划——废弃手机及配件回收联合行动”已在全国40个重点城市开展了多 年。下列有关废弃手机中的金属材料回收利用的说法错误的是( )
A、可以节约金属资源 B、可以节约冶炼相关金属所消耗的能源 C、可以减少对环境的污染 D、回收废弃手机中的金属材料没有任何价值2. 物质的性质在很大程度上决定物质的用途,以下性质和用途的对应错误的是( )A、金属钨的熔点高﹣﹣可作保险丝 B、氮气化学性质稳定﹣﹣用作食品防腐 C、金刚石坚硬﹣﹣用于裁玻璃 D、氧气能供给呼吸﹣﹣用于医疗急救3. 金属钛有银白色金属光泽,密度为4.5g/cm3 , 熔点为1725℃,具有良好的延展性和耐腐蚀性。下列物品不能用钛制作的是( )A、保险丝 B、医疗器械 C、潜艇外壳 D、眼镜架4. 下列实验不能达到实验目的的是( )A、 验证质量守恒定律 B、 检查装置气密性
B、 检查装置气密性  C、 CO2 验满
C、 CO2 验满  D、 比较材料硬度
D、 比较材料硬度  5. 据悉预计2018年11月初,哈市东部地区新増的一条过江通道——“新东江桥”滨北线松花江 公铁两用桥江南江北引桥将达到通车条件。下列有关说法错误的是( )
5. 据悉预计2018年11月初,哈市东部地区新増的一条过江通道——“新东江桥”滨北线松花江 公铁两用桥江南江北引桥将达到通车条件。下列有关说法错误的是( ) A、草绿色的防眩板具有美化景观,解决对向车灯眩光,保证行车安全等作用 B、青黑色的沥青路面所用的沥青来自石油加热炼制 C、亮黄色的桥头堡在建筑中会用熟石灰和沙子混合来砌砖,用石灰浆粉刷墙壁 D、珠白色的路灯杆是由纯铁制成的,抗腐蚀性能好、坚固耐用属于金属材料6. 已知化学反应:X+YSO4═Y+XSO4 , 根据此反应信息判断正确的是( )A、X的金属活动性比Y强 B、Y的金属活动性比X强 C、X一定是金属铁 D、Y一定是金属铜7. 2018年5月我国自主建造的第一艘航母下海,为保证航母的使用寿命,下列防锈措施不可行的是( )A、用抗锈蚀性能优异的合金制造航母零部件 B、刷防锈漆 C、船体表面镀一层黄金 D、给某些部位涂油8. 下列主题知识归纳中完全正确的一组是( )
A、草绿色的防眩板具有美化景观,解决对向车灯眩光,保证行车安全等作用 B、青黑色的沥青路面所用的沥青来自石油加热炼制 C、亮黄色的桥头堡在建筑中会用熟石灰和沙子混合来砌砖,用石灰浆粉刷墙壁 D、珠白色的路灯杆是由纯铁制成的,抗腐蚀性能好、坚固耐用属于金属材料6. 已知化学反应:X+YSO4═Y+XSO4 , 根据此反应信息判断正确的是( )A、X的金属活动性比Y强 B、Y的金属活动性比X强 C、X一定是金属铁 D、Y一定是金属铜7. 2018年5月我国自主建造的第一艘航母下海,为保证航母的使用寿命,下列防锈措施不可行的是( )A、用抗锈蚀性能优异的合金制造航母零部件 B、刷防锈漆 C、船体表面镀一层黄金 D、给某些部位涂油8. 下列主题知识归纳中完全正确的一组是( ) A、A B、B C、C D、D9. 相同质量的Mg、Fe分别与稀盐酸作用,产生H2的质量m(H2)与加入稀盐酸的体积V(稀盐酸)关系如下图所示,其中正确的是( )
A、A B、B C、C D、D9. 相同质量的Mg、Fe分别与稀盐酸作用,产生H2的质量m(H2)与加入稀盐酸的体积V(稀盐酸)关系如下图所示,其中正确的是( )
A、 B、
B、 C、
C、 D、
D、 10. 控制变量法是实验探究的重要方法。利用下图所示实验不能实现探究目的是 ( )
10. 控制变量法是实验探究的重要方法。利用下图所示实验不能实现探究目的是 ( )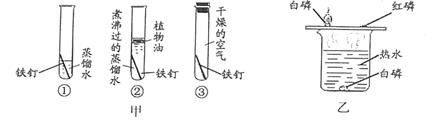 A、甲中①②对比可探究铁的锈蚀与植物油是否有关 B、甲中①③对比可探究铁的锈蚀与水是否有关 C、乙可探究可燃物的燃烧是否需要达到一定温度 D、乙可探究可燃物的燃烧是否需要与氧气接触11. 下列不能作为判断金属Mg 、Fe 、Cu三种金属活动性强弱的是( )A、在纯氧中燃烧的现象 B、与盐酸反应的快慢程度 C、金属导电性强弱 D、三种金属发现和利用的年代的先后顺序12. “愚人金”实为铜锌合金,外观与黄金极为相似,常被不法商贩冒充黄金牟取暴利,下列关于鉴别“愚人金”与黄金的实验方案,合理的是
A、甲中①②对比可探究铁的锈蚀与植物油是否有关 B、甲中①③对比可探究铁的锈蚀与水是否有关 C、乙可探究可燃物的燃烧是否需要达到一定温度 D、乙可探究可燃物的燃烧是否需要与氧气接触11. 下列不能作为判断金属Mg 、Fe 、Cu三种金属活动性强弱的是( )A、在纯氧中燃烧的现象 B、与盐酸反应的快慢程度 C、金属导电性强弱 D、三种金属发现和利用的年代的先后顺序12. “愚人金”实为铜锌合金,外观与黄金极为相似,常被不法商贩冒充黄金牟取暴利,下列关于鉴别“愚人金”与黄金的实验方案,合理的是比较硬度,硬度小的是“愚人金”
灼烧,表面变色的是“愚人金”
浸没在稀硫酸中,表面有气泡产生的是“愚人金”
浸没在硫酸锌溶液中,表面附着白色物质的是“愚人金”
A、 B、 C、 D、13. 下列方法不能达到除杂的目的的是( )选项
物质(括号内为杂质)
方法
A
N2(O2)
将混合气体通过灼热铜网
B
Fe粉(炭粉)
加入足量稀H2SO4充分反应,过滤、洗涤、干燥
C
CaO(CaCO3)
高温煅烧
D
FeCl2溶液(CuCl2)
加入足量Fe粉,过滤
A、A B、B C、C D、D14. 小柯为比较Mg、Fe、Cu三种金属的活动性顺序,进行了如图甲所示的实验。实验后把两试管中的物质倒入烧杯中(如图乙),发现烧杯内的红色固体明显增多,充分反应后过滤。滤液中含有的金属离子可能的组成有( )
①Mg2+ ②Mg2+和Fe2+ ③Fe2+和Cu2+ ④Mg2+、Fe2+和Cu2+
A、①② B、①③ C、②④ D、③④15. 将一定量的金属M加入到含有硝酸锌、硝酸铜、硝酸银的混合溶液中,充分反应后过滤,得到滤渣和滤液,根据实验分析,下列说法正确的是( )①若滤液为蓝色,则滤渣中一定不含锌和M
②若滤液只含一种溶质,滤渣含四种金属,则几种金属活动性顺序:M>锌>铜>银
③若滤渣含有M,则滤液中的溶质种类最多含3种,最少含一种
④向滤渣中加入稀盐酸产生无色气体,则滤渣中一定含锌,可能含M
A、②④ B、①④ C、②③ D、①③二、填空题
-
16. 化学源于生活,生活中蕴含着许多化学知识。(1)、石墨与金刚石的物理性质不同,原因是。(2)、除去食盐水中混有的泥沙,常用的方法是;(3)、生活中把硬水转化为软水,常用的方法是。(4)、氯化钠是重要的调味品,它由(填“分子”“原子”或“离子”)构成。(5)、铁锅容易生锈的原因是。17. 已知锰的金属活动性介于锌和铁之间,请选择下列试剂或药品的组合设计实验方案来验证锰、锌、铁三者的活动性顺序:MnCl2溶液、ZnCl2溶液、FeCl2溶液、铁粉、锌粉、锰粉、稀硫酸;若选三种药品或试剂即可完成实验,你的组合是AB
18. 国际上提倡向中国人学习用铁锅炒菜。工业上常用赤铁矿(主要成分氧化铁)和一氧化碳冶炼生铁,该反应的化学方程式为。用铁锅炒菜时,油锅中的油不慎起火,只需一个简单的操作,火就熄灭了,该操作是 , 其灭火的原理是。
19. 以下是探究Fe、Cu、Ag三种金属活动性的实验。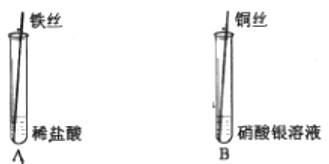
①A中观察到铁丝表面;
②B中发生反应的化学方程式为 , 该实验过程中可观察到的现象有
a.冒气泡
b.出现海绵状银白色固体
c.铜丝表面变黑
d.无色溶液变为蓝色
③为达到实验目的,还需补充一个实验(写成所需试剂化学式)。
三、综合题
-
20. 将下列有关性质、变化、现象不同的原因填写在横线上:(1)、生铁和钢性能不同,主要原因是二者的不同;(2)、硫在空气中和在氧气中燃烧的现象不同,原因是不同;(3)、金刚石和石墨都由碳元素组成,但由于不同,它们的性质存在着明显差异。21. 哈尔滨市大力发展绿色公交,城区主干线路陆续实现了绿色公交车全覆盖。新的公交车型是充电节能减排空调车,要求做到零排放。
请回答:
 (1)、汽车实现零排放,就是不排放废气(答两种废气)(2)、充电汽车使用的空调其能量转化是;(3)、淘汰的汽车要回收金属材料,这样不仅节约 , 而且减少。22. 物质王国举行一场趣味篮球赛。某队由铁、二氧化碳、盐酸、氢氧化钙溶液、硫酸铜溶液五名“队员”组成,比赛中,由硫酸铜溶液“队员”发球,“队员”间传接球,最后由丁位置“队员”投篮进球完成一次有效进攻。场上“队员”位置及传球路线如图所示,图中连线物质间能发生反应。
(1)、汽车实现零排放,就是不排放废气(答两种废气)(2)、充电汽车使用的空调其能量转化是;(3)、淘汰的汽车要回收金属材料,这样不仅节约 , 而且减少。22. 物质王国举行一场趣味篮球赛。某队由铁、二氧化碳、盐酸、氢氧化钙溶液、硫酸铜溶液五名“队员”组成,比赛中,由硫酸铜溶液“队员”发球,“队员”间传接球,最后由丁位置“队员”投篮进球完成一次有效进攻。场上“队员”位置及传球路线如图所示,图中连线物质间能发生反应。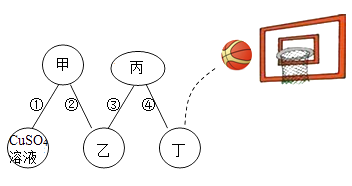
回答下列问题:
(1)、已知丁位置上投篮的“队员”是个灭火“能手”,则甲位置的“队员”代表的物质是。(填化学式)(2)、乙位置的“队员”所代表的物质的一种用途是。(3)、连线④代表的物质间发生反应的方程式为。(4)、连线①②③④代表物质间发生的化学反应中,基本反应类型相同的是。(填序号)23. 由A和B两种物质组成的混合物,可实现下图转化关系,试判断: (1)、写出下列物质的化学式:A;D; F;(2)、写出反应①的化学方程式:写出反应③的化学方程式:
(1)、写出下列物质的化学式:A;D; F;(2)、写出反应①的化学方程式:写出反应③的化学方程式:四、实验探究题
-
24. 小聪同学家新换了水龙头,从说明书上了解到该水龙头是铜质镀铬。好奇的小聪想探究铬(Cr)与常见金属铁、铜的活动性强弱,邀请你一同参加。(1)、【知识回放】金属活动性顺序:K Ca Na Mg Al Zn Sn Pb (H) Hg Ag Pt Au
请你在横线上填写对应金属的元素符号。
(2)、【作出猜想】猜想1.Cr>Fe>Cu; 猜想2. Fe>Cu >Cr; 猜想3.你的猜想是。(3)、【查阅资料】①铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜。②铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液。
【设计与实验】
小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸。
实验
试管1
试管2
试管3
实验操作
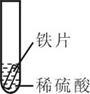
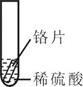
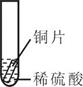
实验现象
铁片表面产生气泡较慢,溶液变成色
铬片表面产生气泡较快,溶液变成为蓝色
无明显现象
【结论与解释】
①小聪得到的结论是猜想正确。
②实验前用砂纸打磨金属片的目的是。
(4)、【知识运用】①将铬片投入FeSO4溶液中,反应(填“能”或“不能”)进行。若能进行,请你写出反应的化学方程式。
②铬片与铜片互相刻划时,在的表面可留下划痕,可以比较出这两种金属的硬度。
③向AgNO3和Cu(NO3)2的混合溶液中加入过量铬粉,充分反应后过滤,滤渣中一定含有。
25. 在高温的条件下,用CO还原金属氧化物ZnO和Fe2O3的混合粉末。[提出问题]在高温的条件下,CO能还原ZnO和Fe2O3混合粉末吗?
(1)、[进行假设]上述猜想正确,请写出其中CO充分还原Fe2O3的化学方程式为①;(2)、[设计实验]教材中设计下列实验,填写实验报告: (3)、[提出问题] 实验后的粉末一定是Zn和Fe吗?
(3)、[提出问题] 实验后的粉末一定是Zn和Fe吗?[设计实验] 实验后,为证明玻璃管中的粉末是Zn和Fe,请你设计下列两个实验:

[反思交流]
①实验1:反应的化学方程式可能是③;
②实验2:观察到的现象是:粉末消失,溶液的颜色④;
③在上述CO还原ZnO和Fe2O3混合粉末装置中,为节省燃料,请你提出在原装置基础上的一种改进方法是⑤;
(4)、[拓展应用] CO能还原某些金属氧化物,在工业上可用于炼铁。在用赤铁矿炼铁时(如图),从高炉里流淌出的高温红热的生铁水没有大量氧化,有多种因素,你所知道的主要原因是:⑥。 26. 世界上每年都有将近总产量十分之一的钢铁锈蚀,造成了巨大的经济损失。为探究铁锈蚀的原因,分别取3枚洁净无锈的铁钉放入试管中,进行如下实验:
26. 世界上每年都有将近总产量十分之一的钢铁锈蚀,造成了巨大的经济损失。为探究铁锈蚀的原因,分别取3枚洁净无锈的铁钉放入试管中,进行如下实验: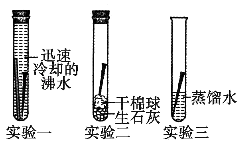 (1)、进行实验一时,老师指导同学们先向迅速冷却后的沸水中,放入一截打磨光亮的略长于铁钉的镁带,几分钟后再放入铁钉。镁带的作用是。(2)、大多数同学都观察到了实验一、实验二中铁钉无锈,实验三中铁钉生锈的现象,得出铁生锈的条件是。某同学却发现本组实验二中的铁钉表面出现了少量铁锈,经仔细检查后发现胶塞已塞紧,产生这种现象的原因可能是。(3)、工业上用锈蚀的废旧铁制品可以回炉炼铁,原理是(用化学方程式表示)。在生活中人们对废旧金属合理的处理方法通常有(写一种)。
(1)、进行实验一时,老师指导同学们先向迅速冷却后的沸水中,放入一截打磨光亮的略长于铁钉的镁带,几分钟后再放入铁钉。镁带的作用是。(2)、大多数同学都观察到了实验一、实验二中铁钉无锈,实验三中铁钉生锈的现象,得出铁生锈的条件是。某同学却发现本组实验二中的铁钉表面出现了少量铁锈,经仔细检查后发现胶塞已塞紧,产生这种现象的原因可能是。(3)、工业上用锈蚀的废旧铁制品可以回炉炼铁,原理是(用化学方程式表示)。在生活中人们对废旧金属合理的处理方法通常有(写一种)。五、计算题
-
27. 黄铜(铜锌合金)的外观与黄金极为相似、容易以假乱真。小红同学想测定黄铜中锌的含量。她称取20g黄铜样品放入烧杯中,加入足量稀硫酸充分反应后,测得生成氢气的质量为0.2g。(1)、该反应属于(填基本反应类型)。(2)、求黄铜样品中锌的质量分数为多少(写计算过程)。28. 金属材料包括纯金属以及它们的合金。(1)、铁锅、铝锅和铜火锅可以用来炒菜、做饭和涮肉,是因为铁、铝、铜能够。(2)、为了验证铁、铝、铜的金属活动性顺序,某同学选择了打磨过的铁丝,他还需要选择的两种盐溶液是。写出实验中发生反应的化学方程式:。(3)、炼铁的原理是利用一氧化碳与氧化铁的反应,化学方程式为 , 该反应中氧化铁表现出(填“氧化性”或“还原性”)。右图是炼铁高炉示意图,写出原料焦炭的一个作用:。
 (4)、5g某钢样在纯氧中完全燃烧,得到0.33g二氧化碳。求此钢样中碳的质量分数。(写出计算过程)
(4)、5g某钢样在纯氧中完全燃烧,得到0.33g二氧化碳。求此钢样中碳的质量分数。(写出计算过程)