上海市普陀区2016-2017学年九年级上学期化学期末考试试卷
试卷更新日期:2019-01-07 类型:期末考试
一、单选题
-
1. 我国古代技术应用中,其工作原理不涉及化学变化的是( )A、粮食酿酒 B、棉线织布 C、冶炼金属 D、烧制陶瓷2. 人体中缺少铁元素会导致的疾病是( )A、骨质疏松 B、贫血 C、老年痴呆 D、大脖子病3. 下列物质中属于单质的是( )A、水 B、碳六十 C、生石灰 D、熟石灰4. 下列化学用语及其表述正确的是( )A、Cl2 两个氧元子 B、3S 三个碳元素 C、FeCl2 氯化铁 D、Mg 一个镁原子5. 下列物质中属于混合物的是( )A、水银 B、冰水混合物 C、空气 D、明矾6. 生活中常见的物质pH大于7的是( )A、蔗糖溶液 B、肥皂水 C、食醋 D、食盐水7. +4价氮元素形成的氧化物分子式是( )A、NO B、N2O C、NO2 D、N2O58. 丙烯酸(C3H4O2)可用于制取“尿不湿”,下列有关丙烯酸的说法正确的是( )A、C3H4O2是混合物 B、—个丙烯酸分子由3个碳原子、4个氢原子和一个氧分子构成 C、其中碳、氢元素的物质的量之比为9:1 D、丙烯酸的式量为729. 下列物质的性质与所对应的用途没有关系的是( )A、氧气助燃 焊接金属 B、稀有气体通电发有色光 保护气 C、石墨导电 可用作电极 D、二氧化碳进行光含作用 植物的肥料10. 下列实验操作错误的是( )A、用电子天平称取2.35克氯化钠 B、用10mL的量筒量取8mL的水 C、用50mL的烧样置取大约20mL的水 D、用石蕊测定某溶液的pH值11. 一定会影响物质溶解度的是( )A、温度 B、压强 C、溶剂的量 D、溶质的质量12. 下图表示的是电解水的微观模型图,根据质量守恒可知该模型图中还需要添加的微粒是( )
 A、
A、 B、
B、 C、
C、 D、
D、 13. 下列实验现象描述错误的是( )A、硫在氧气中燃烧,火焰呈蓝紫色 B、氢氧化钠溶液中滴加硫酸铜溶液,生成蓝色絮状硫酸铜沉淀 C、在大理石上滴加稀盐酸,有气泡产生 D、镁带在空气中燃烧,发出耀眼白光,生成白色粉末14. 下列反应的表达式正确的是( )A、木炭在空气中燃烧:C+O2
13. 下列实验现象描述错误的是( )A、硫在氧气中燃烧,火焰呈蓝紫色 B、氢氧化钠溶液中滴加硫酸铜溶液,生成蓝色絮状硫酸铜沉淀 C、在大理石上滴加稀盐酸,有气泡产生 D、镁带在空气中燃烧,发出耀眼白光,生成白色粉末14. 下列反应的表达式正确的是( )A、木炭在空气中燃烧:C+O2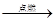 CO2↑
B、铁在氧气中燃烧:4Fe+3O2
CO2↑
B、铁在氧气中燃烧:4Fe+3O2 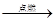 2Fe2O3
C、镁在氧气中燃烧:Mg+O2
2Fe2O3
C、镁在氧气中燃烧:Mg+O2 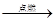 MgO
D、水通电电解2H2O
MgO
D、水通电电解2H2O 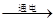 2H2↑+O2↑
15. 物质的两是国际单位制中的一个基本物理量,有关说法正确的是( )A、物质的量符号是N B、物质的量单位是mol C、物质的量就是物质的质量 D、1摩尔任何物质一定含有6.02×1023个微粒16. 将10g质量分数为0.1的氢氧化钠溶液浓度变为0.2,下列操作正确的是( )A、蒸发5g水 B、加入氧化钠固体0.1g C、倒出一半溶液 D、加入10g质量分数为0.2的氢氧化钠溶液17. 下列实验设计中,不能证明二氧化碳的化学性质的是( )A、
2H2↑+O2↑
15. 物质的两是国际单位制中的一个基本物理量,有关说法正确的是( )A、物质的量符号是N B、物质的量单位是mol C、物质的量就是物质的质量 D、1摩尔任何物质一定含有6.02×1023个微粒16. 将10g质量分数为0.1的氢氧化钠溶液浓度变为0.2,下列操作正确的是( )A、蒸发5g水 B、加入氧化钠固体0.1g C、倒出一半溶液 D、加入10g质量分数为0.2的氢氧化钠溶液17. 下列实验设计中,不能证明二氧化碳的化学性质的是( )A、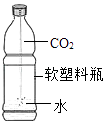 B、
B、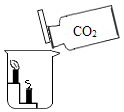 C、
C、 D、
D、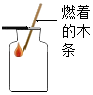 18. 粗盐提纯过程中.称量、溶解、过滤、蒸发四个环节中一定用到烧杯的是( )A、称量、溶解、过滤、蒸发 B、溶解、过滤 C、溶解、过滤、蒸发 D、过滤19. 将二氧化碳气体缓缓通入质量分数为0.2的氢氧化钠溶液中,溶液中某元素质量分数 随时间变化的趋势如图,则 坐标表示的是( )
18. 粗盐提纯过程中.称量、溶解、过滤、蒸发四个环节中一定用到烧杯的是( )A、称量、溶解、过滤、蒸发 B、溶解、过滤 C、溶解、过滤、蒸发 D、过滤19. 将二氧化碳气体缓缓通入质量分数为0.2的氢氧化钠溶液中,溶液中某元素质量分数 随时间变化的趋势如图,则 坐标表示的是( ) A、钠元素的质量分数 B、氧元素的质量分数 C、氢元素的质量分数 D、碳元素的质量分数
A、钠元素的质量分数 B、氧元素的质量分数 C、氢元素的质量分数 D、碳元素的质量分数二、填空题
-
20. 自然界中广泛存在碳元素,请完成下列填空:
自然界中,碳元素存在状态有游离态和 , 写出一种碳单质的名称;
② 采用木炭取暖,不通风往往会形成有毒的一氧化碳,写出该反应的化学方程式;而一氧化碳的产生,人们往往不能感知,是由于其具有的物理性质。
葡萄糖(C6H12O6)可为人体提供能量来源,葡萄糖中碳、氢、氧原子的物质的量之比是;葡萄糖中碳元素的质量分数为
21. 化学实验室常采用白磷来进行一些实验,已知白磷着火点是40℃,红磷着火点是240℃,请回答下列问题:白磷与红磷为同一元素形成的不同单质,该现象称为
利用图作装置测定空气中氧气的体积分数,白磷燃烧的现象是;化学方程式是

利用图右所示装置进行实验,热水温度一定要超过℃白磷才会燃烧,如果该实验换用红磷,就不能对比得出燃烧的条件之一“着火点”,理由是
用二氧化碳溶解白磷,用该溶液将滤纸浸润,挂起晾干,不久滤纸就会燃烧,这种现象称为
 22. A,B,C三种固体物质(均不含结晶水)的溶解度曲线如图所示
22. A,B,C三种固体物质(均不含结晶水)的溶解度曲线如图所示
t1℃时,B物质的溶解度是g/100g水
t2℃时,将15g A加入到g水中,完全溶解后,恰好得到饱和溶液;为了进一步提高该溶液的质量分数,可以进行的操作是
若将t2℃时三种物质的饱和溶液分别降温到t1℃,降温后质量分数最小的是物质的溶液(填“A”、“B”或“C”)
对于溶解度曲线上的点p,以下描述中一定正确的是(填字母序号)
a.B,C的溶液溶质质量分数相同
b. C的溶液100g中有10g溶液
c. B的溶液处于不饱和状态
d. A、C的溶液质量相同
⑤取A、B的混合物50g溶于100g水,待冷却到t1℃,若A析出而B不析出,则混合物中A的质量分数 的取值范围是(质量分数用分数或小数表示)
23. 实验室常用下列仪器来制取某些气体:
(注:导管、塞子省略)
图中仪器“D”的名称是;仪器“F”的名称是
实验室中利用氯酸钾分解来制取氧气,发生反应的化学方程式是;固体粉末送入试管底部,除钥匙外还可以用;如果用排气法收集氧气,必须验满,方法是;
利用双氧水分解制取氧气,上述仪器一定用不到是和(均填写编号)
氯酸钾或双氧水制取氧气,两个反应原理相同的是(写出一点即可),无论哪种方法获得一瓶氧气,上述仪器中除铁架台外还一定要用到的是(填写编号)
24. 大理石、石灰石中主要成分是CaCO3 , 碳酸钙在工业生产,生活及化学实验室中均有大量的应用。(1)、实验室利用大理石并采用下列装置来制取CO2
若采用图甲发生装置,则块状大理石应放在(填写A、B、C编号),若用图丙装置进行反应,使过程中不足之处是
(2)、某种大理石含CaCO3的质量分数为0.8,用该大理石100g与足量盐酸反应制取二氧化碳,(杂志不与盐酸反应,写出计算过程)求:该大理石中含CaCO3多少克?
反应中最多可得到的二氧化碳为多少摩尔?
(3)、实验室利用石灰石(含有加热不分解的杂质)进行如下实验:实验室利用下图装置模拟工业上石灰石的分解,为了充分反应,实验选用(填“块”或“粉末”)状的石灰石,分解得到的氧化钙的用途之一是
实验过程中,为验证石灰石分解,可将导管伸入溶液中,发生的化学方程式是

实验完毕,待固体冷却后,为验证石灰石是否完全分解,切实可行的操作是(选填编号)
加入稀盐酸,观察是否有气泡产生
加入大量水,观察是否放热
称量固体,固体食量减少
加大量水,观察是否有不溶物存在