浙江省慈溪市2017-2018学年九年级上学期科学10月区域联考试卷
试卷更新日期:2018-12-29 类型:月考试卷
一、选择题
-
1. 实验是学习科学的重要方法,下列实验操作正确的是( )A、
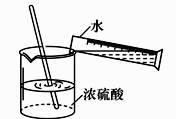 稀释浓硫酸
B、
稀释浓硫酸
B、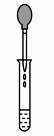 用滴管滴液
C、
用滴管滴液
C、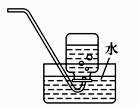 收集二氧化碳气体
D、
收集二氧化碳气体
D、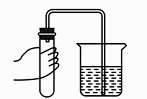 检查气密性
2. “一路一带”是跨越时空的伟大构思,赋予古丝绸之路崭新的时代内涵。丝绸之路将中国的发明和技术传送到国外。下列属于物理变化的是( )A、烧制陶瓷 B、蚕丝织布 C、使用火药 D、冶炼金属3. 与金属锌、氧化铜粉末、烧碱溶液和氯化钡溶液都能反应的物质是( )A、硫酸钠溶液 B、食盐水 C、稀盐酸 D、稀硫酸4. 下列各组物质的溶液不能发生复分解反应的是 ( )A、HCl和Ca(OH)2 B、Na2CO3和H2SO4 C、AgNO3和BaCl2 D、KCl和CuSO45. 如图,为检查装置的气密性,保持装置内温度不变,将导管的末端深入装有水的烧杯中.若装置的气密性良好,烧杯内导管处的现象(画圈部分)是( )
检查气密性
2. “一路一带”是跨越时空的伟大构思,赋予古丝绸之路崭新的时代内涵。丝绸之路将中国的发明和技术传送到国外。下列属于物理变化的是( )A、烧制陶瓷 B、蚕丝织布 C、使用火药 D、冶炼金属3. 与金属锌、氧化铜粉末、烧碱溶液和氯化钡溶液都能反应的物质是( )A、硫酸钠溶液 B、食盐水 C、稀盐酸 D、稀硫酸4. 下列各组物质的溶液不能发生复分解反应的是 ( )A、HCl和Ca(OH)2 B、Na2CO3和H2SO4 C、AgNO3和BaCl2 D、KCl和CuSO45. 如图,为检查装置的气密性,保持装置内温度不变,将导管的末端深入装有水的烧杯中.若装置的气密性良好,烧杯内导管处的现象(画圈部分)是( )选项
A
B
C
D
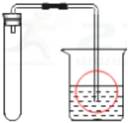
现象放大图
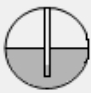
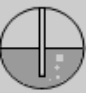
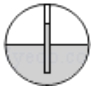
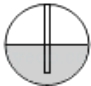 A、A B、B C、C D、D6. “接龙”是化学扑克(和普通扑克相似牌面标注物质的化学式)的一种游戏,其规则是:当上家出牌时,下家跟出的牌所标注的物质必须能与上家的反应。某局游戏中,甲到戊五人各有一张不同的牌,牌面标注有“CuSO4”、“H2SO4”、“NaOH”、“Fe”、“Fe2O3”,若甲的牌是“Fe2O3”,且每人按甲→乙→丙→丁→戊依次出牌时能满足规则的,则丁的牌一定是( )A、NaOH B、Fe C、H2SO4 D、CuSO47. 下列由实验现象得到的结论,正确的是 ( )A、向某溶液中加入BaCl2溶液,生成不溶于稀HNO3的白色沉淀,说明该溶液中必含SO42- B、将某固体加入到稀盐酸中,有气泡产生,说明此固体一定是金属 C、氯化钠晶体不导电,说明氯化钠晶体不含离子 D、向某溶液中滴加无色酚酞试液,酚酞试液变红色,说明该溶液显碱性8. 在Ca(OH)2的饱和溶液中,加入下列物质,不能使溶液的pH有明显改变的是( )A、CO2 B、HCl C、CuCl2 D、CaO9. 盛有饱和氢氧化钠溶液的烧杯在空气中放置一段较长时间,该溶液中的( )A、氧氧化钠的质量减小 B、氧氧化钠的质量保持不变 C、氧氧化钠的质量分数增大 D、氧氧化钠的质量分数保持不变10. 硝酸钾溶液中混有Mg2+、Ba2+、Ag+三种金属离子,现用KOH、K2CO3、KCl三种试剂使它们成为沉淀分离出来,要求每次只加一种试剂,滤出一种沉淀,最后达到除去杂质的目的,则所加试剂顺序正确的是( )A、KCl、KOH、K2CO3 B、KCl、K2CO3、KOH C、K2CO3、KOH、KCl D、KOH、KCl、K2CO311. 下列除去杂质的方法中,错误的是( )
A、A B、B C、C D、D6. “接龙”是化学扑克(和普通扑克相似牌面标注物质的化学式)的一种游戏,其规则是:当上家出牌时,下家跟出的牌所标注的物质必须能与上家的反应。某局游戏中,甲到戊五人各有一张不同的牌,牌面标注有“CuSO4”、“H2SO4”、“NaOH”、“Fe”、“Fe2O3”,若甲的牌是“Fe2O3”,且每人按甲→乙→丙→丁→戊依次出牌时能满足规则的,则丁的牌一定是( )A、NaOH B、Fe C、H2SO4 D、CuSO47. 下列由实验现象得到的结论,正确的是 ( )A、向某溶液中加入BaCl2溶液,生成不溶于稀HNO3的白色沉淀,说明该溶液中必含SO42- B、将某固体加入到稀盐酸中,有气泡产生,说明此固体一定是金属 C、氯化钠晶体不导电,说明氯化钠晶体不含离子 D、向某溶液中滴加无色酚酞试液,酚酞试液变红色,说明该溶液显碱性8. 在Ca(OH)2的饱和溶液中,加入下列物质,不能使溶液的pH有明显改变的是( )A、CO2 B、HCl C、CuCl2 D、CaO9. 盛有饱和氢氧化钠溶液的烧杯在空气中放置一段较长时间,该溶液中的( )A、氧氧化钠的质量减小 B、氧氧化钠的质量保持不变 C、氧氧化钠的质量分数增大 D、氧氧化钠的质量分数保持不变10. 硝酸钾溶液中混有Mg2+、Ba2+、Ag+三种金属离子,现用KOH、K2CO3、KCl三种试剂使它们成为沉淀分离出来,要求每次只加一种试剂,滤出一种沉淀,最后达到除去杂质的目的,则所加试剂顺序正确的是( )A、KCl、KOH、K2CO3 B、KCl、K2CO3、KOH C、K2CO3、KOH、KCl D、KOH、KCl、K2CO311. 下列除去杂质的方法中,错误的是( )选项
物质
杂质
除杂质的方法
A
稀硫酸
铜
过滤
B
CaSO4溶液
稀硫酸
过量CaCO3、过滤
C
FeCl2溶液
CuCl2
过量铁粉、过滤
D
二氧化碳
一氧化碳
点燃
A、A B、B C、C D、D12. 向AgNO3、Cu(NO3)2、Zn(NO3)2的混合溶液中加入一些铁粉,反应完成后过滤,下列情况不可能存在的是( )A、滤纸上有Ag、Cu、Fe,滤液中有Zn2+、Fe2+ B、滤纸上有Ag、Cu,滤液中有Zn2+、Fe2+ C、滤纸上有Ag、Cu,滤液中有Cu2+、Zn2+、Fe2+ D、滤纸上有Ag、Cu、Fe,滤液中有Cu2+、Zn2+、Fe2+13. 对于化学反应A+B=C+D的下列说法中,正确的是( )A、若A和D都是氧化物 ,则B和C中不可能再有氧化物 B、若A和C都是单质,B和D都是化合物,则该反应一定是置换反应 C、若A是可溶性碱,B是可溶性盐,则C和D不可能都是沉淀 D、若C和D分别是盐和水,则该反应一定是中和反应14. 如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球体积的影响)。则滴管和烧瓶中所用试剂可能是( )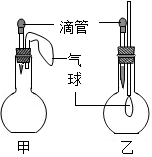
甲
乙
A
稀硫酸和铜片
水和 CO2
B
双氧水和MnO2
NaOH溶液和CO2
C
Na2CO3溶液和稀硫酸
Cu(OH)2和SO2
D
H2O和NH3
硝酸银溶液和HCl
A、A B、B C、C D、D15. 向烧杯中逐滴加入x溶液至过量(图甲),生成沉淀或气体的质量与加入x溶液的质量关系符合图乙的是 ( )

烧杯中的物质
x溶液
A
稀盐酸和硫酸铜溶液
烧碱溶液
B
稀硫酸和稀盐酸
氯化钡溶液
C
镁铝合金
稀盐酸
D
氯化钠和碳酸氢钠溶液
稀盐酸
A、A B、B C、C D、D二、简答题
-
16. 人类的生活和生产都离不开金属材料。(1)、下列物质不属于合金的是 。A、青铜 B、铁锈 C、钢 D、生铁(2)、在ZnCl2和CuCl2的混合溶液中,加入过量的铁粉,充分反应后过滤,所得滤液中含有的溶质是。17. 小强在厨房里发现一瓶没有标签的无色液体。(1)、他闻了闻,初步判断为白醋,小强是利用白醋的(填“物理”或“化学”)性质作出的判断。(2)、他另取少量此液体滴入石蕊试液,溶液变为色,要使其变为蓝色,可向其中加入 (填编号)
a、食盐 b、熟石灰 c、白酒 d、水
18. 为了激发学生学习科学的兴趣,老师在课堂上为大家做了一个“燃纸成铁”的趣味实验:将一张滤纸(组成元素为C、H、O)用FeCl3浓溶液湿润,在酒精灯上烘干后点燃,滤纸变黑、红热,最终生成黑褐色物质。老师告诉大家,黑褐色物质中含有单质铁,小阳同学对此进行了分析验证。(1)、从反应物的组成分析,因为有元素,反应后可能生成单质铁;(2)、将黑褐色物质放入稀盐酸中,发现有连续微小气泡产生,也可初步证明该黑褐色物质中含有单质铁。请写出相关的化学方程式;19. 从Fe、H2O、CO2、Ba(NO3)2、H2SO4、Na2SO411种物质中选择适当物质(每种物质只允许使用一次),分别写出符合下列要求的化学方程式:(1)、化合反应;(2)、复分解反应;(3)、置换反应;20. 探究学习小组在实验室中用如图所示装置制取CO2 , 并探究CO2与过氧化钠(Na2O2)的反应。其中,装置B的作用是吸收CO2中混有的HCl气体。
查阅资料得知:Ⅰ.过氧化钠(Na2O2)是一种淡黄色固体,能与CO2反应生成碳酸钠和氧气,也能与H2O发生反应:2Na2O2+H2O═4NaOH+O2↑; Ⅱ.NaOH溶液能与二氧化碳发生反应。
请回答下列问题:
(1)、装置A中发生反应的化学方程式为。利用A装置制取CO2的优点。(2)、写出过氧化钠(Na2O2)与CO2发生反应的化学方程式。(3)、装置D的作用是 。(4)、装置E中收集到的气体是(填化学式)21. 某同学为比较镁和铝的金属活动性强弱,将两块表面积相同并除去氧化膜的镁条、铝条分别与相同体积、相同质量分数的稀硫酸反应,测定两种金属与稀硫酸反应得到相同体积氢气所需要的时间。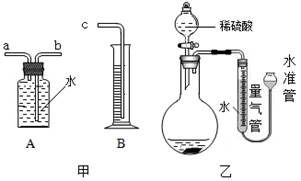 (1)、利用图甲中A、B仪器可以组装一套实验室测量氢气体积的装置,该装置导管的连接顺序是。(2)、图乙中量气管和水准管也可以用来测量氢气体积,为了准确地测量氢气体积,在读取量气管中液面读数的过程中,应注意 (填字母编号).A、读数时视线与凹液面最低处相平。 B、读数前应上下移动水准管,待两管液面相平再读数 C、保持水准管静止,待水准管中液面不再上升时再读数
(1)、利用图甲中A、B仪器可以组装一套实验室测量氢气体积的装置,该装置导管的连接顺序是。(2)、图乙中量气管和水准管也可以用来测量氢气体积,为了准确地测量氢气体积,在读取量气管中液面读数的过程中,应注意 (填字母编号).A、读数时视线与凹液面最低处相平。 B、读数前应上下移动水准管,待两管液面相平再读数 C、保持水准管静止,待水准管中液面不再上升时再读数三、实验探究题
-
22.
根据下列装置图回答问题(装置用代号表示)
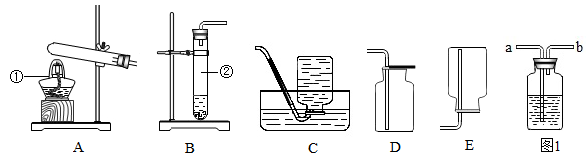 (1)、实验室常用氯化铵固体与碱石灰固体共热来制取氨气.常温下NH3是一种无色、有刺激性气味的气体,密度比空气小.NH3极易溶于水.制取并收集NH3 , 应该从上图中选择的制取和收集装置是;(2)、在医院里给病人输氧时,在氧气钢瓶和病人吸氧器之间连接一个类似右上图所示的装置,在装置中盛放大约半瓶蒸馏水,导气管(填“a”或“b”)端连接在供氧气
(1)、实验室常用氯化铵固体与碱石灰固体共热来制取氨气.常温下NH3是一种无色、有刺激性气味的气体,密度比空气小.NH3极易溶于水.制取并收集NH3 , 应该从上图中选择的制取和收集装置是;(2)、在医院里给病人输氧时,在氧气钢瓶和病人吸氧器之间连接一个类似右上图所示的装置,在装置中盛放大约半瓶蒸馏水,导气管(填“a”或“b”)端连接在供氧气的钢瓶上。
23. 现有一包固体粉末,可能是CaCO3、Na2CO3、Na2SO4、CuSO4、NaCl中的一种或几种,为确定其组成,取适量试样进行下列实验.请根据实验现象判断:(1)、取试样溶于水,得到无色澄清溶液,则此固体粉末中一定没有。(2)、取上述溶液适量,滴加过量的BaCl2溶液,出现白色沉淀,再加入过量的稀硝酸,沉淀部分消失并产生气泡.则此固体粉末中一定有 。(3)、取步骤(2)实验后的上层清液,加入稀硝酸、硝酸银溶液,出现白色沉淀,由此该同学得出此固体粉末中一定含有NaCl,你认为此结论是否正确(填“是”或“否”)。24. 已知常用的强酸(H2SO4、HCl、HNO3 , )跟常用的强碱(NaOH、KOH)反应生成的盐的水溶液呈中性,现将白色粉末溶入一无色中性液体中,按以下图示进行实验: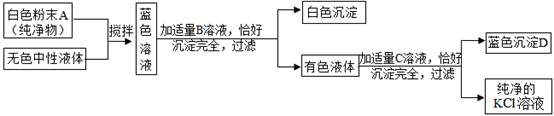 (1)、用化学式写出:B , D(2)、若无色中性液体是只含一种溶质的溶液,则溶质可能有哪几种情况?。(写化学式)25. 2015年中央电视台举办的“3.15”晚会,曝出某品牌金饰品掺假的事件,引起同学们的好奇。某化学兴趣小组在老师的帮助下,对几种常见金属饰品所含的金属进行了相关的探究活动。
(1)、用化学式写出:B , D(2)、若无色中性液体是只含一种溶质的溶液,则溶质可能有哪几种情况?。(写化学式)25. 2015年中央电视台举办的“3.15”晚会,曝出某品牌金饰品掺假的事件,引起同学们的好奇。某化学兴趣小组在老师的帮助下,对几种常见金属饰品所含的金属进行了相关的探究活动。【提出问题】①怎样鉴别真假黄金?
②怎样确定钯的金属活动性?
【查阅资料】①假黄金通常是黄铜(Cu-Zn合金);
②钯(Pd)呈银白色,有金属光泽,可用作饰品。
【实验药品】钯、铂(Pt)、稀盐酸、硝酸银溶液和氯化钯(PdCl2)溶液
【实验探究】
(1)、鉴别黄金样品的真假取黄金样品于试管中,滴加稀盐酸后,观察到黄金样品表面有气泡产生,说明此样品为 .(选填“真”或“假”)黄金。
(2)、探究钯的金属活动性依据生活经验,同学们猜想钯的活动性可能与银和铂相近,于是他们利用上述药品进行如下实验:
实验步骤
实验现象
实验结论
把钯浸入硝酸银溶液中
钯的活动性比银弱
把铂浸入氯化钯溶液中
无明显现象
钯的活动性比铂.
(3)、转化成沉淀。小组同学将所有液体倒入废液缸中,出现白色沉淀。写出产生该现象的化学方程式 .(写出一个即可);四、解答题
-
26. 2017年5月,某市自来水有股奇怪的味道,经专家多轮综合检测,基本认定引起此次异味的主要物质是邻叔丁基苯酚。将30g邻叔丁基苯酚完全燃烧,生成88gCO2和25.2gH2O(无其他产物)。已知邻叔丁基苯酚的相对分子质量为150,求:(1)、30g邻叔丁基苯酚中含碳元素g,氢元素g。(2)、邻叔丁基苯酚的化学式为。27. 现有铜与另一种金属的混合物粉末,另一种金属可能是镁、铁、锌中的一种,现欲测定其组成。现取该混合物粉末8.0g放入烧杯中,将140.0g、14.0%的稀硫酸分四次加入该烧杯中,充分反应后,测得剩余固体质量数据记录如下:
通过计算(写出计算过程),求:
(1)、该混合物粉末中铜的质量分数 ;(2)、该混合物粉末中另一金属为何种金属(3)、第三次加入硫酸充分反应后,所得溶液中溶质的质量分数是多少?次数
1
2
3
4
加入稀硫酸的质量/g
35.0
35.0
35.0
35.0
剩余固体的质量/g
6.8
5.6
4.4
4.2
28. 做实验时,小迪取了40mL的Ba(OH)2溶液,并随手倒入等量的稀盐酸(均未知浓度)。老师发现后,递给他一瓶未知质量分数的K2CO3溶液,让小科来检测混合溶液的酸碱性。小迪在混合液中慢慢滴入K2CO3溶液,获得相关数据并绘成图象(如图)。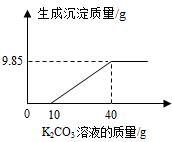 (1)、写出K2CO3 与BaCl2反应的化学方程式;(2)、刚加入K2CO3溶液时,发现没有沉淀生成,却有气泡产生,则原混合溶液呈(填“酸性”、“碱性”或“中性”),其中所含的溶质有(用化学式表示)(3)、计算K2CO3溶液中溶质的质量分数。29. 向含CuCl2和HCl的100g混合溶液中,逐滴加入溶质质量分数为10%NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图,据图回答:
(1)、写出K2CO3 与BaCl2反应的化学方程式;(2)、刚加入K2CO3溶液时,发现没有沉淀生成,却有气泡产生,则原混合溶液呈(填“酸性”、“碱性”或“中性”),其中所含的溶质有(用化学式表示)(3)、计算K2CO3溶液中溶质的质量分数。29. 向含CuCl2和HCl的100g混合溶液中,逐滴加入溶质质量分数为10%NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图,据图回答: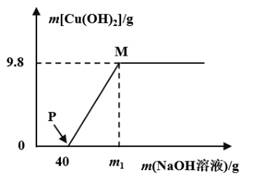 (1)、写出PM段发生的化学方程式。(2)、P点溶液中的溶质是。(3)、原混合物中CuCl2的质量是。(4)、试通过计算确定m1的值是。(5)、M点溶液的溶质质量分数是多少?(结果保留0.1%)30. 三位同学分别用相同质量分数的稀盐酸,测定某石灰石样品中碳酸钙的质量分数(石灰石中的杂质既不与酸反应,也不溶于水)。
(1)、写出PM段发生的化学方程式。(2)、P点溶液中的溶质是。(3)、原混合物中CuCl2的质量是。(4)、试通过计算确定m1的值是。(5)、M点溶液的溶质质量分数是多少?(结果保留0.1%)30. 三位同学分别用相同质量分数的稀盐酸,测定某石灰石样品中碳酸钙的质量分数(石灰石中的杂质既不与酸反应,也不溶于水)。
(1)、小敏的方法可用如下流程表示,测得的碳酸钙的质量分数为;在过滤操作中,需要用到的玻璃仪器有(填序号)。
A.酒精灯、漏斗、玻璃棒 B. 漏斗、玻璃棒、烧杯 C. 酒精灯、试管、玻璃棒
(2)、小华取10g样品,用如图甲实验装置进行实验,反应结束后,测得B装置质量增加了4.6g,根据上述数据,算得碳酸钙的质量分数,发现与事实严重不符,造成这种情况的可能原因是。 (3)、小军用如图乙的实验装置进行实验,将20g稀盐酸加入到1.25g样品中,生成的CO2体积与反应时间的关系如图丙。已知本实验条件下CO2的密度为1.8g/l,求该石灰石样品中CaCO3的质量分数。(4)、求实验所用的稀盐酸溶质质量分数。31. 将质量为44.4克含有少量NaCl的纯碱晶体(Na2CO3·nH2O)样品,平均分成A、B、C三份,进行如图实验(Na2CO3受热不分解)。
(3)、小军用如图乙的实验装置进行实验,将20g稀盐酸加入到1.25g样品中,生成的CO2体积与反应时间的关系如图丙。已知本实验条件下CO2的密度为1.8g/l,求该石灰石样品中CaCO3的质量分数。(4)、求实验所用的稀盐酸溶质质量分数。31. 将质量为44.4克含有少量NaCl的纯碱晶体(Na2CO3·nH2O)样品,平均分成A、B、C三份,进行如图实验(Na2CO3受热不分解)。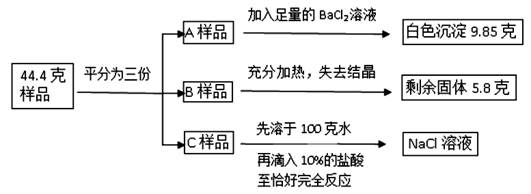 (1)、将A样品与BaCl2溶液反应生成的白色沉淀分离出来的方法是。(2)、A样品中与BaCl2溶液反应的Na2CO3的质量是克。(3)、B样品中含有结晶水的质量是克。(4)、化学式Na2CO3·nH2O中n是(5)、对C样品的操作结束后,所得NaCl溶液的溶质质量分数是多少?(精确到0.01%)
(1)、将A样品与BaCl2溶液反应生成的白色沉淀分离出来的方法是。(2)、A样品中与BaCl2溶液反应的Na2CO3的质量是克。(3)、B样品中含有结晶水的质量是克。(4)、化学式Na2CO3·nH2O中n是(5)、对C样品的操作结束后,所得NaCl溶液的溶质质量分数是多少?(精确到0.01%)