2016-2017学年山东省泰安市东平县九年级上学期期末化学试卷
试卷更新日期:2017-03-31 类型:期末考试
一、选择题
-
1. 日益严峻的能源危机促进了可再生能源的研究.下列属于可再生能源的是( )A、太阳能 B、煤 C、石油 D、天然气2. 欲将含少量盐酸的氯化钙溶液变为中性,在不用指示剂的条件下,应加入的试剂是( )A、石灰石 B、生石灰 C、氢氧化钠 D、熟石灰3. 下列气体能用浓硫酸干燥,而不能用氢氧化钠固体干燥的是( )A、H2 B、O2 C、CO2 D、N24. 某溶液可使酚酞试液变红色,则该溶液会使石蕊试液( )A、变红 B、变紫 C、变蓝 D、不变色5. 下列关于石油的叙述不正确的是( )A、石油属于清洁能源 B、石油是一种混合物 C、可利用石油产品发电 D、将石油分馏可得到多种产品6. 关于空气中的二氧化碳说法正确的是( )A、有剧毒 B、植树造林导致二氧化碳含量升高 C、含量剧增导致温室效应 D、越少越好7. 二氧化碳在生活和生产中具有广泛的应用.如图中能体现二氧化碳用途的是( )A、
 医疗急救
B、
医疗急救
B、 霓红灯
C、
霓红灯
C、 人工降雨
D、
人工降雨
D、 高能燃料
8. Ba(OH)2+H2SO4 , HCl+Ca(OH)2这两个反应的共同点是( )
高能燃料
8. Ba(OH)2+H2SO4 , HCl+Ca(OH)2这两个反应的共同点是( )①都是中和反应 ②都是复分解反应 ③都有气体生成 ④都生成白色沉淀.
A、①② B、①④ C、②④ D、①③9. 下列反应,需要借助酸碱指示剂才能判断反应是否发生的是( )A、Fe和稀H2SO4 B、Cu(OH)2和稀HCl C、稀H2SO4和NaOH溶液 D、Fe与CuSO4溶液10. 如图为某反应的微观示意图,“ ”和“
”和“  ”表示两种不同的原子,下列说法正确的是( )
”表示两种不同的原子,下列说法正确的是( )  A、反应前后原子数目不变 B、反应中有单质生成 C、反应前后分子种类不变 D、参加反应的两种分子个数比为3:111. 下面是某学生的一些实验记录,其中正确的是( )A、用托盘天平称取12.05gNaCl固体 B、用量筒量取5.28mL稀硫酸 C、用pH试纸测得某种稀氢氧化钠溶液的pH为8.8 D、向酒精灯中添加酒精至约占酒精灯容积的 处12. 能源问题是当今世界三大问题之一,下列有关能源的叙述不正确的是( )A、乙醇汽油中添加的乙醇属于可再生能源 B、人类通过化石燃料获得能量的过程是物理变化 C、将煤球制成“蜂窝煤”是为了增大与空气的接触面积,使其燃烧更充分 D、氢气作为一种最理想的燃料,现在还不能被广泛应用13. 下列关于燃烧及事故处理的叙述中正确的是( )A、室内起火,迅速打开所有门窗通风 B、厨房煤气管道漏气,迅速关闭阀门并开窗通风 C、只有含有碳元素的物质才能燃烧 D、可燃物与氧气接触,就能燃烧14. 我国自2015年1月1日起,对地级及以上城市执行空气质量监测新标准,监测数据包括可吸入颗粒(PM10)、细微粒物(PM2.5)、SO2、NO2、O3和CO等6项指标.某同学对SO2、NO2、O3和CO四种物质的认识,不正确的是( )A、O3属于单质 B、SO2、NO2和CO都属于氧化物 C、SO2、NO2中都含有氧分子 D、SO2、NO2、O3和CO中都含有氧元素15. 某种消化药片的有效成分氢氧化镁,能减缓因胃酸过多引起的疼痛.在氢氧化镁与胃酸作用的过程中,胃液pH变化的情况是( )A、
A、反应前后原子数目不变 B、反应中有单质生成 C、反应前后分子种类不变 D、参加反应的两种分子个数比为3:111. 下面是某学生的一些实验记录,其中正确的是( )A、用托盘天平称取12.05gNaCl固体 B、用量筒量取5.28mL稀硫酸 C、用pH试纸测得某种稀氢氧化钠溶液的pH为8.8 D、向酒精灯中添加酒精至约占酒精灯容积的 处12. 能源问题是当今世界三大问题之一,下列有关能源的叙述不正确的是( )A、乙醇汽油中添加的乙醇属于可再生能源 B、人类通过化石燃料获得能量的过程是物理变化 C、将煤球制成“蜂窝煤”是为了增大与空气的接触面积,使其燃烧更充分 D、氢气作为一种最理想的燃料,现在还不能被广泛应用13. 下列关于燃烧及事故处理的叙述中正确的是( )A、室内起火,迅速打开所有门窗通风 B、厨房煤气管道漏气,迅速关闭阀门并开窗通风 C、只有含有碳元素的物质才能燃烧 D、可燃物与氧气接触,就能燃烧14. 我国自2015年1月1日起,对地级及以上城市执行空气质量监测新标准,监测数据包括可吸入颗粒(PM10)、细微粒物(PM2.5)、SO2、NO2、O3和CO等6项指标.某同学对SO2、NO2、O3和CO四种物质的认识,不正确的是( )A、O3属于单质 B、SO2、NO2和CO都属于氧化物 C、SO2、NO2中都含有氧分子 D、SO2、NO2、O3和CO中都含有氧元素15. 某种消化药片的有效成分氢氧化镁,能减缓因胃酸过多引起的疼痛.在氢氧化镁与胃酸作用的过程中,胃液pH变化的情况是( )A、 B、
B、 C、
C、 D、
D、 16. 下列各组离子在pH=l或pH=10的溶液中都能大量共存的是( )A、C u2+、Mg2+、NO3ˉ、SO42ˉ B、Na+、H+、NO3ˉ、SO42ˉ C、K+、Na2+、CO32ˉ、SO42ˉ D、K+、Clˉ、Ba2+、NO3ˉ17. 下列鉴别物质的方法中,切实可行的是( )A、用酚酞溶液鉴别NaCl溶液和盐酸 B、用燃着的木条鉴别CO2和CO C、用石蕊溶液鉴别稀盐酸和稀硫酸 D、用水鉴别NaOH和CaCO3固体18. 北京大学的两位教授发现人体心肺血管中存在微量的硫化氢(H2S),它对调节心血管功能具有重要作用.硫化氢能溶于水,其水溶液显酸性,称为氢硫酸.下列叙述不正确的是( )A、硫化氢由2种元素组成 B、硫化氢中硫元素的化合价为﹣2价 C、氢硫酸能使紫色石蕊试液变蓝 D、氢硫酸能与氢氧化钠溶液发生中和反应19. 某地农业科技工作者在进行“酸雨对农业生产影响及其对策研究”中,得出酸雨的pH是( )
16. 下列各组离子在pH=l或pH=10的溶液中都能大量共存的是( )A、C u2+、Mg2+、NO3ˉ、SO42ˉ B、Na+、H+、NO3ˉ、SO42ˉ C、K+、Na2+、CO32ˉ、SO42ˉ D、K+、Clˉ、Ba2+、NO3ˉ17. 下列鉴别物质的方法中,切实可行的是( )A、用酚酞溶液鉴别NaCl溶液和盐酸 B、用燃着的木条鉴别CO2和CO C、用石蕊溶液鉴别稀盐酸和稀硫酸 D、用水鉴别NaOH和CaCO3固体18. 北京大学的两位教授发现人体心肺血管中存在微量的硫化氢(H2S),它对调节心血管功能具有重要作用.硫化氢能溶于水,其水溶液显酸性,称为氢硫酸.下列叙述不正确的是( )A、硫化氢由2种元素组成 B、硫化氢中硫元素的化合价为﹣2价 C、氢硫酸能使紫色石蕊试液变蓝 D、氢硫酸能与氢氧化钠溶液发生中和反应19. 某地农业科技工作者在进行“酸雨对农业生产影响及其对策研究”中,得出酸雨的pH是( )酸雨的pH
3.58
4.59
4.86
小麦减产(%)
10
5
3
A、酸雨的pH越大,小麦减产幅度越大 B、酸雨的pH越小,小麦减产幅度越小 C、酸雨的酸性越强,小麦减产幅度越小 D、酸雨的酸性越弱,小麦减产幅度越小20. 在一个密闭容器中加入四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表:物质
甲
乙
丙
丁
反应前质量/g
2
2
21
5
反应后质量/g
10
2
9
待测
通过分析,判断下列说法不正确的是( )
A、甲是生成物 B、测得反应后丁的质量为4g C、乙可能是催化剂 D、该反应是分解反应二、填空题
-
21. 目前,我国的能源主要依赖于化石燃料,因此开发利用新能源显得格外重要.(1)、常见的三种化石燃料包括石油、天然气和 . 美国墨西哥湾石油钻井平台爆炸,大量石油泄漏燃烧造成了严重的污染,开发公司采用堵塞油管、喷水的方法灭火.其中喷水灭火的原理是;(2)、利用新能源发电的类型有潮汐能发电、地热能发电、等(请举一例);(3)、海底埋藏着大量的“可燃冰”,其主要成分由甲烷分子和水分子组成.如果开采和贮存方法得到突破,“可燃冰”可以成为未来的新能源.“可燃冰”燃烧的化学方程式为 .22. 已知A、E、F是单质,B、C、D是化合物,它们分别是由碳、氢、氧三种元素中的一种或者几种组成.其中B是相对分子质量最小的氧化物,D物质很不稳定,容易分解生成B和C,它们之间的转化关系如图所示.
 (1)、则A、E的化学式为A , E .(2)、请你写出以下变化的化学方程式:A+F→C;D→B+C .23. 酸碱反应与人们的日常生活和生产有密切的关系.(1)、由于人的胃里有胃酸,因此胃液分泌过多会引起胃病,服用含有氢氧化铝的药物可缓解病痛.其治疗的化学原理为 (用化学方程式表示).(2)、做馒头发酵面团时,会产生乳酸等有机酸,蒸馒头前需加进适量的纯碱或小苏打等碱性物质,它们相互作用产生了 (填化学式)气体,使蒸出的馒头疏松多孔;若加入的碱性物质过多,可向面团或蒸锅中滴加少许含 (填名称)的酸性调味料,否则蒸出的馒头会变涩,颜色发黄.24. X和白色沉淀I、Ⅱ都是含有镁元素的化合物,Z是一种能使地球产生“温室效应”的气体,A是一种碱.它们的有关变化如下图所示(微溶物以沉淀形式出现).
(1)、则A、E的化学式为A , E .(2)、请你写出以下变化的化学方程式:A+F→C;D→B+C .23. 酸碱反应与人们的日常生活和生产有密切的关系.(1)、由于人的胃里有胃酸,因此胃液分泌过多会引起胃病,服用含有氢氧化铝的药物可缓解病痛.其治疗的化学原理为 (用化学方程式表示).(2)、做馒头发酵面团时,会产生乳酸等有机酸,蒸馒头前需加进适量的纯碱或小苏打等碱性物质,它们相互作用产生了 (填化学式)气体,使蒸出的馒头疏松多孔;若加入的碱性物质过多,可向面团或蒸锅中滴加少许含 (填名称)的酸性调味料,否则蒸出的馒头会变涩,颜色发黄.24. X和白色沉淀I、Ⅱ都是含有镁元素的化合物,Z是一种能使地球产生“温室效应”的气体,A是一种碱.它们的有关变化如下图所示(微溶物以沉淀形式出现). (1)、写出下列物质的化学式:A;B;白色沉淀I是;Z是 .(2)、X跟C反应的化学方程式是 .25. 完成下列反应的化学方程式:(1)、盐酸和金属锌反应;(2)、氢氧化钠溶液和氯化铁溶液反应;(3)、用稀盐酸除铁锈 .
(1)、写出下列物质的化学式:A;B;白色沉淀I是;Z是 .(2)、X跟C反应的化学方程式是 .25. 完成下列反应的化学方程式:(1)、盐酸和金属锌反应;(2)、氢氧化钠溶液和氯化铁溶液反应;(3)、用稀盐酸除铁锈 .三、探究题
-
26. 小华同学用如图所示装置进行中和反应实验,反应后为确定硫酸和氢氧化钠是否刚好完全反应,他取出一定量反应后的溶液于一支试管中,向其中滴入几滴无色酚酞试液,振荡,观察到酚酞试液不变色,于是他得出“两种物质已恰好完全中和”的结论.
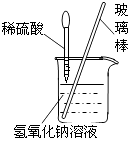 (1)、写出该中和反应的化学方程式 .(2)、小亮认为小华的结论不准确,他认为除了“恰好中和”外还有第二种可能性,这种可能性是 .(3)、请你另外设计一个实验,探究上述烧杯中的溶液是否恰好完全中和.
(1)、写出该中和反应的化学方程式 .(2)、小亮认为小华的结论不准确,他认为除了“恰好中和”外还有第二种可能性,这种可能性是 .(3)、请你另外设计一个实验,探究上述烧杯中的溶液是否恰好完全中和.实验
实验操作
实验现象
实验结论
乙
第二种可能性
27. 三位同学对滴有紫色石蕊试液的蒸馏水通入CO2变红色的原因进行了深入研究.【提出问题】是什么物质使紫色石蕊试液变红色?
(1)、【假设】①是水使紫色石蕊试液变红色;② ;
③ .
(2)、【查阅资料】浓硫酸不能和CO2反应,能吸收大量水分,可用于气体干燥.
【实验】
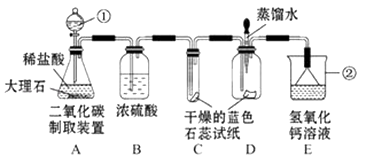
【实验分析】请回答下列问题:
(i)写出编有标号仪器的名称:
① , ② .
(ii)写出装置A中反应的化学方程式: .
(iii)①实验过程中,装置C内蓝色石蕊试纸的颜色始终没有变化,这说明 .
②装置D中胶头滴管中的蒸馏水在二氧化碳气体生成前滴在蓝色石蕊试纸上,未见试纸发生颜色变化,当有二氧化碳通过时发现湿润的蓝色石蕊试纸变红,此现象说明 .
(3)、【结论】原假设成立[选填①,②,③编号].28. 化学反应往往伴随着一些现象发生,但CO2与NaOH溶液的反应没有明显的现象.为了通过一些现象说明CO2与NaOH发生了反应,某班同学分两组作了如下探究实验:(1)、第一组同学把一支收集有CO2的试管倒立在装有饱和NaOH溶液的烧杯中(如图),看到试管内液面上升.这种现象是因为试管内外产生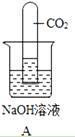 A、温度差 B、重力差 C、压强差 D、浮力差(2)、第二组同学从中得到启发,也设计了如图实验装置进行探究:A现象为 .
A、温度差 B、重力差 C、压强差 D、浮力差(2)、第二组同学从中得到启发,也设计了如图实验装置进行探究:A现象为 . (3)、同学们经过分析讨论,认为第一组的实验中产生液面上升现象的原因可能有两种.一种是因为CO2与溶液中的NaOH反应,消耗了CO2 , 你认为另一种原因是(4)、为了进一步证实CO2与NaOH溶液已经发生了反应,他们设计了如下方案:取上述实验后的溶液,第一组同学滴加稀盐酸,现象为有无色气体产生; 第二组同学滴加 , 现象为 . 方程式 . 他们虽然看到的现象不同,但都可以证实CO2与NaOH溶液已经发生了反应.
(3)、同学们经过分析讨论,认为第一组的实验中产生液面上升现象的原因可能有两种.一种是因为CO2与溶液中的NaOH反应,消耗了CO2 , 你认为另一种原因是(4)、为了进一步证实CO2与NaOH溶液已经发生了反应,他们设计了如下方案:取上述实验后的溶液,第一组同学滴加稀盐酸,现象为有无色气体产生; 第二组同学滴加 , 现象为 . 方程式 . 他们虽然看到的现象不同,但都可以证实CO2与NaOH溶液已经发生了反应.四、本题包括2小题
-
29. 据央视报道,有不法酒类生产企业在白酒中添加酯类物质以增强口感.下表是几种常见的酯.
酯的名称
甲酸甲酯
甲酸乙酯
乙酸甲酯
乙酸乙酯
化学式
C2H4O2
C3H6O2
C3H6O2
X
(1)、甲酸甲酯中碳、氢、氧的原子个数比为;(2)、据表推测X的化学式为;(3)、实验测得由甲酸甲酯和甲酸乙酯组成的混合物中碳元素的质量分数是43.2%,则氧元素的质量分数是多少?(计算结果保留0.1%)30. 取碳酸钠和氯化钠的固体混合物13.6g,与质量为73g的稀盐酸恰好完全反应?产生二氧化碳气体的质量为4.4g,计算:(1)、固体混合物中碳酸钠的质量.(2)、该稀盐酸中溶质的质量分数.(3)、反应所得的溶液中溶质的质量分数(最后结果保留一位小数).