2018-2019学年人教版化学九年级下册第九单元课题3 溶液的浓度 同步训练
试卷更新日期:2018-12-13 类型:同步测试
一、单选题
-
1. 下列说法正确的是( )A、凡是均一、稳定、无色的液体一定是溶液 B、“洗洁精”能够洗去油污是因为洗洁精能够溶解油污 C、饱和溶液可能是浓溶液,也可能是稀溶液 D、10g某物质完全溶解于水中配成100g溶液,所得溶液的质量分数一定是10%2. 对“10%的食盐溶液”含义的理解错误的是( )
A、100g水中溶解了10g食盐 B、100g食盐溶液中溶解了10g食盐 C、将10g食盐溶于90g水中形成的溶液 D、该溶液中溶质与溶液的质量比为1∶103. 实验室将10g质量分数为98%的浓硫酸稀释成10%的稀硫酸,稀释后得到稀硫酸溶液,这个过程中需加水( )
A、 49g B、98g C、88g D、88.2g4. 向100g溶液质量分数为10%的氯化钠溶液中加入10g硝酸钾,并完全溶解,该溶液中氯化钠的溶质质量分数会( )
A、变大 B、变小 C、不变 D、无法确定5. 现有100克溶质质量分数为10%的食盐溶液,若使溶液的溶质质量分数增加一倍,下列操作中正确的是 ( )
A、加入食盐10克 B、加入水50克 C、蒸发掉溶剂的一半 D、加入100克溶质质量分数为30%的食盐溶液6. t1℃时,取a、b两种固体物质各25g于两只烧杯中,分别加入100g水,充分溶解后,两种固体均有剩余。升温到t2℃时,a完全溶解,b固体增多。a、b两种物质的溶解度曲线如图所示。以下判断正确的是( )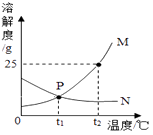 A、图中曲线M表示b物质的溶解度曲线 B、t1℃时,两只烧杯中剩余物质的质量不相等 C、t2℃时,两只烧杯中的溶液都是饱和溶液 D、t2℃时,两只烧杯中溶液的溶质质量分数相同7. 下图是甲、乙两种固体物质的溶解度曲线。下列说法中错误的是( )
A、图中曲线M表示b物质的溶解度曲线 B、t1℃时,两只烧杯中剩余物质的质量不相等 C、t2℃时,两只烧杯中的溶液都是饱和溶液 D、t2℃时,两只烧杯中溶液的溶质质量分数相同7. 下图是甲、乙两种固体物质的溶解度曲线。下列说法中错误的是( )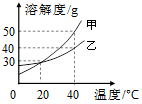 A、20℃时,甲、乙饱和溶液中溶质质量分数相等 B、40℃时,甲的溶解度大于乙的溶解度 C、40℃时,乙的饱和溶液中溶质的质量分数为40% D、将40℃甲的饱和溶液降温到20℃,会有晶体析出8. 小芳在配制一定溶质质量分数的氯化钠溶液时,没有按照正确的称量氯化钠、量取水的操作规程进行操作(图示为小芳操作时的读数,其它操作都正确)。小芳实际配制的氯化钠溶液的溶质质量分数(水的密度为1g/cm3)约为( )
A、20℃时,甲、乙饱和溶液中溶质质量分数相等 B、40℃时,甲的溶解度大于乙的溶解度 C、40℃时,乙的饱和溶液中溶质的质量分数为40% D、将40℃甲的饱和溶液降温到20℃,会有晶体析出8. 小芳在配制一定溶质质量分数的氯化钠溶液时,没有按照正确的称量氯化钠、量取水的操作规程进行操作(图示为小芳操作时的读数,其它操作都正确)。小芳实际配制的氯化钠溶液的溶质质量分数(水的密度为1g/cm3)约为( ) A、12.4% B、17.2% C、16.9% D、12.5%9. 实验室配制100g溶质质量分数为8%的氯化钠溶液,下列说法中错误的是( )A、若在量取水时俯视凹液面的最低处,则配制溶液的质量分数小于8% B、溶解过程中玻璃棒搅拌的作用是加快氯化钠的溶解速率 C、实验的步骤为计算、称量、量取、溶解、装瓶贴标签 D、量取水时,用规格为100mL的量筒10. 下表是NaCl和Na2CO3在不同温度下的溶解度,下列说法中错误的是( )
A、12.4% B、17.2% C、16.9% D、12.5%9. 实验室配制100g溶质质量分数为8%的氯化钠溶液,下列说法中错误的是( )A、若在量取水时俯视凹液面的最低处,则配制溶液的质量分数小于8% B、溶解过程中玻璃棒搅拌的作用是加快氯化钠的溶解速率 C、实验的步骤为计算、称量、量取、溶解、装瓶贴标签 D、量取水时,用规格为100mL的量筒10. 下表是NaCl和Na2CO3在不同温度下的溶解度,下列说法中错误的是( )温度/℃
0
10
20
30
40
溶解度/g
NaCl
35.0
35.5
36.0
36.5
37.0
Na2CO3
6.0
10.0
18.0
36.5
50.0
A、两种物质溶解度相等的温度在30℃ B、生活在盐碱湖附近的人们习惯“夏天晒盐、冬天捞碱” C、40℃时,5gNaCl中加10g水可得溶质质量分数为26.3%的溶液 D、40℃时,9g Na2CO3中加20g水,充分溶解后再降温到10℃,析出固体的质量为7g11. 现有某锌铝合金(Zn-Al)样品8.3g,将其放入200g稀硫酸中,经测定恰好完全反应,蒸发结晶,称量所得固体质量为27.5g,则所用稀硫酸的溶质质量分数为( )。A、6.26% B、9.8% C、19.6% D、22.6%12. 向盛有5g氢氧化钠固体的烧杯中加入45g水,完全溶解后,所得溶液溶质的质量分数是( )A、20% B、11.1% C、10% D、5%二、填空题
-
13. 10%的CaCl2溶液可用作路面保湿剂。欲配制100kg该路面保湿剂,需要水的质量是kg。14. 食盐是人类生存的必需品,获取食盐的途径有多种。
①开采岩盐,地下盐层含氯化钠等物质,灼烧氯化钠,火焰呈色。配置某氯化钠溶液需85mL水,应选用mL量筒量取(选填编号)。
a.10 b.20 c.100
②熬制井盐。《天工开物》记载:抽取深井中的盐水,用井中产生的天然气作为燃料熬制井盐。CH4燃烧的化学方程式是。氯化钠与硝酸钠的溶解度曲线如下,20℃时溶解度较小的物质是。

③海水晒盐。某地海水中主要物质的含量见上表。
该海水中氯化钠的质量分数为。20℃时的100g该海水,当水的蒸发量大于g时,开始析出氯化钠。除去氯化钠中的硫酸钠应选用的试剂是。
15. 如图是甲、乙两种固体的溶解度曲线.将t3℃时相同质量的甲、乙两种物质的饱和溶液降温到t1℃,只有甲的溶液中有固体析出.则乙的溶解度曲线为(填“X”或“Y”);甲和乙的溶解度相等时的温度为;t3℃时,将30g 甲的饱和溶液稀释为质量分数为10%的溶液,需加水的质量为g. 16. 如图是甲、乙、丙三种物质的溶解度曲线.回答下列问题:
16. 如图是甲、乙、丙三种物质的溶解度曲线.回答下列问题: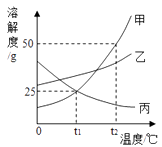
①t1℃时,甲的溶解度为;
②现有甲、乙、丙三种物质的浓溶液,适用海水晒盐原理进行结晶提纯的是;
③t3℃时,甲的饱和溶液中含有少量的丙,现要提纯甲可采用的方法是;
④下列说法正确的是 .
A.t2℃时把50g甲放入50g水中所得到甲的饱和溶液中溶质与溶液的质量比为1:2
B.t2℃时,等质量的甲、乙、丙分别制成饱和溶液,需水的质量最多的是甲
C.t1℃时,甲、乙、丙三种溶液分别升温,其浓度都不可能发生变化
D.t1℃时,向100g20%甲的饱和溶液中加100g水,充分搅拌,溶液的浓度为10%
E.t2℃时,将甲、乙、丙三种物质的饱和溶液降温至t1℃,这三种溶液的溶质质量分数的大小关系是乙>甲=丙
F.t1℃时,甲、乙、丙三种溶液的浓度可能相等.
三、计算题
-
17. 实验室有一瓶未开封的浓盐酸,部分标签如图所示。
 (1)、求这瓶浓盐酸的质量。
(1)、求这瓶浓盐酸的质量。
(2)、若用这瓶浓盐酸来配制200 g溶质质量分数为10%的稀盐酸,求需量取浓盐酸的体积和水的体积。