浙江省绍兴市2018-2019学年八年级上学期科学教学质量检测(一)
试卷更新日期:2018-12-08 类型:月考试卷
一、选择题
-
1. 下列操作均在室温下进行,且不考虑水分的蒸发。则溶液中溶质的溶解度和溶质质量分数都一定发生变化的是( )A、将一定量硝酸钾不饱和溶液升温 10℃ B、将一定量饱和石灰水升温 10℃ C、取一定量蔗糖不饱和溶液向其中加入少量蔗糖 D、取一定量氯化钠饱和溶液向其中加入少量水2. 在粗盐提纯的实验中,下列操作不规范的是( )A、称量
 B、溶解
B、溶解  C、过滤
C、过滤  D、蒸发
D、蒸发  3. 20℃时,四个实验小组分别取不同质量的氯化钠,逐渐加入到各盛有 50g 水的烧杯中,不断搅拌直到不再溶解为止,然后分别称量剩余氯化钠的质量。记录数据如下表:
3. 20℃时,四个实验小组分别取不同质量的氯化钠,逐渐加入到各盛有 50g 水的烧杯中,不断搅拌直到不再溶解为止,然后分别称量剩余氯化钠的质量。记录数据如下表:实验小组
第一组
第二组
第三组
第四组
水的质量/g
50
50
50
50
所取氯化钠的质量/g
15
20
25
30
剩余氯化钠的质量/g
0
2
7
12
下列说法错误的是( )
A、20℃时,50g 氯化钠饱和溶液中含有 18g 氯化钠 B、用蒸发的方法可以使不饱和溶液变成饱和溶液 C、第二组所得溶液的溶质与溶剂的质量比为 9∶25 D、相同温度下,氯化钠在水里的溶解度与水的质量无关4. 从试剂瓶中取用氯化钠固体、硝酸银溶液,需要用到的器材是( ) A、甲—①,乙—① B、甲—①,乙—② C、甲—②,乙—② D、甲—②,乙—①5. 一圆柱体先后放入密度为ρ1和ρ2的2种液体中,均处于漂浮状态,如图所示。圆柱体在两液体中所受浮力依次是F1和F2 , 则( )
A、甲—①,乙—① B、甲—①,乙—② C、甲—②,乙—② D、甲—②,乙—①5. 一圆柱体先后放入密度为ρ1和ρ2的2种液体中,均处于漂浮状态,如图所示。圆柱体在两液体中所受浮力依次是F1和F2 , 则( ) A、ρ1>ρ2 F1>F2 B、ρ1<ρ2 F1<F2 C、ρ1<ρ2 F1=F2 D、ρ1>ρ2 F1=F26. 硝酸钾的溶解度随温度升高而增大。如图是有关硝酸钾溶液的实验操作及变化情况。下列说法正确的是( )
A、ρ1>ρ2 F1>F2 B、ρ1<ρ2 F1<F2 C、ρ1<ρ2 F1=F2 D、ρ1>ρ2 F1=F26. 硝酸钾的溶解度随温度升高而增大。如图是有关硝酸钾溶液的实验操作及变化情况。下列说法正确的是( )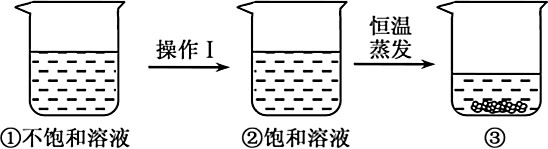 A、操作Ⅰ一定是降温 B、操作Ⅰ一定是加溶质 C、①与③的溶质质量一定相等 D、②与③的溶质质量分数一定相等7. 2018 年 5 月,台州南部湾区引水工程开工,以级解台州南部地区的用水紧张状况。该工程通过管道,将台州北部水资源向南部输送,该工程改变的水循环环节是( )A、 降水 B、地表径流 C、海水蒸发 D、水汽输送8. 下图为自来水生产过程示意图。下列说法正确的是( )
A、操作Ⅰ一定是降温 B、操作Ⅰ一定是加溶质 C、①与③的溶质质量一定相等 D、②与③的溶质质量分数一定相等7. 2018 年 5 月,台州南部湾区引水工程开工,以级解台州南部地区的用水紧张状况。该工程通过管道,将台州北部水资源向南部输送,该工程改变的水循环环节是( )A、 降水 B、地表径流 C、海水蒸发 D、水汽输送8. 下图为自来水生产过程示意图。下列说法正确的是( ) A、清水池中的水是溶液 B、过滤池中主要发生化学变化 C、消毒用的液氯是化合物 D、供水系统流出的水是纯净物9. 下列各项中,前者一定大于后者的是( )A、20℃时硝酸钾的溶解度、80℃时硝酸钾的溶解度 B、30℃时食盐不饱和溶液的质量分数、20℃时食盐饱和溶液的质量分数 C、20℃时熟石灰的溶解度、30℃时熟石灰的溶解度 D、20℃时食盐饱和溶液的质量分数、50℃时食盐不饱和溶液的质量分数10. 如图是 a、b、c 三种物质的溶解度曲线。由图示判断下列说法中不正确的是( )
A、清水池中的水是溶液 B、过滤池中主要发生化学变化 C、消毒用的液氯是化合物 D、供水系统流出的水是纯净物9. 下列各项中,前者一定大于后者的是( )A、20℃时硝酸钾的溶解度、80℃时硝酸钾的溶解度 B、30℃时食盐不饱和溶液的质量分数、20℃时食盐饱和溶液的质量分数 C、20℃时熟石灰的溶解度、30℃时熟石灰的溶解度 D、20℃时食盐饱和溶液的质量分数、50℃时食盐不饱和溶液的质量分数10. 如图是 a、b、c 三种物质的溶解度曲线。由图示判断下列说法中不正确的是( ) A、在 t1℃时,a 的溶解度等于 c 的溶解度 B、c 的溶解度随着温度升高而减少 C、a 的饱和溶液从 t2℃降温至 t1℃时变为不饱和溶液 D、当 a 中含有少量 b 时,可以用降温结晶的方法提纯 a11. 将重为20N的实心金属块挂在弹簧测力计下,金属体积的1/4浸入水中并静止时,弹簧测力计的示数为18N,当金属块全部浸入水中并与杯底接触时,弹簧测力计的示数可能变为( )A、18N B、16N C、14N D、10N12. 下列分离或提纯物质的方法,所依据的原理正确的是( )
A、在 t1℃时,a 的溶解度等于 c 的溶解度 B、c 的溶解度随着温度升高而减少 C、a 的饱和溶液从 t2℃降温至 t1℃时变为不饱和溶液 D、当 a 中含有少量 b 时,可以用降温结晶的方法提纯 a11. 将重为20N的实心金属块挂在弹簧测力计下,金属体积的1/4浸入水中并静止时,弹簧测力计的示数为18N,当金属块全部浸入水中并与杯底接触时,弹簧测力计的示数可能变为( )A、18N B、16N C、14N D、10N12. 下列分离或提纯物质的方法,所依据的原理正确的是( )选项
混合物的分离或提纯
分离物质的原理
A
除去粗盐中的泥沙
氯化钠和泥沙的溶解性不同
B
将石油分馏得到石油产品
石油中各成分的密度不同
C
分离硝酸钾和氯化钠组成的混合物
硝酸钾和氯化钠分解温度不同
D
分离液态空气制取氧气
利用氮气和氧气的熔点不同
A、A B、B C、C D、D13. 配制一定质量分数的食盐溶液时,会引起食盐质量分数偏小的操作是( )A、称量食盐时,天平指针向左倾斜 B、实验所用的固体食盐已在空气中久置 C、用量筒取水时,俯视读数 D、取配制好的食盐溶液时,少量溶液洒在瓶外14. 如图是 a、b、c 三种物质的溶解度曲线。把 t1℃时三种物质的饱和溶液温度升高到 t2℃,则三种溶液的溶质质量分数大小关系是( ) A、a >b >c B、c >b >a C、b >a =c D、b >a >c15. 如图是表示 M、N 两种固体物质的溶解度曲线,有关图示信息的描述正确的是( )
A、a >b >c B、c >b >a C、b >a =c D、b >a >c15. 如图是表示 M、N 两种固体物质的溶解度曲线,有关图示信息的描述正确的是( ) A、30℃时 M 的溶解度小于 N 的溶解度 B、M、N 都不是易溶物质 C、阴影处(不包含曲线上的点)N 为不饱和溶液,M 为饱和溶液 D、P 点表示 20℃时 M、N 的溶解度相等16. 下列有关溶液的说法,不正确的是( )A、蔗糖溶液是均一的、稳定的混合物 B、硝酸钾在 20℃时溶解度是 31.6g,则100g 硝酸钾溶液中含有硝酸钾 31.6g C、在鱼池中设立水泵,把水喷向空中可以增加水中氧气的溶解量 D、冷却或蒸发溶剂都能使接近饱和的硝酸钾溶液达到饱和17. 如图是 A、B、C 三种物质的溶解度随温度的变化趋势。则下列说法正确的是( )
A、30℃时 M 的溶解度小于 N 的溶解度 B、M、N 都不是易溶物质 C、阴影处(不包含曲线上的点)N 为不饱和溶液,M 为饱和溶液 D、P 点表示 20℃时 M、N 的溶解度相等16. 下列有关溶液的说法,不正确的是( )A、蔗糖溶液是均一的、稳定的混合物 B、硝酸钾在 20℃时溶解度是 31.6g,则100g 硝酸钾溶液中含有硝酸钾 31.6g C、在鱼池中设立水泵,把水喷向空中可以增加水中氧气的溶解量 D、冷却或蒸发溶剂都能使接近饱和的硝酸钾溶液达到饱和17. 如图是 A、B、C 三种物质的溶解度随温度的变化趋势。则下列说法正确的是( ) A、t1℃时 A,B,C 三种物质的溶解度由大到小的顺序是 ACB B、t1℃时 30gA 物质加入到 50g 水中不断搅拌,形成的溶液质量是 80g C、A,B 两种物质的混合溶液可通过蒸发结晶的方式提纯 A D、将 t1℃时 A,B,C 三种物质饱和溶液的温度升高到 t2℃时,三种溶液的溶质质量分数由大小关系是 B>C>A18. 有一体积为 0.1m3 的冰块漂浮在水面上(ρ 冰=0.9×103kg/m3 , ρ 水=1.0×103kg/m3 , g=10N/kg),则该冰块( )A、总重量是 1×103N B、浸入液面以下的体积是 0.08m3 C、水上部分体积占总体积的 1/9 D、受到的浮力是 900N19. 将一个密度为 0.9×103kg/m3 的实心小球,先后浸没在水和酒精中,松开手后,小球静止时,排开水和酒精的体积分别为 V1 和 V2 , 小球在水和酒精中所受的浮力分別为 F1 和 F2。以下判断正确的是( )A、V1∶V2=1∶1 F1∶F2=5∶4 B、V1∶V2=4∶5 F1∶F2=1∶1 C、V1∶V2=9∶10 F1∶F2=9∶8 D、V1∶V2=8∶9 F1∶F2=10∶920. 如图所示,烧杯的底面积是 200cm2 , 里面装有一定量水(图甲),用弹簧测力计吊着未知物体,先将物体浸没在水中(图乙),水位升高到 B 处,示数是 18N;再将物体缓慢提出,使水位下降到 AB 的中点 C 处,示数是 23N(不计物体带出的水)。g 取 10N/kg,下列判断中正确的是( )
A、t1℃时 A,B,C 三种物质的溶解度由大到小的顺序是 ACB B、t1℃时 30gA 物质加入到 50g 水中不断搅拌,形成的溶液质量是 80g C、A,B 两种物质的混合溶液可通过蒸发结晶的方式提纯 A D、将 t1℃时 A,B,C 三种物质饱和溶液的温度升高到 t2℃时,三种溶液的溶质质量分数由大小关系是 B>C>A18. 有一体积为 0.1m3 的冰块漂浮在水面上(ρ 冰=0.9×103kg/m3 , ρ 水=1.0×103kg/m3 , g=10N/kg),则该冰块( )A、总重量是 1×103N B、浸入液面以下的体积是 0.08m3 C、水上部分体积占总体积的 1/9 D、受到的浮力是 900N19. 将一个密度为 0.9×103kg/m3 的实心小球,先后浸没在水和酒精中,松开手后,小球静止时,排开水和酒精的体积分别为 V1 和 V2 , 小球在水和酒精中所受的浮力分別为 F1 和 F2。以下判断正确的是( )A、V1∶V2=1∶1 F1∶F2=5∶4 B、V1∶V2=4∶5 F1∶F2=1∶1 C、V1∶V2=9∶10 F1∶F2=9∶8 D、V1∶V2=8∶9 F1∶F2=10∶920. 如图所示,烧杯的底面积是 200cm2 , 里面装有一定量水(图甲),用弹簧测力计吊着未知物体,先将物体浸没在水中(图乙),水位升高到 B 处,示数是 18N;再将物体缓慢提出,使水位下降到 AB 的中点 C 处,示数是 23N(不计物体带出的水)。g 取 10N/kg,下列判断中正确的是( )
①物体的质量是 2.8kg;②物体的体积是 1×10-3m3;
③物体浸没时受到的浮力是 15N;④从乙到丙,水
对烧杯底面的压强减小了 260Pa。
A、只有①、②、④正确 B、只有①、②、③正确 C、只有①、②正确 D、只有③、④正确二、填空题
-
21. 在生活中我们知道这样的事实:①食盐易溶于水,而难溶于植物油;②硝酸钾易溶于水,而碳酸钙难溶于水;③蔗糖在热水中溶解的质量比在等质量的冷水中溶解的质量多。上述事实①②③分别说明,固体物质的溶解度主要与、、三个因素有关。22. 氯化钾在不同温度下制成饱和溶液的实验数据如下:
①0℃时 50 克水中溶有 13.8 克氯化钾;
②20℃时 200 克饱和溶液,加热蒸发掉 20 克水后,再冷却到原温度有 6.8 克氯化钾析出;
③40℃时饱和溶液的溶液和溶质的质量比为 7∶2。
氯化钾在 20℃时的溶解度为 , 在 40℃时的溶解度为;
23. 下表是不同温度时硝酸钾的溶解度。温度(℃)
10
20
30
40
50
60
70
80
90
溶解度(克)
21
32
46
64
86
110
138
169
202
50℃时,将 10.5 克硝酸钾与 50 克水混合配成 60.5 克不饱和溶液。若将其变为饱和溶液,可采用哪些方法?请选用一种方法计算说明。
24. 在实验室可用如图所示装置制取蒸馏水。请据图回答下列问题: (1)、写出仪器的名称:a.、b.。(2)、得到的蒸馏水在中。(3)、仔细观察 b 仪器,它起到冷凝的作用。冷水进入到 b 仪器的方向如图所示,如果改为从上端流入,下端流出行不行?(填“行”或“不行”)。其原因是:。(4)、水在圆底烧瓶中由液态变为气态,在中由气态变为液态。(5)、在 a 中加入碎瓷片的目的是。(6)、先收集到的2-3mL蒸馏水要弃去的原因是什么?。25. 现有 60℃的饱和氯化钠溶液,与该溶液有关的量:①水的质量;②溶液中溶质氯化钠的质量;③氯化钠的质量分数;④60℃时氯化钠的溶解度:⑤溶液的质量。用序号填空:(1)、将该饱和溶液稀释,不变的量有:;(2)、将该饱和溶液降温至 20℃,一定变化的量有。26. 爱好科技的小刚自己制作了一条小木船,船上带有金属船锚,船舷上表明了三种情况的排水量。
(1)、写出仪器的名称:a.、b.。(2)、得到的蒸馏水在中。(3)、仔细观察 b 仪器,它起到冷凝的作用。冷水进入到 b 仪器的方向如图所示,如果改为从上端流入,下端流出行不行?(填“行”或“不行”)。其原因是:。(4)、水在圆底烧瓶中由液态变为气态,在中由气态变为液态。(5)、在 a 中加入碎瓷片的目的是。(6)、先收集到的2-3mL蒸馏水要弃去的原因是什么?。25. 现有 60℃的饱和氯化钠溶液,与该溶液有关的量:①水的质量;②溶液中溶质氯化钠的质量;③氯化钠的质量分数;④60℃时氯化钠的溶解度:⑤溶液的质量。用序号填空:(1)、将该饱和溶液稀释,不变的量有:;(2)、将该饱和溶液降温至 20℃,一定变化的量有。26. 爱好科技的小刚自己制作了一条小木船,船上带有金属船锚,船舷上表明了三种情况的排水量。⑴将锚放在船舱里,当船静止在水槽中时观察船舷对应的排水量为 m1;
⑵用细线拴住船锚,悬挂在船下方的水中且完全浸没,观察船舷对应的排水量为 m2 , 此时水槽中的水面将;(选填“升高”、“降低”或“不变”)
⑶把细线放得更长些,直至线松了,锚沉在盆底,记下此时船舷对应的排水量为 m3 , 于是利用这些排水量测出了船锚的密度。则锚的密度为。
27. 根据图 A、B、C 三种固体的溶解度曲线回答: (1)、在某一温度时,A、B 两饱和溶液的溶质质量分数相等,此时为℃。(2)、在 t1℃~t2℃范围内,A、B、C 三种物质的溶解度由大到小的顺序为。(3)、要使 C 的饱和溶液变为不饱和溶液,可采用的一种方法是。(4)、要从含有少量 A 的 B 溶液中得到较多的 B 晶体,通常采用的方法是。(5)、t3℃时,将 30gA 加入到装有 50g 水的烧杯中,充分搅拌,所得溶液的溶质质量分数为(结果精确至 0.1%)。(6)、在室温时将 A 物质加入到盛水的烧杯中,充分搅拌后发现仍有少量 A 未溶解,但放置一段时间后,发现 A 完全溶解了,可能的原因是。28. 空心铝球的质量是 270g,悬浮在水中,空心铝球的体积是cm3。(ρ铝2.7×103kg/ m3)
(1)、在某一温度时,A、B 两饱和溶液的溶质质量分数相等,此时为℃。(2)、在 t1℃~t2℃范围内,A、B、C 三种物质的溶解度由大到小的顺序为。(3)、要使 C 的饱和溶液变为不饱和溶液,可采用的一种方法是。(4)、要从含有少量 A 的 B 溶液中得到较多的 B 晶体,通常采用的方法是。(5)、t3℃时,将 30gA 加入到装有 50g 水的烧杯中,充分搅拌,所得溶液的溶质质量分数为(结果精确至 0.1%)。(6)、在室温时将 A 物质加入到盛水的烧杯中,充分搅拌后发现仍有少量 A 未溶解,但放置一段时间后,发现 A 完全溶解了,可能的原因是。28. 空心铝球的质量是 270g,悬浮在水中,空心铝球的体积是cm3。(ρ铝2.7×103kg/ m3)三、实验探究题
-
29. 在探究“影响浮力大小的因素”这一问题时,请你根据下图所示实验操作,从中选出一些图,针对某一个因素进行研究,并通过分析弹簧测力计的示数,说明你的探究结果。
 (1)、探究的因素是: , 选用的图是:(填图中的序号)。(2)、小明想探究“物体受到的浮力与其形状是否有关”,他找来薄铁片、烧杯和水进行实验,实验步骤如下:
(1)、探究的因素是: , 选用的图是:(填图中的序号)。(2)、小明想探究“物体受到的浮力与其形状是否有关”,他找来薄铁片、烧杯和水进行实验,实验步骤如下:步骤一:将铁片放入盛水的烧杯中,铁片下沉至杯底;
步骤二:将铁片弯成“碗状”再放入水中,它漂浮在水面上。
①通过分析可知,第一次铁片受到的浮力第二次铁片受到的浮力(选填“大于”、“等于”或“小于”);
②小明得出:物体受到的浮力与其形状有关,小明得出错误结论的原因是:他只关注了铁片的改变,忽视了对浮力大小的影响。
30. 小红和小华讨论盛有液体的容器在放入物体前、后容器底部所受液体压强的增加量Δp与哪些因素有关时,有了两种不同的猜想,并分别进行了实验。①小红猜想:Δp液与放入的物体所受重力 G 有关,于是选择所受重力不同、体积相同的三个物体 A,B,C,先后放入盛有某种液体的同一容器中,并测得 Δp 液。实验示意图及相应数据见表一。分析比较表一中 Δp 液和相关条件,可得:Δp 液与 G(选填“有关”或“无关”)。

②小华猜想:Δp 液与放入的物体所受浮力 F 浮有关,于是将物体 D 挂在测力计下,将其
逐步浸入液体中,读出相应的测力计示数 F,经计算得出 F 浮 , 并测得 Δp 液 , 实验示意
图及相应数据见表二。

根据表二的实验示意图和相关数据,验证Δp 液与F 浮相关的猜想(选填“可以”或“不可以”),依据是:同一物体浸入盛有某种液体的同一容器中,。请填写实验序号 9 中的相关数据:F 浮为牛、Δp液为帕。
31. 20℃时,在盛有 50g 水的烧杯中加入 15g 固体 X(不含杂质),充分溶解后,逐渐升温,并测定不同温度时析出固体 X 的质量。测定结果记录如下表:
溶液的温度/℃
20
35
50
65
75
析出固体 X 的质量/g
10.4
8.0
5.0
0
0
若不考虑水蒸发对实验的影响,请回答下列问题。
①35℃时,该溶液的质量是g;
②65℃时,该溶液是(选填编号);
Ⅰ.饱和溶液 Ⅱ.不饱和溶液 Ⅲ.无法判断
③根据下表溶解度与溶解性的关系,可知 X 属于物质;
溶解性
易溶
可溶
微溶
难溶(或不溶)
溶解度(20℃)
>10
1-10
0.01-1
<0.01
④50℃时,使烧杯中析出的 5g 固体 X 全部溶解,至少加入g 水;
⑤20℃时,用固体粉末 X 和水配制 100g 溶质质量分数为 5%的 X 溶液,必须用到的仪器
有:电子天平、烧杯、。
四、分析计算题
-
32. 溶液与人类的生活息息相关,溶液的配制是日常生活和化学实验中的常见操作。下表是硫酸溶液和氨水的密度与其溶质的质量分数对照表(20℃)。
溶液中溶质的质量分数/%
4
12
16
24
28
硫酸溶液的密度/g/mL
1.02
1.08
1.11
1.17
1.20
氨水的密度/g/mL
0.98
0.95
0.94
0.91
0.90
请仔细分析后回答下列问题:
(1)、20℃时,随着溶液中溶质的质量分数逐渐增大,硫酸溶液的密度逐渐(填增大、减小或不变);氨水的密度逐渐(填增大、减小或不变)(2)、取 12%的硫酸溶液 100%配制成 6%的溶液,向 100g12%的硫酸溶液中加水的质量应100g(填大于、小于或等于)。(3)、向 100g24%的氨水中加入 100g 水,摇匀,溶液体积是mL。(保留到 0.1)33. “蛟龙号”是我国首台自主设计、自主集成研制、世界上下潜最深的作业型深海载人潜水器。“蛟龙号”体积约为 30 米 3 , 空载时质量约为 22 吨,最大荷载 240 千克。 (1)、“蛟龙号”空载漂浮在水面时受到的浮力为多大?(2)、若“蛟龙号”某次满载时下沉是采用注水方式实现的,则至少注入多少立方米的水?(海水密度取 1.0×103 千克/米 3 , g 取 10 牛/千克)34. 实验室有一瓶未开封的浓盐酸,部分标签如图所示。
(1)、“蛟龙号”空载漂浮在水面时受到的浮力为多大?(2)、若“蛟龙号”某次满载时下沉是采用注水方式实现的,则至少注入多少立方米的水?(海水密度取 1.0×103 千克/米 3 , g 取 10 牛/千克)34. 实验室有一瓶未开封的浓盐酸,部分标签如图所示。 (1)、这瓶浓盐酸溶液的质量为多少 g?(2)、若用这瓶浓盐酸来配制 200g 溶质质量分数为 10%的稀盐酸,需量取浓盐酸的体积是多少 mL?水的体积是多少 mL?
(1)、这瓶浓盐酸溶液的质量为多少 g?(2)、若用这瓶浓盐酸来配制 200g 溶质质量分数为 10%的稀盐酸,需量取浓盐酸的体积是多少 mL?水的体积是多少 mL?