2017年科学中考复习专题:物质的分类与分离
试卷更新日期:2017-03-24 类型:二轮复习
一、单选题
-
1. 据报道,日本科学家确认世界上存在一种与C60结构非常相似的具有空心类似于足球结构的分子—N60 , 它在高温或机械撞击后,其中积蓄的巨大能量会在瞬间释放出来。N60的发现,开辟了世界能源的新领域,它有可能成为一种最好的火箭燃料。 N60属于( )
A、化合物 B、混合物 C、单质 D、元素2.如图图示表示的是纯净物、单质、化合物、含氧化合物、氧化物之间的包含与不包含关系,若整个大圆圈代表纯净物,则在下列选项中,正确指出①、②、③、④所属物质类别的是( )
 A、①单质、③氧化物 B、②化合物、④氧化物 C、①含氧化合物、③单质 D、①单质、④化合物3. 下列关于化肥的说法正确的是( )A、区分各种化肥一般先观察外观、溶解性,再观察化学反应中的现象 B、CO(NH2)2(尿素)、K2CO3、和Ca(H2PO4)2均可做氮肥 C、在K2SO4中加入熟石灰研磨能闻到刺激性气味 D、KOH,KCl、KNO3都可以做钾肥4. 逻辑推理是化学学习常用的思维方法,下列推理正确的是( )A、水能灭火,所以电脑一旦失火应立即用水浇灭 B、原子在化学变化中不能再分,则分子在化学变化中也不能再分 C、点燃H2与O2混合气体可能爆炸,则点燃煤气(CO)与O2的混合气体也可能爆炸 D、氧化物都含有氧元素,所以含有氧元素的化合物都是氧化物5. 除去下列物质中的少量杂质,所用试剂和方法正确的是( )
A、①单质、③氧化物 B、②化合物、④氧化物 C、①含氧化合物、③单质 D、①单质、④化合物3. 下列关于化肥的说法正确的是( )A、区分各种化肥一般先观察外观、溶解性,再观察化学反应中的现象 B、CO(NH2)2(尿素)、K2CO3、和Ca(H2PO4)2均可做氮肥 C、在K2SO4中加入熟石灰研磨能闻到刺激性气味 D、KOH,KCl、KNO3都可以做钾肥4. 逻辑推理是化学学习常用的思维方法,下列推理正确的是( )A、水能灭火,所以电脑一旦失火应立即用水浇灭 B、原子在化学变化中不能再分,则分子在化学变化中也不能再分 C、点燃H2与O2混合气体可能爆炸,则点燃煤气(CO)与O2的混合气体也可能爆炸 D、氧化物都含有氧元素,所以含有氧元素的化合物都是氧化物5. 除去下列物质中的少量杂质,所用试剂和方法正确的是( )选项
物质
杂质
试剂和方法
A
NaNO3
Na2CO3
滴入适量稀盐酸至不再产生气泡
B
KCl
K2SO4
滴入适量Ba(NO3)2溶液、过滤
C
CO
CO2
通过灼热的氧化铜粉末
D
H2
HCl
先通过NaOH溶液,再通过浓硫酸
A、A B、B C、C D、D6. 化学就在我们身边。下表是生活中常见的两种清洁剂及其有效成分,且NaClO+2HCl=NaCl+Cl2↑+H2O,下列说法正确的是( )清洁剂名称
洁厕灵
84消毒液
有效成分
HCl
NaClO
A、“洁厕灵”与“84消毒液”可以混合使用 B、“洁厕灵”可用于清洁金属表面 C、“洁厕灵”可用于清洁大理石地面 D、“84消毒液”中NaClO属于盐7. 下列说法不正确的是( )A、配制5%的硝酸钾溶液的一般步骤依次是计算、称量和溶解 B、氢氧化钠溶液要密封保存,因为其会与空气中的二氧化碳反应 C、消除路面上的积雪可以撒些粗盐,这样可以使雪较快的溶解 D、粗盐提纯实验中,蒸发结晶时一定要在滤液蒸干时再停止加热8. 下列实验方案设计中,正确的是( )A、除去NaCl中少量的Na2CO3杂质,先加入过量的CaCl2溶液,过滤后再蒸发结晶 B、检验可燃性气体中是否含有氢元素,在其燃烧火焰上方罩上干冷的烧杯,观察有无水雾 C、实验测定某矿石中碳酸钙的质量分数,先加入稀硫酸,再比较反应前后的质量变化 D、实验室制备干燥纯净的氢气,用锌与浓盐酸反应,产生的气体经浓硫酸干燥后收集9. 根据事物的某些相似性类推其他的相似性,并预测类似的可能性,是我们经常使用的一种思维方法。以下类推结果与实际相符的是( )①氧化物中都含有氧元素 含有氧元素的化合物都是氧化物
②某饱和溶液不能继续溶解某相应溶质 饱和溶液也不能继续溶解其它溶质
③氢氧化钠溶液中有OH— , 能与酸反应 氢氧化钾溶液中也有OH— , 也能与酸反应
④盐中含有金属离子和酸根离子 NH4NO3没有金属离子,不属于盐类
A、只有③ B、①③ C、①③④ D、②③④10. 下列叙述中,不符合实验事实的是( )
A、在K2CO3、K2SO4、AgNO3三种溶液中分别滴入BaCl2溶液,都有白色沉淀生成 B、将少量SO3加入到滴有石蕊试液的蒸馏水中,溶液显红色 C、未密封保存的苛性钠遇盐酸有气体生成 D、将Fe(OH)3加入到滴有酚酞试液的蒸馏水中,溶液显红色二、填空题
-
11. 铁粉和硫粉以适当的质量比混合,堆放在石棉网上,然后用烧红的玻璃板一端接触混合物,这时部分混合物迅速变红热状态,撤离玻璃棒后,反应继续进行,直至全部混合物都呈红热的状态,冷却后得到一种黑色无磁性的固态物质.该黑色无磁性的固态物质在物质分类上属于(选填“酸”、“碱”、“盐”或“氧化物”).
12.下列分别盛有不同物质的容器中,所盛物质属于纯净物的是 ,混合物的是 ,单质的是 ,化合物的是 。(均填容器代号)
 13. 已知某混合溶液由HCl、K2CO3、H2SO4、CuCl2溶液中的几种混合而成,向该混合液中加Ba(OH)2溶液,产生沉淀量与加的Ba(OH)2溶液体积关系如图.则混合溶液中一定有的是 , 沉淀完全时,消耗Ba(OH)2g.
13. 已知某混合溶液由HCl、K2CO3、H2SO4、CuCl2溶液中的几种混合而成,向该混合液中加Ba(OH)2溶液,产生沉淀量与加的Ba(OH)2溶液体积关系如图.则混合溶液中一定有的是 , 沉淀完全时,消耗Ba(OH)2g. 14.
14.构建知识网络是学习化学的重要方法,如图是不同物质相互转化关系图.其中A、B、C、D属于不同类别的物质,且都含有铜元素,B为黑色粉末,C为红色粉末.“→”表示一种物质一步转化成另一种物质(部分反应物、生成物及反应条件未标出),请回答问题:
(1)C的化学式 ,A的化学式 .
(2)写出由B生成硫酸铜的化学方程式 .
(3)在该知识网络所涉及的化学反应中,可以归纳出能与盐发生反应的物质类别有 .
A、单质 B、氧化物 C、酸 D、碱 E、盐.

三、综合题
-
15.
水是生命之源,“珍惜水、节约水、保护水”是每个公民的义务和责任。
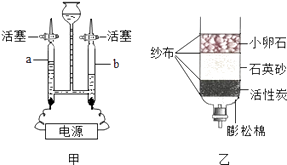 (1)、下列“水”属于纯净物的是 (填序号)A、蒸馏水 B、河水 C、自来水 D、矿泉水(2)、用如图甲装置进行电解水的实验,b中收集到的气体是。16.
(1)、下列“水”属于纯净物的是 (填序号)A、蒸馏水 B、河水 C、自来水 D、矿泉水(2)、用如图甲装置进行电解水的实验,b中收集到的气体是。16.如图中各物质间的反应均在溶液中进行,已知甲、乙为化合物,丙为单质.请根据图示关系回答下列问题:
 (1)、X的化学式是 .(2)、CuCl2与物质丙反应的基本类型是 .17.
(1)、X的化学式是 .(2)、CuCl2与物质丙反应的基本类型是 .17.某工厂的废液中含有较多的CuSO4和FeSO4两种物质,工厂常用下列流程将废液充分利用:
 (1)、写出步骤①中发生的化学方程式 ,为什么要加入过量的铁粉 ;(2)、写出步骤②中发生的化学反应现象是;(3)、写出滤渣B的化学式: ;(4)、将步骤①和②中产生的滤液B混合进行蒸发结晶,此操作过程需要用到的仪器有玻璃棒、酒精灯、带铁圈的铁架台和 .18. 物质的性质、用途与其组成有密切的联系。现有石墨、甲烷、氧气、乙炔(C2H2)、水、丁烷(C4H10)等六种物质,试根据要求回答下列问题。(1)、科学家常根据组成来对物质进行分类,上述物质中的石墨和氧气归为一类,甲烷、乙炔、水、丁烷归为另一类,其分类依据是。(2)、甲烷、乙炔、丁烷三种物质都具有可燃性,据此性质,它们常用来作燃料。在运输储存时,需将这些气体加压液化。已知它们的沸点随着相对分子质量的增大而降低,若使这三种气体在常温下液化,则需要施加的压强最大的是。19. 宁波有较长的海岸线,每年能生产大量的食用盐。从海水中结晶的食盐一般混有MgCl2、CaCl2、Na2SO4等杂质,为了除去上述杂质,设计了如下实验方案:先将固体溶解,然后向溶液中依次加入过量的BaCl2、NaOH、Na2CO3溶液,充分反应后过滤,将滤液蒸发结晶,得到较纯净的食盐。(1)、溶解、过滤和蒸发操作中都要用到玻璃棒。过滤时,玻璃棒的作用是。(2)、加入BaCl2溶液的目的是为了除去杂质。(3)、以上方案不够完善.应在过滤后增加一个步骤:往滤液中加入适量的。20. 碳酸钠俗名纯碱,是玻璃、造纸、肥皂、洗涤剂、纺织、制革等工业的重要原料.我国化学家侯德榜对制碱工业有重大贡献,他发明的制碱方法,被誉为“侯氏制碱法”,其生产工艺流程示意图及过程中涉及的主要反应如图:
(1)、写出步骤①中发生的化学方程式 ,为什么要加入过量的铁粉 ;(2)、写出步骤②中发生的化学反应现象是;(3)、写出滤渣B的化学式: ;(4)、将步骤①和②中产生的滤液B混合进行蒸发结晶,此操作过程需要用到的仪器有玻璃棒、酒精灯、带铁圈的铁架台和 .18. 物质的性质、用途与其组成有密切的联系。现有石墨、甲烷、氧气、乙炔(C2H2)、水、丁烷(C4H10)等六种物质,试根据要求回答下列问题。(1)、科学家常根据组成来对物质进行分类,上述物质中的石墨和氧气归为一类,甲烷、乙炔、水、丁烷归为另一类,其分类依据是。(2)、甲烷、乙炔、丁烷三种物质都具有可燃性,据此性质,它们常用来作燃料。在运输储存时,需将这些气体加压液化。已知它们的沸点随着相对分子质量的增大而降低,若使这三种气体在常温下液化,则需要施加的压强最大的是。19. 宁波有较长的海岸线,每年能生产大量的食用盐。从海水中结晶的食盐一般混有MgCl2、CaCl2、Na2SO4等杂质,为了除去上述杂质,设计了如下实验方案:先将固体溶解,然后向溶液中依次加入过量的BaCl2、NaOH、Na2CO3溶液,充分反应后过滤,将滤液蒸发结晶,得到较纯净的食盐。(1)、溶解、过滤和蒸发操作中都要用到玻璃棒。过滤时,玻璃棒的作用是。(2)、加入BaCl2溶液的目的是为了除去杂质。(3)、以上方案不够完善.应在过滤后增加一个步骤:往滤液中加入适量的。20. 碳酸钠俗名纯碱,是玻璃、造纸、肥皂、洗涤剂、纺织、制革等工业的重要原料.我国化学家侯德榜对制碱工业有重大贡献,他发明的制碱方法,被誉为“侯氏制碱法”,其生产工艺流程示意图及过程中涉及的主要反应如图:
①NH3+H2O+CO2═NH4HCO3 ②NH4HCO3+NaCl═NH4Cl+NaHCO3(晶体)
③2NaHCO3 Na2CO3+H2O+CO2↑,请回答下列问题:
(1)、碳酸钠属于(填“酸”、“碱”或“盐”),它的俗名叫纯碱是因为 .(2)、粗盐水中主要含有Ca2+、Mg2+、SO42﹣等杂质离子,工业上常加入稍过量的NaOH溶液、BaCl2溶液、Na2CO3溶液及适量的盐酸等除去杂质离子、精制.加入稍过量的NaOH溶液可以除去 , 加NaOH溶液和加BaCl2溶液的先后顺序(选填“可以”或“不可以”)颠倒;最后加入盐酸的目的是 .(3)、X是滤液中最主要的成分,X与Ca(OH)2反应的产物之一可用于该生产工艺流程的循环使用,该产物为 .