2017年科学中考复习专题:化学式与化合价
试卷更新日期:2017-03-24 类型:二轮复习
一、单选题
-
1. “84”消毒液广泛应用于宾馆、医院、家庭等的卫生消毒,其主要成分是次氯酸钠(NaClO).NaClO中氯元素的化合价为( )A、﹣1 B、0 C、+1 D、+22. 用“王水”(浓盐酸与浓硝酸的混合物)溶解某金属M后得到一种酸性物质:HMCl4 , 则下列物质所含M元素的化合价与HMCl4不同的是( )A、M2O3 B、M(NO3)3 C、M2ClO D、MPO43. 有四位同学对某化学式的描述是:甲表示一种物质;乙表示一个分子;丙表示该物质由不同种元素组成;丁表示一个分子由二个原子构成。他们描述的化学式是( )A、CO B、SO2 C、N2 D、H2O4. 水中好坏直接影响人的健康,高铁酸钾(K2FeO4)是一种新型高效净水处理剂.高铁酸钾是暗紫色粉末,溶于水中生成紫红色溶液.下列有关高铁酸钾的分析中,正确的是( )A、高铁酸钾是一种氧化物 B、高铁酸钾中铁元素的化合价是+3价 C、高铁酸钾是由三种元素组成 D、高铁酸钾中含有单质铁5.
如图所示是某化学反应的微观示意图.下列关于该化学反应的说法错误的是( )
 A、反应类型是分解反应 B、反应前后各元素化合价不变 C、反应前后两种原子的数目不变 D、反应物是由两种元素组成的化合物6. 中国药学家屠呦呦因发现并提取出青蒿素,获得2015年诺贝尔生理学或医学奖,青蒿素(化学式:C15H22O5)被广泛用于治疗疟疾.下列说法正确的是( )A、青蒿素属于氧化物 B、青蒿素分子由C、H、O三种元素组成 C、青蒿素中碳、氢、氧元素的质量比为15:22:5 D、每个青蒿素分子都由15个碳原子、22个氢原子和5个氧原子构成7. 某硝酸铵(NH4NO3)样品中混有一种其他氮肥,经分析样品含有36%的氮,那么该样品可能混有的氮肥是( )A、NH4HCO3 B、(NH4)2SO4 C、NH4Cl D、CO(NH2)28.
A、反应类型是分解反应 B、反应前后各元素化合价不变 C、反应前后两种原子的数目不变 D、反应物是由两种元素组成的化合物6. 中国药学家屠呦呦因发现并提取出青蒿素,获得2015年诺贝尔生理学或医学奖,青蒿素(化学式:C15H22O5)被广泛用于治疗疟疾.下列说法正确的是( )A、青蒿素属于氧化物 B、青蒿素分子由C、H、O三种元素组成 C、青蒿素中碳、氢、氧元素的质量比为15:22:5 D、每个青蒿素分子都由15个碳原子、22个氢原子和5个氧原子构成7. 某硝酸铵(NH4NO3)样品中混有一种其他氮肥,经分析样品含有36%的氮,那么该样品可能混有的氮肥是( )A、NH4HCO3 B、(NH4)2SO4 C、NH4Cl D、CO(NH2)28.中国科学院某研究小组设计了一种高性能锂空气电池,其反应原理可表示为:2Li+O2
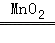 Li2O2 , 已知锂元素在化合物中显+1价,下列说法错误的是( )A、反应物锂是金属单质 B、该反应中MnO2是催化剂 C、Li2O2中氧元素的化合价显﹣2价 D、该反应是化合反应9. 下列化学用语与所表述的意义相符的是( )
Li2O2 , 已知锂元素在化合物中显+1价,下列说法错误的是( )A、反应物锂是金属单质 B、该反应中MnO2是催化剂 C、Li2O2中氧元素的化合价显﹣2价 D、该反应是化合反应9. 下列化学用语与所表述的意义相符的是( )①2Ca2+﹣﹣2个钙离子 ②O2﹣﹣2个氧原子 ③2H2O﹣﹣2个水分子
④2H﹣﹣2个氢元素 ⑤ ﹣﹣氮气中氮元素的化合价为零.
A、①④⑤ B、②④ C、①③⑤ D、②③10. 下列有关化学符号“CO2”表示的意义,正确的是( )
A、二氧化碳这种物质 B、二氧化碳由两个氧元素和一个碳元素组成 C、一个二氧化碳分子中含有一个氧分子 D、二氧化碳由碳原子和氧原子构成11. 下列有关“2”的解释中,正确的是( )A、“Zn2+”中的“2+”表示锌粒带两个单位的正电荷 B、2NO中的“2”表示两个一氧化氮分子 C、H2SO4中的“2”表示一个分子中含有两个氢元素 D、H2中的“2”表示氢气含有两个氢原子12. 元素周期表中,同周期元素的结构和性质呈现一定的规律性变化。下表列出的是第三周期元素的原子半径及主要化合价(部分信息未列出).下列有关说法不正确的是( )元素
Na
Mg
①
Si
P
②
Cl
原子的最外层电子数
1
2
3
4
5
6
7
原子半径(10﹣10m)
1.86
1.60
1.43
③
1.10
1.02
0.994
最高正价
最低负价
+1
+2
④
+4
﹣4
+5
﹣3
⑤
+7
﹣1
A、⑤处的最高正价是+6,最低负价是﹣2 B、③处的数值介于1.10﹣1.43之间 C、第三周期元素(Na→Cl)的最高正价数等于其原子的最外层电子数 D、元素①的原子序数是13,①和②形成的化合物的化学式为AlS二、填空题
-
13. 今年科学家成功制备了一种含有铱元素(Ir)的带一个单位正电荷的离子(四氧化铱正离子),结构模型如图所示,则该离子的符号为 , 其中铱元素的化合价是。
 14. 有6种物质能按下列顺序排列:①CO ②H2O ③NH3 ④X ⑤C2H4 ⑥P2O5。根据它们的组成和排列的规律,X可能是(填选项字母),解释你选择的理由:。
14. 有6种物质能按下列顺序排列:①CO ②H2O ③NH3 ④X ⑤C2H4 ⑥P2O5。根据它们的组成和排列的规律,X可能是(填选项字母),解释你选择的理由:。A.Na2SO4
B.CH4
C.PCl5
D.Fe2O3
15. 用文字描述下列化学符号的意义:①2H2O;②3C ;
③O2;④SO2中2的含义 ;
⑤Al3+ 中“3+”表示;⑥3个铵根离子;
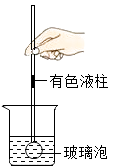
16.化学反应常伴随能量变化,如图所示,在装有水的烧杯中放入一定质量的生石灰固体,反应片刻后可观察到玻璃管中的有色液体柱将(选填“上升”、“下降”或“不变”),请写出反应后所得溶液中溶质的化学式 .
三、综合题
-
17. 为适应不同人群的需要,市场上供应的食盐除普通碘盐外还有无碘竹盐、低钠盐和健康平衡盐等,现有两种品牌的食盐A和B,主要成分的含量见表:(注:两种食盐仅NaCl中含有钠元素:35.1g/100g表示每100g食盐中含钠元素质量为35.1g)
食盐种类
食盐A
食盐B
主要成分的含量
(以钠元素质量计)35.1g/100g
(以NaCl质量计)93.0g/100g
(1)、加碘盐是通过加入KIO3的方法制成的,KIO3中碘元素的化合价为 .(2)、NaCl中钠元素质量分数以39%计,请比较食盐A、B中NaCl含量高低,其中含量较高的是(填食盐种类).18. 最近电茶壶等不锈钢食具容器安全问题引起消费者关注.不锈钢中有铁、碳、硅和锰.有些食具容器所用不锈钢材料锰含量较高,若材料中的金属锰析出超标,通过食物进入人体,可能会对神经系统有损害.(1)、铁元素在地壳中主要以化合态存在,从铁矿石中冶炼出铁的主要反应如下:Fe2O3+3CO
 2Fe+3CO2该反应分解反应;(选填“是”或“不是”)(2)、已知锰(Mn)的金属活动性强于锌,不锈钢材料中锰若析出进入人体胃中,会与胃液中的盐酸发生置换反应,反应产物中锰元素化合价+2价,请写出该反应的化学方程式;(3)、
2Fe+3CO2该反应分解反应;(选填“是”或“不是”)(2)、已知锰(Mn)的金属活动性强于锌,不锈钢材料中锰若析出进入人体胃中,会与胃液中的盐酸发生置换反应,反应产物中锰元素化合价+2价,请写出该反应的化学方程式;(3)、已知碳、铁和硅等单质能发生以下反应:①C+O2
 CO2 ②Fe+2HCl═FeCl2+H2↑ ③Si+2NaOH+H2O═Na2SiO3+2H2↑
CO2 ②Fe+2HCl═FeCl2+H2↑ ③Si+2NaOH+H2O═Na2SiO3+2H2↑请从反应前与反应后元素化合价改变的角度,归纳出3个反应的共同规律 .
19.1774年,英国科学家普里斯特利进行了如图实验,取一根一端封闭的玻璃管,在玻璃管的底部装入红色固体氧化汞,再装满汞(水银),将其倒扣在盛有汞的烧杯中,通过凸透镜将阳光会聚到氧化汞上,对其加热,使其发生化学反应,化学方程式为2HgO
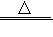 2Hg+O2↑.
2Hg+O2↑. (1)、为使加热效果最好,应使氧化汞处于凸透镜的处.(2)、氧化汞(HgO)中汞元素的化合价为 .(3)、写出该实验的现象: . (列举一点)20. 在一定条件下,甲和乙发生化学反应生成丙和丁,其反应的微观变化如图所示.
(1)、为使加热效果最好,应使氧化汞处于凸透镜的处.(2)、氧化汞(HgO)中汞元素的化合价为 .(3)、写出该实验的现象: . (列举一点)20. 在一定条件下,甲和乙发生化学反应生成丙和丁,其反应的微观变化如图所示. (1)、物质甲中氮元素的化合价是 .(2)、甲、乙、丙与丁中属于氧化物的是 .(3)、该化学反应属于基本类型中的反应.21. 抗流感药物—“达菲”被认为是迄今为止对禽流感最有疗效的药物后,全球对达菲的市场需求膨胀,达菲的主要原料莽草酸一下子成了抢手货,价格上涨几倍。全球蔓延的H1N1甲型流感,感染早期用达菲(Oseltamivir)有显著效果。“达菲”的原料莽草酸是我国传统的香料——八角茴香的重要成分。请你根据莽草酸的化学式(C7H10O5)计算:
(1)、物质甲中氮元素的化合价是 .(2)、甲、乙、丙与丁中属于氧化物的是 .(3)、该化学反应属于基本类型中的反应.21. 抗流感药物—“达菲”被认为是迄今为止对禽流感最有疗效的药物后,全球对达菲的市场需求膨胀,达菲的主要原料莽草酸一下子成了抢手货,价格上涨几倍。全球蔓延的H1N1甲型流感,感染早期用达菲(Oseltamivir)有显著效果。“达菲”的原料莽草酸是我国传统的香料——八角茴香的重要成分。请你根据莽草酸的化学式(C7H10O5)计算: (1)、莽草酸中碳、氢、氧元素的质量比为;(2)、莽草酸中碳元素的质量分数是多少;(保留一位小数);(3)、174 克莽草酸中含有多少克碳元素;(4)、目前“达菲”两颗装售价涨至30元,其中一颗“达菲”药物质量为75毫克,其中莽草酸占该药质量的80%,而目前莽草酸的市场价格为3元/克,则一颗“达菲”中莽草酸的成本价为多少元?
(1)、莽草酸中碳、氢、氧元素的质量比为;(2)、莽草酸中碳元素的质量分数是多少;(保留一位小数);(3)、174 克莽草酸中含有多少克碳元素;(4)、目前“达菲”两颗装售价涨至30元,其中一颗“达菲”药物质量为75毫克,其中莽草酸占该药质量的80%,而目前莽草酸的市场价格为3元/克,则一颗“达菲”中莽草酸的成本价为多少元?