江苏省无锡市新吴区2018-2019学年九年级上学期化学期中考试试卷
试卷更新日期:2018-11-26 类型:期中考试
一、单选题
-
1. “绿色化学”的提出,使更多的化学工艺和产品向着环境友好的方向发展,化学必将使世界变得更加绚丽多彩.下列说法中错误的是( )A、利用化学合成药物,保障人体健康 B、利用化学开发新能源,改善生存条件 C、利用多种稀有气体,制成各种光源 D、利用大量化肥和农药,增加粮食产量2. 下列变化中前者属于化学变化,后者属于物理变化的是:( )A、烟花燃放 干冰升华 B、铜丝弯曲 橘子榨汁 C、牛奶变质 钢铁生锈 D、玻璃破碎 葡萄酿酒3. 下图所示的实验操作错误的是( )A、
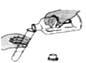 倾倒液体
B、
倾倒液体
B、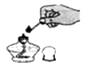 点燃酒精灯
C、
点燃酒精灯
C、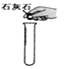 取固体颗粒
D、
取固体颗粒
D、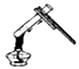 加热液体
4. 下列符号中数字“2”所表示的含义正确的是( )A、Ca2+中的“2”表示钙元素的化合价为+2价 B、H2中的“2”表示二个氢原子 C、CO2中的“2”表示一个二氧化碳分子中含有2个氧原子 D、 中的“2”表示一个钙离子带2个单位正电荷5. 不能用质量守恒定律解释的现象是( )A、蜡烛燃烧后,越来越短、最终消失 B、铁丝燃烧,其固体质量增加 C、潮湿的衣服在阳光下晒干 D、高锰酸钾受热后,固体质量减少6. 如图是几种微粒的结构示意图,有关说法错误的是( )
加热液体
4. 下列符号中数字“2”所表示的含义正确的是( )A、Ca2+中的“2”表示钙元素的化合价为+2价 B、H2中的“2”表示二个氢原子 C、CO2中的“2”表示一个二氧化碳分子中含有2个氧原子 D、 中的“2”表示一个钙离子带2个单位正电荷5. 不能用质量守恒定律解释的现象是( )A、蜡烛燃烧后,越来越短、最终消失 B、铁丝燃烧,其固体质量增加 C、潮湿的衣服在阳光下晒干 D、高锰酸钾受热后,固体质量减少6. 如图是几种微粒的结构示意图,有关说法错误的是( )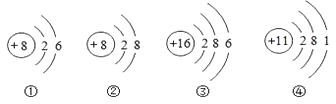 A、①和②属于同种元素 B、②表示的微粒符号为O2- C、①和③的化学性质相似 D、④表示的原子容易得到电子7. 小红的笔记本中记录了如下实验现象,其中正确的是( )A、铁丝在氧气中剧烈燃烧,生成四氧化三铁 B、红磷在空气中燃烧产生浓厚的白色烟雾 C、纯净的氢气燃烧时产生淡蓝色的火焰 D、木炭在空气中燃烧发出白光8. “神舟七号”带着国人的祝福,顺利实现太空出仓行走。“神七”在升天前加注火箭燃料四氧化二氮(N2O4)。下列叙述中,正确的是( )A、四氧化二氮是由6个元素构成的 B、四氧化二氮的相对分子质量是92g C、四氧化二氮中氮、氧元素的质量比为7:8 D、四氧化二氮分子中氮、氧原子的个数比为1:29. 建立宏观与微观之间的联系是化学学科特有的思维方式。下列对宏观事实的微观解释错误的是( )A、50mL酒精与50mL水混合后总体积小于100mL,是因为分子变小了 B、救援犬能根据气味发现因地震埋藏于地下的生命迹象,是因为分子在不断运动 C、氧气加压后变成液氧,是因为分子间的间隔变小 D、冰和干冰的化学性质不同,是因为构成它们的分子不同10. 硝酸银(AgNO3)固体见光或受热易分解,故用棕色试剂瓶保存。AgNO3受热分解,放出的有刺激性气味的气体可能是( )A、SO2 B、NO2 C、NH3 D、N211. 下列实验操作中,“先”与“后”的顺序错误的是( )A、在检查装置气密性的时候,先用双手紧握容器外壁,后将导管浸入水中 B、用酒精灯加热试管中液体时,先预热,后对准液体集中加热 C、用排水法收集完氧气时,先把导管移出水面,后熄灭酒精灯 D、做氢气可燃性实验时,先检验氢气的纯度,后点燃气体12. 某同学梳理归纳了以下知识:①物质与氧气发生的反应一定属于氧化反应 ②无论是吸入的空气还是呼出的气体中含量最多的气体都是氮气 ③门捷列夫主持测定了多个相对原子质量 ④质子数相同的微粒一定属于同种元素 ⑤纯净物一定是由同种分子构成的。其中正确的个数有( )A、1个 B、2个 C、3个 D、4个13. 据报道,中国科学技术大学研究人员用钴及其氧化物研制成一种新型催化剂,可将二氧化碳高效“清洁”地转化成液体燃料,反应的微观示意图如下。下列说法错误的是( )
A、①和②属于同种元素 B、②表示的微粒符号为O2- C、①和③的化学性质相似 D、④表示的原子容易得到电子7. 小红的笔记本中记录了如下实验现象,其中正确的是( )A、铁丝在氧气中剧烈燃烧,生成四氧化三铁 B、红磷在空气中燃烧产生浓厚的白色烟雾 C、纯净的氢气燃烧时产生淡蓝色的火焰 D、木炭在空气中燃烧发出白光8. “神舟七号”带着国人的祝福,顺利实现太空出仓行走。“神七”在升天前加注火箭燃料四氧化二氮(N2O4)。下列叙述中,正确的是( )A、四氧化二氮是由6个元素构成的 B、四氧化二氮的相对分子质量是92g C、四氧化二氮中氮、氧元素的质量比为7:8 D、四氧化二氮分子中氮、氧原子的个数比为1:29. 建立宏观与微观之间的联系是化学学科特有的思维方式。下列对宏观事实的微观解释错误的是( )A、50mL酒精与50mL水混合后总体积小于100mL,是因为分子变小了 B、救援犬能根据气味发现因地震埋藏于地下的生命迹象,是因为分子在不断运动 C、氧气加压后变成液氧,是因为分子间的间隔变小 D、冰和干冰的化学性质不同,是因为构成它们的分子不同10. 硝酸银(AgNO3)固体见光或受热易分解,故用棕色试剂瓶保存。AgNO3受热分解,放出的有刺激性气味的气体可能是( )A、SO2 B、NO2 C、NH3 D、N211. 下列实验操作中,“先”与“后”的顺序错误的是( )A、在检查装置气密性的时候,先用双手紧握容器外壁,后将导管浸入水中 B、用酒精灯加热试管中液体时,先预热,后对准液体集中加热 C、用排水法收集完氧气时,先把导管移出水面,后熄灭酒精灯 D、做氢气可燃性实验时,先检验氢气的纯度,后点燃气体12. 某同学梳理归纳了以下知识:①物质与氧气发生的反应一定属于氧化反应 ②无论是吸入的空气还是呼出的气体中含量最多的气体都是氮气 ③门捷列夫主持测定了多个相对原子质量 ④质子数相同的微粒一定属于同种元素 ⑤纯净物一定是由同种分子构成的。其中正确的个数有( )A、1个 B、2个 C、3个 D、4个13. 据报道,中国科学技术大学研究人员用钴及其氧化物研制成一种新型催化剂,可将二氧化碳高效“清洁”地转化成液体燃料,反应的微观示意图如下。下列说法错误的是( )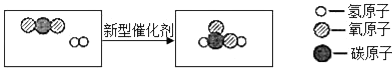 A、上图中含有3种分子 B、分子在化学变化中可以再分 C、反应物和生成物中共有两种氧化物 D、化学反应前后原子种类、数目及元素种类没有发生变化14. 已知物质A、B的组成元素相同,E是一种有刺激性气味的气体。下列推断错误的是 ( )
A、上图中含有3种分子 B、分子在化学变化中可以再分 C、反应物和生成物中共有两种氧化物 D、化学反应前后原子种类、数目及元素种类没有发生变化14. 已知物质A、B的组成元素相同,E是一种有刺激性气味的气体。下列推断错误的是 ( )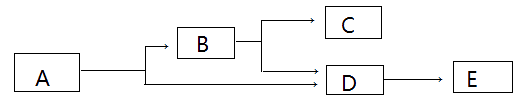 A、物质C具有可燃性 B、反应②生成的C和D的体积比是1:2 C、反应③会放出大量的热 D、反应①可以用硫酸铜溶液做催化剂
A、物质C具有可燃性 B、反应②生成的C和D的体积比是1:2 C、反应③会放出大量的热 D、反应①可以用硫酸铜溶液做催化剂二、填空题
-
15. 我们生活在一个丰富多彩的物质世界中,人类的生产、生活和化学密不可分。(1)、用适当的化学符号填空。
①地壳中含量最多的金属元素是②用于炼钢和气焊的气体
③保持二氧化碳化学性质最小的粒子④构成氯化钠的粒子
(2)、海洋不断地与陆地进行物质交换,海水中蕴藏着大量的资源。①在河水、海水、蒸馏水中不含氧分子的是。
②陆地上的河流给海水带来水和氯化钠、氯化镁、硫酸镁等盐分,镁离子的符号为。海水吸收太阳能,液态水变成气态水,盐分依然留在海水中,气态水与冷空气遭遇后冷凝形成降雨,正常的雨水属于(填“硬水”或“软水”)。硬水转化成软水的方法有(填一种)。
三、实验题
-
16. 下面几种图形是常见的气体发生和收集装置,请结合题意,回答有关问题:
 (1)、图中标有a的仪器名称是。(2)、实验室用高锰酸钾制取氧气,需要对装置A进行的改进是。试管口略向下倾斜的原因是。写出该反应的符号表达式为 , 要收集较纯净的氧气,应选择的收集装置是(填编号,下同),如果用F装置来收集氧气则应从端通入(填“①”或“②”),用此装置收集氧气时检验氧气收集满的方法是。(3)、已知二氧化碳气体可由大理石(固体)和稀盐酸(液体)反应,在常温下制得。该气体能溶于水,相同条件下,密度比空气大。由上述信息推知实验室制取二氧化碳可选用的装置组合是。(4)、某同学用如图发生装置进行过氧化氢溶液制取氧气的实验,写出过氧化氢与二氧化锰混合发生反应的符号表达式:。请写出该装置的一个优点是。实验结束后若要回收其中的二氧化锰,可采取的操作步骤是:溶解、、洗涤、烘干。
(1)、图中标有a的仪器名称是。(2)、实验室用高锰酸钾制取氧气,需要对装置A进行的改进是。试管口略向下倾斜的原因是。写出该反应的符号表达式为 , 要收集较纯净的氧气,应选择的收集装置是(填编号,下同),如果用F装置来收集氧气则应从端通入(填“①”或“②”),用此装置收集氧气时检验氧气收集满的方法是。(3)、已知二氧化碳气体可由大理石(固体)和稀盐酸(液体)反应,在常温下制得。该气体能溶于水,相同条件下,密度比空气大。由上述信息推知实验室制取二氧化碳可选用的装置组合是。(4)、某同学用如图发生装置进行过氧化氢溶液制取氧气的实验,写出过氧化氢与二氧化锰混合发生反应的符号表达式:。请写出该装置的一个优点是。实验结束后若要回收其中的二氧化锰,可采取的操作步骤是:溶解、、洗涤、烘干。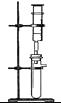
四、流程题
-
17. 煤是社会生产、生活中的重要能源,工业上常把煤进行气化和液化处理,使煤变成清洁能源。煤气化和液化流程示意图如下,请结合图像回答问题。
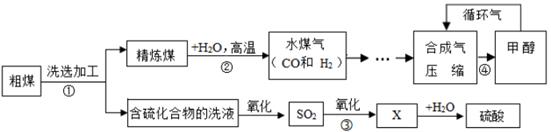 (1)、精炼煤中的主要成分是碳,步骤②中发生反应的符号表达式为。(2)、步骤③中,SO2进一步氧化得到X,X为硫的另一种氧化物,其中硫元素的化合价为+6价,X的化学式为。(3)、经过进一步净化,含较多杂质的水煤气转化成合成气(CO和H2的混合气体),步骤④中生成的甲醇(CH3OH)是一种重要的化工原料,该反应的符号表达式为 , 该反应的基本类型是。(4)、循环气的主要成分是和少量未完全分离出去的甲醇。
(1)、精炼煤中的主要成分是碳,步骤②中发生反应的符号表达式为。(2)、步骤③中,SO2进一步氧化得到X,X为硫的另一种氧化物,其中硫元素的化合价为+6价,X的化学式为。(3)、经过进一步净化,含较多杂质的水煤气转化成合成气(CO和H2的混合气体),步骤④中生成的甲醇(CH3OH)是一种重要的化工原料,该反应的符号表达式为 , 该反应的基本类型是。(4)、循环气的主要成分是和少量未完全分离出去的甲醇。五、综合题
-
18. 空气中氧气含量测定的再认识。
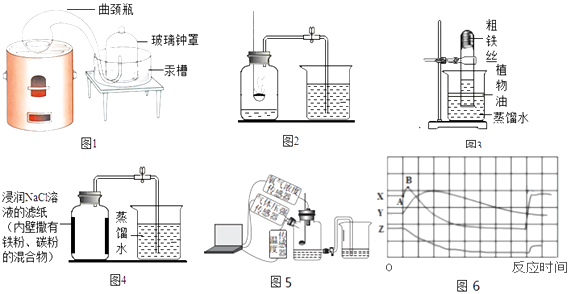 (1)、[经典赏析]拉瓦锡用定量的方法研究空气的成分(实验装置如图1)。
(1)、[经典赏析]拉瓦锡用定量的方法研究空气的成分(实验装置如图1)。该实验中选择使用汞的优点有
A.汞俗称水银,常温下呈液态,安全无毒
B.能将密闭装置内空气中的氧气几乎耗尽
C.反应生成的氧化汞是固态,不影响压强
D.生成的化合物加热分解又能得到汞和氧气
(2)、(实验回顾)实验室常用红磷燃烧的方法测定空气中氧气的含量(装置如图2),写出红磷燃烧的符号表达式。图2中集气瓶底部的水的作用为。(填字母)A.吸收有害物质
B.降温,快速冷却
C.保护瓶底
但是用该方法测出的氧气含量常常低于21%。
(3)、(提出问题)用该方法测出的氧气含量为什么低于21%?(进行猜想)①;
② , 装置内氧气有剩余
(4)、(反思拓展)结合Y、Z两条曲线,解释图6中AB段压强变化的原因是 。(5)、(实验与交流)为了帮助同学们更好地理解空气中氧气含量测定的实验原理,老师利用传感器技术定时测定了实验装置(如图5)内的压强、温度和氧气浓度,三条曲线变化趋势如图6所示。X曲线表示压强变化趋势,Y曲线表示(填“温度”或“氧气浓度”)变化趋势。(6)、(实验探究1)已知,铁丝在纯氧中才能燃烧,反应的符号表达式为 , 一般不能在空气中燃烧,因此无法用铁丝代替红磷进行该实验。小明根据铁生锈的原理(铁在常温下可以和氧气、水生成铁锈)来测定空气中氧气的含量,于是进行了实验(装置如图3)。通过7天测得的数据计算出空气中氧气的含量为19.13%。(交流与反思)与用红磷燃烧的方法相比,用铁丝生锈的方法的主要优点(填字母)。
A.装置内残留的氧气更少
B.反应更彻底,实验结果更准确
C.铁丝生锈比红磷燃烧反应更快
(7)、(实验探究2)小明利用铁粉、炭粉、氯化钠等物质又进行了实验(装置如图4)。8分钟后测得的数据如下表:请计算出空气中氧气含量(计算结果保留一位小数)。实验前的体积
实验后的体积
集气瓶内空气
烧杯内蒸馏水
烧杯内剩余蒸馏水
131mL
90.0mL
63.6mL
(8)、(拓展延伸)铜能与空气中氧气、水、二氧化碳反应生成铜绿其主要成分为:Cu2(OH)2CO3。请计算:①Cu2(OH)2CO3的相对分子质量是 。
②11.1gCu2(OH)2CO3中含有g铜元素。
-
-
-