浙江省丽水市2018-2019学年九年级上学期科学教学质量检测(一)
试卷更新日期:2018-11-16 类型:月考试卷
一、选择题
-
1. 如图是四种常见饮料的pH,其中呈碱性的饮料是( )
 A、可乐 B、橙汁 C、牛奶 D、苏打水2. 材料与人类生活密切相关,下列物品中是由有机合成材料制成的是( )A、羊毛衫
A、可乐 B、橙汁 C、牛奶 D、苏打水2. 材料与人类生活密切相关,下列物品中是由有机合成材料制成的是( )A、羊毛衫 B、装料盆
B、装料盆  C、不锈钢餐具
C、不锈钢餐具  D、玻璃杯
D、玻璃杯  3. 某校实验室将药品分类后放在不同的药品柜里,已存放的部分药品如下:
3. 某校实验室将药品分类后放在不同的药品柜里,已存放的部分药品如下:药品柜编号
①
②
③
④
…
药品
氢氧化钠
氢氧化钙
盐酸
硫酸
二氧化锰
氧化铜
氯化钠
硫酸钠
…
该实验室新购进部分生石灰和纯碱。应将它们分别放在( )
A、③和① B、④和① C、③和④ D、①和②4. 推理是化学学习中常用的思维方法。下列推理正确的是( )A、酸能使紫色石蕊溶液变红,通入 CO2 后的紫色石蕊溶液变红,所以 CO2 是酸 B、溶液中有晶体析出时,溶质质量减小,所以溶质的质量分数一定减小 C、在同一化合物中,金属元素显正价,所以非金属元素一定显负价 D、酸性溶液的 pH 小于 7,食醋是酸性溶液,所以食醋的 pH 小于 75. 如图所示实验中,①、④为用紫色石蕊溶液润湿的棉球,②、③为用石蕊溶液染成紫色的干燥棉球。下列能说明 CO2 密度大于空气且能与水反应的现象是( ) A、④比①先红,②、③不变红 B、①比④先红,②、③不变红 C、④变红,①②③不变红 D、①变红,②③④不变红6. 最近,科学家研制出一种纸质电池,这种“软电池”采用薄层纸片作为载体和传导体,在一边附着锌,在另一边附着二氧化锰。电池总反应为:Zn+2MnO2+X=ZnO+2MnOOH。下列说法正确的是( )A、X 为 H2O B、该反应中 MnO2 为催化剂 C、该反应为复分解反应 D、该反应中锌元素的化合价没有发生改变7. 科学家最近在-100℃的低温下合成了一种化合物 X,此分子的模型如图所示,其中每个
A、④比①先红,②、③不变红 B、①比④先红,②、③不变红 C、④变红,①②③不变红 D、①变红,②③④不变红6. 最近,科学家研制出一种纸质电池,这种“软电池”采用薄层纸片作为载体和传导体,在一边附着锌,在另一边附着二氧化锰。电池总反应为:Zn+2MnO2+X=ZnO+2MnOOH。下列说法正确的是( )A、X 为 H2O B、该反应中 MnO2 为催化剂 C、该反应为复分解反应 D、该反应中锌元素的化合价没有发生改变7. 科学家最近在-100℃的低温下合成了一种化合物 X,此分子的模型如图所示,其中每个 代表一个碳原子,每个
代表一个碳原子,每个  代表一个氢原子,下列说法中不正确的是:( )
代表一个氢原子,下列说法中不正确的是:( ) A、该分子的分子式 C5H4 B、该分子中碳元素的质量分数为 93.75% C、该分子中的氢原子与碳原子的原子个数比为 4∶5 D、等质量的该物质与甲烷相比,燃烧时消耗的氧气更多8. 为除去下列物质中的杂质(括号内是杂质),下列操作方法正确的是( )
A、该分子的分子式 C5H4 B、该分子中碳元素的质量分数为 93.75% C、该分子中的氢原子与碳原子的原子个数比为 4∶5 D、等质量的该物质与甲烷相比,燃烧时消耗的氧气更多8. 为除去下列物质中的杂质(括号内是杂质),下列操作方法正确的是( )选项
物质
操作方法
A
Fe(Fe2O3)
加入过量稀盐酸,充分反应后过滤
B
CaO 粉末(CaCO3 粉末)
加足量的水,充分搅拌后过滤
C
CuSO4 溶液(硫酸)
加入过量 CuO 粉末,加热,充分反应后过滤
D
NaOH 溶液(Ca(OH)2 溶液)
通入过量 CO2 气体,充分反应后过滤
A、A B、B C、C D、D9. 为了除去粗盐中的 Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作。其中不正确的操作顺序是( )①过滤,②加过量的 NaOH 溶液,③加适量盐酸,④加过量 Na2CO3 溶液,⑤加过量 BaCl2溶液。
A、④②⑤①③ B、⑤④②①③ C、②⑤④①③ D、⑤②④①③10. 将铁粉加入到一定量的硝酸银、硝酸铜及硝酸锌的混合溶液中。待充分反应后过滤,再在滤渣中加入稀盐酸,没有气体产生,则在滤液中( )
A、只有硝酸锌和水 B、如果没有硝酸铜,一定没有硝酸银 C、一定没有硝酸银 D、一定有硝酸银和硝酸亚铁11. 为适应火车提速,一些铁路线上原有的短轨需要连接成为长轨。工人常用铝热反应原理来焊接钢轨,发生的反应是 2Al+Fe2O3 Al2O3+2Fe。有关该反应的说法中,正确的是( )A、该反应属于化合反应 B、该反应中,铝作为氧化剂 C、该反应中,Fe2O3 发生还原反应 D、该反应过程中,铁元素的化合价升高12. “绿色化学”是 21 世纪科学发展的主导方向,要求从根本上杜绝污染。它包括“原料绿色化”“化学反应绿色化”“产品绿色化”等内容。其中“化学反应绿色化”要求原料物质中的所有原子完全被利用,全部转入期望的产物中。下列符合“化学反应绿色化”要求的是( )
A、制取氢气:Zn+H2SO4=ZnSO4+H2↑ B、制取氧气:2KMnO4 K2MnO4+MnO2+O2↑ C、制取碳酸氢铵:CO2+H2O+NH3=NH4HCO3 D、制取氨气:(NH4)2SO4+Ca(OH)2=CaSO4+2NH3↑+2H2O13. 等质量的 X、Y 两种金属分别和足量的同体积、同浓度的盐酸反应,产生气体的质量与时间的关系如图所示。下列说法中不正确的是( ) A、t1 时,产生气体的质量:X>Y B、t2 时,消耗金属的质量:X>Y C、t3 时,消耗金属的质量:X=Y D、t3 时,消耗盐酸的质量:X=Y14. 某学生设计的下列四个实验方案中,理论上正确、操作上可行、经济上合理的是( )
A、t1 时,产生气体的质量:X>Y B、t2 时,消耗金属的质量:X>Y C、t3 时,消耗金属的质量:X=Y D、t3 时,消耗盐酸的质量:X=Y14. 某学生设计的下列四个实验方案中,理论上正确、操作上可行、经济上合理的是( )
A、Cu CuCl2 Cu(OH)2 B、H2O O2 MgO C、CaCO3 CaO Ca(OH)2 溶液 NaOH 溶液 D、MgCl2 Mg(OH)2 Mg15.某同学为研究相同条件下一氧化碳和氢气哪个还原氧化铁的量更多,将一氧化碳和氢气等体积混合后先通过图甲装置,再通过图乙中的仪器组合。为达到实验目的,图乙中仪器选择和连接最好的是( )
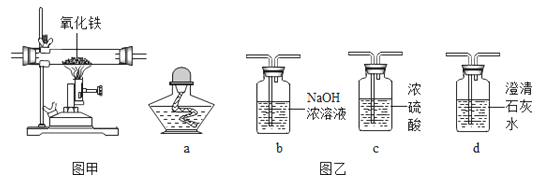 A、cba B、cda C、cbd D、bca
A、cba B、cda C、cbd D、bca二、填空题
-
16. 某市学业水平考试中有三个科学实验操作试题:①食盐溶液的配制;②二氧化碳的制取、收集和验满;③氧气的制取、收集和验满。考试的方式是由考生抽签确定试题,小凯同学抽签后被监考老师带到准备了下列仪器和药品的实验桌前:

请回答:
(1)、指出上图中仪器 a 的名称;
(2)、由实验桌上提供的仪器和药品,你认为小凯抽到的是第个试题;
(3)、以下是小凯完成该实验部分操作过程的示意图。按评分标准,每项操作正确得 1 分,实验完毕后小凯被扣了 2 分。找出有错误的实验操作(填序号)。 17. 某科学兴趣小组做了一个实验:将一个鸡蛋放入稀盐酸中。鸡蛋先沉到底部,同时在蛋壳表面看到气泡,随着气泡的增多,鸡蛋慢慢上浮。问:
17. 某科学兴趣小组做了一个实验:将一个鸡蛋放入稀盐酸中。鸡蛋先沉到底部,同时在蛋壳表面看到气泡,随着气泡的增多,鸡蛋慢慢上浮。问:
(1)、蛋壳表面看到气泡是由于产生了气体;(2)、写出产生气泡的有关化学方程式;
(3)、检验这种气体应使用的试剂是。18. 小敏设计了一种填空游戏。请按要求在方框内填入物质的化学式或反应类型。规则是:(1)、竖列必须符合物质分类要求;(2)横行必须符合基本化学反应类型;(3)所填物质的组成元素在 H、O、S、Cu 中选择。
则 1 是、3 是。
19. 运用酸、碱、盐的性质可以解决工业生产中的许多问题。(1)、工业上常选用来除去铁锈。(写出一种具体物质)(2)、某工厂向含有 AgNO3、Cu(NO3)2 的废水中加入一定量的锌粉(Zn)以回收金属,充分反应后,得到的金属组成可能有哪几种情况?。
20. 实验室用下图所示装置的部分或全部组合后完成如下实验,请回答下列问题: (1)、小明要证明鸡蛋壳的主要成分是碳酸盐,他将 A 装置中的导气管 a 与 C 装置中的导气管相连,当装置 C 中产生的现象时即达到实验目的。
(1)、小明要证明鸡蛋壳的主要成分是碳酸盐,他将 A 装置中的导气管 a 与 C 装置中的导气管相连,当装置 C 中产生的现象时即达到实验目的。
(2)、若将 A 装置中的药品换成稀硫酸和锌粒,产生的 H2 经干燥后用 D 装置收集,当 D 装置的瓶口向下时,导管口的连接顺序应是 a→b→c→。(3)、B 装置中使用过的浓硫酸稀释后,还可以用作它用,用烧杯稀释浓硫酸时,应后向烧杯中倒入的物质是。21. 氯化钠是日常生活中的必需品,某氯化钠样品中除含氯化钠外,还含有少量的 CaCl2 和MgCl2 以及不溶性杂质。以下是提纯该样品的操作流程图。

请回答下列问题:
(1)、操作 X 的名称是。(2)、Y 溶液中溶质的化学式是。(3)、上述操作流程中共发生个复分解反应。22. 某白色固体由 CuSO4、MgCl2、CaCl2、NaOH、Na2CO3 中的三种物质组成,为确定其成分,相关实验及现象如下(微溶性物质按可溶处理):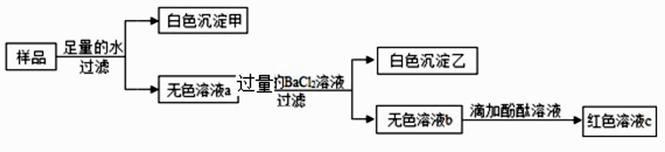
综合分析上述实验,回答下列问题:
(1)、原白色固体中一定没有的物质是;
(2)、无色溶液 a 中一定含有的溶质是;
(3)、原白色固体中只有一种物质没有确定其是否存在,要确定其是否存在,还需补充的实验是。
三、实验探究题
-
23. 利用图示仪器测量氧气体积,来测定高锰酸钾样品的纯度(杂质不参加反应),实验步骤如下:
 (1)、检查气密性:连好发生装置后,将导管口的下端浸入水中, , 如果观察到导管口有气泡冒出,就证明装置不漏气。
(1)、检查气密性:连好发生装置后,将导管口的下端浸入水中, , 如果观察到导管口有气泡冒出,就证明装置不漏气。
(2)、组装装置:连好的装置如图甲,其中有一处明显错误,在不移动、不调整酒精灯的前提下,需要调节螺母(选填字母)改正错误。(3)、进行实验:采用正确的反应装置和图乙所示的收集装置制取并收集气体,下列说法正确的是( )。A、加热时间过短,会使测量结果不准 B、反应一段时间后,排出反应装置内原有空气再连接乙装置收集气体,会使结果更准确24. 化学小组同学在加热二氧化锰样品时,发现有气泡产生(如图一所示),于是他们对这个异常现象进行了探究。
 (1)、对气体成分的探究:加热二氧化锰样品,用燃着的木条靠近试管口,木条熄灭。将气体通入澄清的石灰水,发现石灰水变浑浊,产生的气体是。
(1)、对气体成分的探究:加热二氧化锰样品,用燃着的木条靠近试管口,木条熄灭。将气体通入澄清的石灰水,发现石灰水变浑浊,产生的气体是。
(2)、对气体来源的探究:【假设 1】甲同学认为:该气体来自于试管中的空气,请你设计实验证明该假设不成立
实验步骤及现象
结论
假设不成立。
【假设2】乙同学认为:二氧化锰样品中可能混有炭粉,炭粉发生反应生成了该气体。他设计了如图二所示的实验进行研究,其中 B 装置的作用是检验 A 中反应是否完全,B中的试剂是 , 实验中乙同学从装置左端通入空气的目的是 , 结果观察到 D 处澄清石灰水变浑浊。他又用氮气代替空气(氮气不参与该实验中的任何反应),重复上述实验,发现 D 处澄清的石灰水也变浑浊。
(3)、【结论】通过乙同学的实验证明,二氧化锰中混有炭粉,炭粉与反应产生了这种气体。25. 某化学兴趣小组在实验室做了如图所示的 A、B 两个实验。 (1)、B 实验中发生反应的化学方程式为。
(1)、B 实验中发生反应的化学方程式为。
(2)、A、B 两个实验结束后,小明同学将两支试管中的物质同时加入一纯净的烧杯中(如图 C 所示),混合后,观察到烧杯中有蓝色沉淀。同学们将烧杯内的物质过滤,对所得滤液中溶质的成分进行探究。【猜想】
小明猜想:滤液中的溶质是 Na2SO4、CuSO4;
小光猜想:滤液中的溶质是 Na2SO4、NaOH;
小英猜想:滤液中的溶质是 Na2SO4、CuSO4、H2SO4;
你的猜想:滤液中的溶质还可能是 。
(3)、【讨论】你认为的猜想一定不合理。如果滤液为无色,还可排除的猜想,理由是。(4)、【实验】若小光的猜想正确,请完成下表的方案。实验步骤
预想的实验现象
实验结论
取少量滤液与试管中,滴入酚酞溶液
小光的猜想正确
26. 科学兴趣小组的同学在学了俗名为苏打的碳酸钠后,得知它还有一个俗名为小苏打的“兄弟”,这个“兄弟”的性质是否和它相似?它们之间能发生转化吗?小明查阅了资料,将相关信息整理如下:
俗名
苏打 纯碱
小苏打
化学式
Na2CO3
NaHCO3
构成微粒
Na+、
Na+ 、
溶解度(常温)
21.5 克
9.6 克
两者的转化
Na2CO3+CO2+H2O=2NaHCO3
2NaHCO3 Na2CO3+CO2↑+H2O
下面是小明同学进行的探究:
(1)、用试管取适量 NaHCO3 溶液,滴加酚酞试液,观察试液颜色变化。此实验的目的是。
(2)、在研究 Na2CO3 与 NaHCO3 转化时,小明觉得 Na2CO3 转化为 NaHCO3 过程中,由于NaHCO3 溶于水,整个过程不会有明显现象。老师笑着对小明说:“做实验吧,实验会告诉你答案。”于是,小明在老师的指导下,向饱和的 Na2CO3 溶液中通入 CO2。起初无明显现象,继续不断地通入 CO2 , 溶液中出现了白色沉淀。这让小明很疑惑:NaHCO3 溶于水,为什么还有白色沉淀产生呢?小明经过思考,明白了白色沉淀产生的原因是。
(3)、在小明同学的带动下,兴趣小组又对 NaHCO3 的其他性质进行了探究,发现两“兄弟”既有相似的性质也有不同的个性。从微观的角度分析,造成两“兄弟”不同个性的原因是不同。27. 由于大量使用一次性塑料方便袋造成的“白色污染”,已成为一个严重的社会问题。某科学研究小组的同学欲对某种塑料的组成分析探究(资料显示该塑料识含有 C、H 两种元素),他们设计了如图所示的实验装置。目的是通过测量有关数据,推算塑料组成元素的含量。图中字母 A 至 G 均表示装置编号。请根据实验装置,回答下列问题: (1)、由于发生装置 A 制取的氧气中混有 CO2 和水蒸气,为使 D 装置中塑料试样在纯氧中燃烧,装置 C 中盛放的试剂应该是。(2)、E、F 装置是气体的吸收装置,该处的设计有不正确的地方,写出如何改进并说明理由。(3)、碱石灰的成分是氢氧化钠和氧化钙,则装置连接正确时,G 装置的作用是。
(1)、由于发生装置 A 制取的氧气中混有 CO2 和水蒸气,为使 D 装置中塑料试样在纯氧中燃烧,装置 C 中盛放的试剂应该是。(2)、E、F 装置是气体的吸收装置,该处的设计有不正确的地方,写出如何改进并说明理由。(3)、碱石灰的成分是氢氧化钠和氧化钙,则装置连接正确时,G 装置的作用是。
四、解答题
-
28. 芋艿是一种常见的食品,既可当粮食,又可作蔬菜。(1)、新鲜芋艿在去皮时会产生一种白色汁液,汁液内含有一种碱性物质皂角甙,沾上它会奇痒难忍。下列物质可用来涂抹止痒的是( )。
A、食醋 B、熟石灰 C、纯碱(2)、有经验的人遇到这种情况,会将手靠近火源烘一烘,也可以达到止痒的效果;如果将带皮芋艿煮熟后,再用手去皮也不再会有痒的感觉。根据上述现象,请你推测皂角甙的一种化学性质;。
(3)、去皮的芋艿在自然条件下,表面很快因氧化而变黄色,但并不影响营养价值。有些不法商贩会用亚硫酸钠溶液浸泡,使其外观变得嫩白,造成食品安全问题。下面做法也会带来食品安全问题的是( )。A、粮库内充入氮气使粮食不易变质 B、食盐中加碘防止甲状腺肿大 C、水产品用甲醛溶液保鲜 D、用纯碱除去面团发酵产生的酸29. 某牙膏的标签内容如图所示,请回答下列问题: (1)、组成单氟磷酸钠的元素种类有种;
(1)、组成单氟磷酸钠的元素种类有种;
(2)、单氟磷酸钠中氟元素的质量分数是多少?(计算结果用最简分数表示)(3)、一支新买的该牙膏中氟元素的质量是多少克?(4)、一支新买的该牙膏中单氟磷酸钠的质量是多少克?(计算结果精确到 0.1 克)30. 为了测定某品牌食用纯碱中碳酸钠的质量分数,小明取 10 克食用纯碱样品和足量的溶质质量分数为 10%的稀硫酸,进行如图甲实验,实验前后,均需往装置中缓慢通一会氮气。(样品中其它不与稀硫酸反应) (1)、实验前,先往 A 装置通入一会氮气的目的是。
(1)、实验前,先往 A 装置通入一会氮气的目的是。
(2)、随着纯碱样品与稀硫酸反应,C 装置增加的质量变化情况如图乙所示,则该食用纯碱中碳酸钠的质量分数是多少?(碳酸钠与稀硫酸反应的化学方程式:Na2CO3+H2SO4═Na2SO4+H2O+CO2↑)
(3)、若将稀硫酸换为浓盐酸,实验中 C 装置增加的质量会偏大,请说明理由。
31. 用氢气还原氧化铜的方法测定某氧化铜样品的纯度(杂质不与氢气反应),同学们设计了以下实验装置,准确称取 15 克干燥样品进行实验。 (1)、在实验中,乙装置的作用是。
(1)、在实验中,乙装置的作用是。
(2)、准确称取完全反应前后装置丙和丁的质量如下表:装置丙
装置丁
反应前
48.8 克
161.2 克
反应后
46.5 克
163.9 克
小明根据装置丙减少的质量就是氧元素质量,求得氧化铜质量为 11.5 克,纯度为 76.7%。
小丽想根据装置丁的质量变化进行计算,请帮小丽求出氧化铜样品的纯度(写出计算过程)。
(3)、比较两种计算结果,请分析导致这一结果的原因可能是( )。A、装置的气密性不好 B、空气中的水分被丁处浓硫酸吸收 C、通入的氢气量不足 D、空气中的二氧化碳被丁处浓硫酸吸收32. 小敏对实验室用石灰石和稀盐酸制取二氧化碳后的废液,进行溶质成分鉴定。取废液上层清液 50 克,逐滴加入质量分数为 26.5%的碳酸钠溶液,出现气泡,滴加至 10 克开始出现白色沉淀。继续滴加至沉淀不再产生,过滤,测得沉淀的质量为 5 克,并绘制了图象。 (1)、滴加的溶液中溶质属于(选填“盐”或“碱”);
(1)、滴加的溶液中溶质属于(选填“盐”或“碱”);
(2)、10 克碳酸钠溶液中含有的溶质质量是克;
(3)、图象中的 a 点数值是;
(4)、废液中含有的溶质是(写化学式);(5)、通过计算说明,图象横坐标中的 b 点表示的溶液的质量是多少克?