2017年中考化学备考专题九:酸和碱
试卷更新日期:2017-03-21 类型:二轮复习
一、单选题
-
1. 下列操作中,玻璃棒其引流作用的是( )A、
 溶解
B、
溶解
B、 过滤
C、
过滤
C、 蒸发
D、
蒸发
D、 测酸碱度
2. 下列有关实验操作“先”与“后”的说法中正确的是( )A、测定溶液的pH,先将试纸用水湿润,后用干净的玻璃棒蘸取待测液点在试纸上 B、加热氯酸钾制取氧气时,用排水法收集气体;实验完毕后,先熄灭酒精灯,后将导管从水槽中移出 C、一氧化碳还原氧化铁时,先加热氧化铁粉末至红热,后通入一氧化碳气体 D、稀释浓硫酸时,先在烧杯中倒入水,后将浓硫酸沿烧杯壁缓慢地注入水中,并不断搅拌3. 推理是研究和学习化学的一种重要方法.下列推理正确的是( )A、浓盐酸具有挥发性所以浓硫酸也具有挥发性 B、某固体中加入稀盐酸,生成无色无味的气体,证明该物质一定是碳酸盐 C、点燃氢气前需要检验纯度,所以点燃甲烷前也需要检验纯度 D、向碳酸钠溶液中滴加无色酚酞溶液,溶液变成红色,说明碳酸钠属于碱类4. 要除去下列物质中的少量杂质(括号内为杂质),下列实验方案设计中,不合理的是( )A、N2(O2):将气体缓缓通过灼热的铜网 B、NaCl溶液(NaOH):加入过量的H2SO4溶液 C、CaCO3(CaCl2):加水溶解→过滤→洗涤→干燥 D、KCl溶液(K2CO3):加入适量的稀盐酸5. 将一定质量金属X的粉末放入盛有Fe(NO3)2溶液的烧杯中,充分反映后溶液呈无色;继续向烧杯中加入一定量的AgNO3溶液,待充分反应后过滤,得浅绿色滤液和滤渣.根据实验分析,以下结论错误的是( )A、金属活动性顺序:X>Fe>Ag B、滤液中一定含有X的阳离子和Fe2+ C、滤渣中一定含有Ag和Fe D、向滤液中滴加稀盐酸,可能产生白色沉淀6. 下列有关NaOH的实验方案中,正确的是( )A、用NaOH固体干燥CO2气体 B、用酚酞溶液检验NaOH溶液是否变质 C、用熟石灰和纯碱为原料制取NaOH D、用CaCl2溶液除去NaOH溶液中的少量Na2CO37. 下列实验操作、现象与结论对应关系正确的是( )
测酸碱度
2. 下列有关实验操作“先”与“后”的说法中正确的是( )A、测定溶液的pH,先将试纸用水湿润,后用干净的玻璃棒蘸取待测液点在试纸上 B、加热氯酸钾制取氧气时,用排水法收集气体;实验完毕后,先熄灭酒精灯,后将导管从水槽中移出 C、一氧化碳还原氧化铁时,先加热氧化铁粉末至红热,后通入一氧化碳气体 D、稀释浓硫酸时,先在烧杯中倒入水,后将浓硫酸沿烧杯壁缓慢地注入水中,并不断搅拌3. 推理是研究和学习化学的一种重要方法.下列推理正确的是( )A、浓盐酸具有挥发性所以浓硫酸也具有挥发性 B、某固体中加入稀盐酸,生成无色无味的气体,证明该物质一定是碳酸盐 C、点燃氢气前需要检验纯度,所以点燃甲烷前也需要检验纯度 D、向碳酸钠溶液中滴加无色酚酞溶液,溶液变成红色,说明碳酸钠属于碱类4. 要除去下列物质中的少量杂质(括号内为杂质),下列实验方案设计中,不合理的是( )A、N2(O2):将气体缓缓通过灼热的铜网 B、NaCl溶液(NaOH):加入过量的H2SO4溶液 C、CaCO3(CaCl2):加水溶解→过滤→洗涤→干燥 D、KCl溶液(K2CO3):加入适量的稀盐酸5. 将一定质量金属X的粉末放入盛有Fe(NO3)2溶液的烧杯中,充分反映后溶液呈无色;继续向烧杯中加入一定量的AgNO3溶液,待充分反应后过滤,得浅绿色滤液和滤渣.根据实验分析,以下结论错误的是( )A、金属活动性顺序:X>Fe>Ag B、滤液中一定含有X的阳离子和Fe2+ C、滤渣中一定含有Ag和Fe D、向滤液中滴加稀盐酸,可能产生白色沉淀6. 下列有关NaOH的实验方案中,正确的是( )A、用NaOH固体干燥CO2气体 B、用酚酞溶液检验NaOH溶液是否变质 C、用熟石灰和纯碱为原料制取NaOH D、用CaCl2溶液除去NaOH溶液中的少量Na2CO37. 下列实验操作、现象与结论对应关系正确的是( )选项
实验操作
现象
结论
A
向固体碳酸钙中加入稀硫酸
未见大量气泡产生
两者不反应
B
向久置于空气中的氢氧化钠溶液中滴加稀硫酸
有气泡产生
氢氧化钠已完全变质
C
将铁丝在酒精灯上加热
剧烈燃烧,火星四射
铁能被氧气氧化
D
向某溶液中滴加酚酞溶液
溶液变红
该溶液显碱性
A、A B、B C、C D、D8. 实验废液中可能含有离子K+、Mg2+、Cl﹣、Ba2+、SO42﹣、CO32﹣中的几种,为确定可能含有的离子,兴趣小组进行了下面的实验:①取一份废液,加入氯化钡溶液有白色沉淀产生,再加入足量稀盐酸,沉淀无变化;
②另取一份废液,加入氢氧化钾溶液出现白色沉淀,再加入足量稀盐酸,沉淀全部溶解,
分析上面实验得出的结论中,正确的是( )
A、只含有Mg2+、SO42﹣ B、一定含有K+、Mg2+、Cl﹣、SO42﹣ C、一定含有Mg2+、SO42﹣ , 可能含有Cl﹣、K+ D、一定含有Cl﹣、K+ , 可能含有Mg2+、SO42﹣9. 爱国科学家侯德榜先生发明了侯氏制碱法,为我国民族工业的发展做出了杰出的贡献.该方法是将CO2和NH3通过饱和的NaCl溶液中充分反应,其中的一步反应是 NH4HCO3+NaCl═NaHCO3↓+NH4Cl,下列叙述错误的是( )A、该反应不符合复分解反应发生的条件 B、该反应中四种物质都是盐 C、反应后可用过滤的方法分离出NaHCO3 D、反应后的溶液中还能继续溶解NaCl10. 下列说法正确的是( )A、酸碱中和反应生成盐和水,生成盐和水的反应一定是中和反应 B、向固体中滴加稀盐酸,有气泡产生,该固体不一定是碳酸盐 C、CO2能灭火,将燃着的镁条伸入充满CO2的瓶中,镁条立即熄灭 D、农作物生长需要N、P、K等元素,为增加肥效,可把NH4H2PO4与草木灰混合施用11. 下列反应中属于置换反应的是( )A、Fe+CuSO4=FeSO4+Cu B、2NO+O2=2NO2 C、3CO+Fe2O3 2Fe+3CO2
D、2NaCl
2Fe+3CO2
D、2NaCl  2Na+Cl2↑
12. 属于复分解反应的是( )
2Na+Cl2↑
12. 属于复分解反应的是( )
A、4NH3+3O2 6H2O+2N2
B、Na2SiO3+H2SO4═H2SiO3↓+Na2SO4
C、2FeCl2+Cl2═2FeCl3
D、2HgO
6H2O+2N2
B、Na2SiO3+H2SO4═H2SiO3↓+Na2SO4
C、2FeCl2+Cl2═2FeCl3
D、2HgO  2Hg+O2↑
13. 下列整理归纳得出的结论正确的是( )A、溶液中的溶剂一定是水 B、酸、碱中一定都含有氧元素 C、同种物质分子间的间隔,气体一定比液体大 D、生成盐和水的反应一定是中和反应14. 下列图示,不能正确反映化学反应原理的是( )A、
2Hg+O2↑
13. 下列整理归纳得出的结论正确的是( )A、溶液中的溶剂一定是水 B、酸、碱中一定都含有氧元素 C、同种物质分子间的间隔,气体一定比液体大 D、生成盐和水的反应一定是中和反应14. 下列图示,不能正确反映化学反应原理的是( )A、 向饱和的氢氧化钙中加入氧化钙
B、
向饱和的氢氧化钙中加入氧化钙
B、 向氢氧化钠溶液中滴加稀盐酸至恰好完全反应
C、
向氢氧化钠溶液中滴加稀盐酸至恰好完全反应
C、 向混有硫酸的硫酸铜溶液中逐滴加入氢氧化钠溶液
D、
向混有硫酸的硫酸铜溶液中逐滴加入氢氧化钠溶液
D、 等质量的镁、铝、锌与等质量,等质量分数的硫酸溶液反应
等质量的镁、铝、锌与等质量,等质量分数的硫酸溶液反应
二、填空题
-
15. 钢铁的生产和使用是人类文明和社会进步的一个重要标志,但钢铁的锈蚀也给人类带来了巨大的损失.铁在空气中锈蚀,实际上是铁跟等物质相互作用的结果.工人师傅在焊接钢铁制品时,通常先用稀盐酸清洗铁制品除锈,原因是(用化学方程式表示).
16. 实验室有A、B两种溶液,A能使紫色石蕊溶液变红色,B能使无色酚酞溶液变红色,则A、B两种溶液的pH大小关系是AB(填“大于”或“小于”).要测定A、B溶液的酸碱度,其做法是 .17. 填写实验报告.实验内容
实验现象
分析、结论及解释
(1)测定碱溶液的pH
取两片pH试纸,放在白瓷板上,分别用玻璃棒蘸取稀氢氧化钠溶液,将试纸显示的颜色与比较,读出pH.
/
若实验过程中,用沾有水的玻璃棒蘸取溶液,则所测得的pH
(填“>”、“=”或“<”)实际值.
(2)碱和指示剂作用取两只洁净的试管,分别加入约2mL的稀氢氧化钠溶液,澄清石灰水,再分别加入3滴无色酚酞溶液,观察溶液颜色变化.
两只试管汇中的酚酞溶液均变为
色
稀氢氧化钠溶液、澄清石灰水都呈 性.
(3)碱和非金属氧化物的反应用排水法收集一瓶呼出的气体,然后加入约2mL澄清石灰水,振荡,观察现象.
澄清石灰水变浑浊
反应的化学方程式
.
18.实验室有五瓶标签损失的物质A、B、C、D、E,它们分别是硫酸铜固体、氯化钠固体、硫酸钾固体、氢氧化钠溶液、稀盐酸,请根据下列操作鉴别它们:
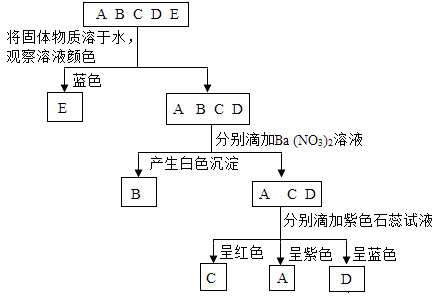
D:(填化学式);E:(填化学式)
三、综合题
-
19.
元旦联欢会上,雯雯拿出一幅画(如图所示),表演了一个化学魔术.
 (1)、她向画中的衣服上喷了一种无色溶液,衣服由紫色变成红色,若衣服上预先涂过石蕊溶液,则喷的无色溶液可能是 .(2)、她向画中的灯笼上喷了另一种无色溶液,灯笼由白色变成红色,则该无色溶液及灯笼上预先涂过的试剂分别是 .20. 请选择与下列叙述相对应物质的序号填空:
(1)、她向画中的衣服上喷了一种无色溶液,衣服由紫色变成红色,若衣服上预先涂过石蕊溶液,则喷的无色溶液可能是 .(2)、她向画中的灯笼上喷了另一种无色溶液,灯笼由白色变成红色,则该无色溶液及灯笼上预先涂过的试剂分别是 .20. 请选择与下列叙述相对应物质的序号填空:①活性炭 ②稀硫酸 ③pH试纸 ④硝酸钾 ⑤氯化钠
(1)、可用于测定溶液酸碱度的是 ;(2)、具有吸附性的是 ;(3)、生理盐水中的溶质是 ;(4)、可用于金属表面除锈的是 ;(5)、属于复合肥料的是 .21. 了解日用化工品的成分,有利于我们正确使用.名称
洗洁精
炉具清洁剂
洁厕灵
“84”消毒液
有效成分
表面活性剂
氢氧化钠
盐酸
次氯酸钠
(1)、洗洁精能清洗餐具上的油污,是因为它具有功能(填“吸附”或乳化);(2)、炉具清洁剂的pH7(填“>”“<”或“=”),使用时禁止与皮肤接触是因为氢氧化钠具有性.(3)、不能用洁厕灵清洗铁制品的原因是(用化学方程式表示).(4)、洁厕灵与“84”消毒液不能混合使用,因为两者混合会发生反应:2HCl+NaOH=NaCl+H2O+X↑有毒.X的化学式为 .22.实验是学习化学的重要途径,小亮在学习酸碱盐的化学性质时做了如下实验,请你和他一起完成实验活动.
 (1)、在白色点滴板上完成实验A,请将实验现象补充完整.
(1)、在白色点滴板上完成实验A,请将实验现象补充完整.稀硫酸
氢氧化钙溶液
实验现象
溶液变蓝色
(2)、在实验B的烧杯②中滴加2滴酚酞溶液后,扣上大烧杯,一段时间后看到的现象是 , 得出的结论是 .(3)、在实验C的试管①中,滴加少量的氢氧化钠溶液,看到的现象是 , 反应的化学方程式是 . 要使试管②中产生白色沉淀,应滴加溶液(写一种溶液).(4)、小亮用实验D验证二氧化碳与氢氧化钠溶液反应,看到的现象是 , 他根据三氧化硫与二氧化碳所属的类别,推断三氧化硫也能与氢氧化钠溶液反应,反应的化学方程式为 .23. 生活与化学密切相关,生活中处处有化学,请你根据所学化学知识回答下列问题:(1)、从分子的角度解释,25mL汽油与25mL酒精混合,体积小于50mL原因是 .(2)、农业生产中常用于改良酸性土壤的是熟石灰,其化学式为 .(3)、生活中可用于除去铁锈的两种常见的酸是稀和稀(填物质的名称).(4)、氢能源是清洁的绿色能源,其燃烧的化学方程方程式为: , 乙醇(C2H5OH)俗称“酒精”,其属于(填“有机物”或“无机物”)(5)、日常生活中可以用区分硬水和软水;可以用区分羊毛和棉花.24. 某固体物质可能含有Na2SO4、Na2CO3、CaCl2、CuSO4、KCl和KOH中的一种或几种.为探究其组成,流程和现象记录如下:【资料】CaCl2、BaCl2、KCl三种溶液均呈中性
 (1)、依据步骤①的实验现象得出故土物质中一定不含(填化学式).(2)、步骤②中发生的化学方程式为 .(3)、根据上述实验得出固体物质中一定含有(填化学式,下同);可能含有 . 为进一步确定可能含有的物质,采用的方法是(写出实验的操作、现象和结论)
(1)、依据步骤①的实验现象得出故土物质中一定不含(填化学式).(2)、步骤②中发生的化学方程式为 .(3)、根据上述实验得出固体物质中一定含有(填化学式,下同);可能含有 . 为进一步确定可能含有的物质,采用的方法是(写出实验的操作、现象和结论)