2016-2017学年江苏省南京市九年级上学期期末化学试卷
试卷更新日期:2017-03-20 类型:期末考试
一、选择题
-
1. 将下列物质分别加入水中,能形成溶液的是( )A、酒精 B、面粉 C、花生油 D、冰块2. 地壳中含量最多的金属元素是( )A、硅 B、铁 C、铝 D、钙3. 下列图示实验操作中,正确的是( )A、
 读液体体积
B、
读液体体积
B、 称量固体
C、
称量固体
C、 过滤
D、
过滤
D、 加入大理石
4. 下列图标中,表示“禁止烟火”的是( )A、
加入大理石
4. 下列图标中,表示“禁止烟火”的是( )A、 B、
B、 C、
C、 D、
D、 5. 下列各组物质中,组成元素不同的是( )A、水银和银 B、红磷和白磷 C、水和过氧化氢 D、金刚石和石墨6. 下列物质由分子构成的是( )A、C60 B、汞 C、铁 D、硫酸铜7. 下列粒子结构示意图中,表示阳离子的是( )A、
5. 下列各组物质中,组成元素不同的是( )A、水银和银 B、红磷和白磷 C、水和过氧化氢 D、金刚石和石墨6. 下列物质由分子构成的是( )A、C60 B、汞 C、铁 D、硫酸铜7. 下列粒子结构示意图中,表示阳离子的是( )A、 B、
B、 C、
C、 D、
D、 8. 有X,Y,Z三种金属,只有Y在自然界主要以单质形式存在,如果把X放入Z的硫酸盐溶液中,X表面有Z析出.据此判断这三种金属的活动性由强到弱的顺序为( )A、Y,X,Z B、Z,X,Y C、Y,Z,X D、X,Z,Y9. 下列变化,吸收热量的是( )A、木炭不充分燃烧 B、氢氧化钠固体溶于水 C、二氧化碳与碳反应 D、镁与盐酸反应10. 下列有关物质用途的叙述不正确的是( )A、汽油作除去油污的乳化剂 B、活性炭可作冰箱的除味剂 C、氮气在某些食品袋内作防腐剂 D、生石灰在某些食品袋内作干燥剂11. 化学家已经开发出多种酯类人工香料,如丁酸甲酯(C5H10O2)具有苹果香味.下列有关丁酸甲酯的说法正确的是( )A、丁酸甲酯属于氧化物 B、丁酸甲酯由17个原子构成 C、丁酸甲酯中氧元素的质量分数约为58.82% D、丁酸甲酯中碳元素、氢元素和氧元素的质量比为30:5:1612. 酸雨形成过程中某一步反应的微观示意图如下,下列说法正确的是( )
8. 有X,Y,Z三种金属,只有Y在自然界主要以单质形式存在,如果把X放入Z的硫酸盐溶液中,X表面有Z析出.据此判断这三种金属的活动性由强到弱的顺序为( )A、Y,X,Z B、Z,X,Y C、Y,Z,X D、X,Z,Y9. 下列变化,吸收热量的是( )A、木炭不充分燃烧 B、氢氧化钠固体溶于水 C、二氧化碳与碳反应 D、镁与盐酸反应10. 下列有关物质用途的叙述不正确的是( )A、汽油作除去油污的乳化剂 B、活性炭可作冰箱的除味剂 C、氮气在某些食品袋内作防腐剂 D、生石灰在某些食品袋内作干燥剂11. 化学家已经开发出多种酯类人工香料,如丁酸甲酯(C5H10O2)具有苹果香味.下列有关丁酸甲酯的说法正确的是( )A、丁酸甲酯属于氧化物 B、丁酸甲酯由17个原子构成 C、丁酸甲酯中氧元素的质量分数约为58.82% D、丁酸甲酯中碳元素、氢元素和氧元素的质量比为30:5:1612. 酸雨形成过程中某一步反应的微观示意图如下,下列说法正确的是( ) A、该反应属于化合反应 B、该反应前后共涉及到4种分子 C、该反应前后硫元素化合价不变 D、该反应不符合质量守恒定律13. 除去下列物质中的少量杂质(括号内为杂质),方法不正确的是( )
A、该反应属于化合反应 B、该反应前后共涉及到4种分子 C、该反应前后硫元素化合价不变 D、该反应不符合质量守恒定律13. 除去下列物质中的少量杂质(括号内为杂质),方法不正确的是( )选项
物质(杂质)
除去杂质的方法
A
MnO2固体(KCl固体)
加足量水溶解,过滤、洗涤、干燥
B
O2(H2)
点燃
C
CaO固体(CaCO3固体)
高温充分煅烧
D
FeSO4溶液(CuSO4)
加入足量的Fe粉充分反应后,过滤
A、A B、B C、C D、D14. 下列通过对比实验得出的结论不正确的是( )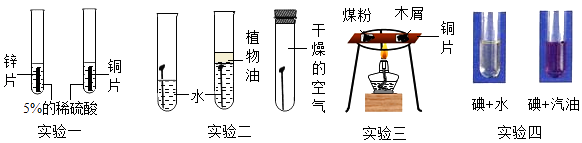 A、实验一可以证明锌的金属活动性比铜强 B、实验二可以说明铁生锈的条件是与氧气和水同时解除 C、实验三可以说明燃烧的条件之一是需要可燃物 D、实验四可以说明物质的溶解性与溶剂种类有关15. 为探究锌、铜、铁三种金属的活动性顺序,某小组做了如甲图所示实验。实验结束后,将试管①、试管②内的物质全部倒入同一烧杯中,充分反应后发现烧杯中的红色固体物质明显增多(如乙图所示)。
A、实验一可以证明锌的金属活动性比铜强 B、实验二可以说明铁生锈的条件是与氧气和水同时解除 C、实验三可以说明燃烧的条件之一是需要可燃物 D、实验四可以说明物质的溶解性与溶剂种类有关15. 为探究锌、铜、铁三种金属的活动性顺序,某小组做了如甲图所示实验。实验结束后,将试管①、试管②内的物质全部倒入同一烧杯中,充分反应后发现烧杯中的红色固体物质明显增多(如乙图所示)。
下列说法正确的是( )
A、甲图试管①中溶液颜色发生改变 B、甲图试管②中的溶液中含有FeCl3 C、乙图烧杯中的溶液一定只含有两种溶质 D、乙图烧杯中最后所得固体的质量可能等于3.2g二、非选择题
-
16. 根据下列装置图,回答有关问题.
 (1)、写出装置图中标号仪器的名称:a , b .(2)、实验室用高锰酸钾制取氧气的化学方程式为 , 收集装置可用C或(填字母).(3)、实验室用大理石与稀盐酸制取二氧化碳气体时,应选择的发生装置是(填字母);发生反应的化学方程式为 .(4)、实验室需少量甲烷气体,可用加热无水硫酸钾与碱石灰的固体混合物制得,则可选用的发生装置是(填字母).(5)、实验室可用粗锌与稀硫酸制取氢气,若用此方法制得0.3g氢气,至少需要含锌97.5%的粗锌的质量是多少(假设杂质不反应)?17. 根据如表回答问题:
(1)、写出装置图中标号仪器的名称:a , b .(2)、实验室用高锰酸钾制取氧气的化学方程式为 , 收集装置可用C或(填字母).(3)、实验室用大理石与稀盐酸制取二氧化碳气体时,应选择的发生装置是(填字母);发生反应的化学方程式为 .(4)、实验室需少量甲烷气体,可用加热无水硫酸钾与碱石灰的固体混合物制得,则可选用的发生装置是(填字母).(5)、实验室可用粗锌与稀硫酸制取氢气,若用此方法制得0.3g氢气,至少需要含锌97.5%的粗锌的质量是多少(假设杂质不反应)?17. 根据如表回答问题:温度(℃)
20
40
50
60
80
溶解度g
NaCl
36.0
36.6
37.0
37.3
38.4
NH4Cl
37.2
45.8
50.4
55.2
65.6
KNO3
31.6
63.9
85.5
110
169
(1)、20℃时,溶解度最大的物质是 .(2)、40℃时,100g水中最多溶解NaClg.(3)、甲是80℃含有110g水的KNO3溶液,经过如下操作,得到20gKNO3固体.
①丁溶液为(选填“饱和”或“不饱和”)溶液.
②对以上过程的分析,正确的是(填字母).
A.甲到乙的过程中,溶质质量没有改变
B.乙种溶质与溶剂的质量比为169:100
C.开始析出KNO3固体的温度在40℃至50℃之间
D.甲溶液的质量等于161.6g.
18. 能源、环境、安全已成为人们日益关注的问题.(1)、三大化石燃料包括煤、、天然气等;它们都是(填“可再生”或“不可再生”)能源.(2)、控制反应的条件可使燃料充分燃烧.燃煤发电时,将煤块粉碎成煤粉的目的是(3)、天然气主要成分为甲烷,写出甲烷充分燃烧的化学方程式下列有关天然气(或甲烷)的说法正确的是(填字母).
A.沼气中的主要成分是甲烷
B.甲烷气体不会产生温室效应
C.用天然气代替煤作燃料,有利于减少酸雨形成
(4)、二氧化碳灭火器可用于扑救档案室发生的火灾,下列说法正确的是(填字母).A.液态二氧化碳汽化后不会污染档案
B.二氧化碳密度比空气大,覆盖在可燃物表面,隔绝空气
C.液态二氧化碳汽化时吸热,降低可燃物的着火点.
19. 21世纪是钛的世纪.利用钛白粉(TiO2)生产海绵钛(Ti)的工艺流程如下: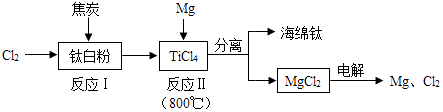 (1)、该工艺流程所使用的原料中,属于氧化物的是(填化学式).(2)、反应II可获得海绵钛,化学方程式为 .(3)、该工艺流程中,可以循环使用的物质有氯气和 .20. 图中的A~H表示几种初中化学常见的物质,分别是由H、C、O、Al、S、Cu中的一种或几种元素组成的.其中B、C、D、E、F均属于单质,G、H属于氧化物.B具有恨到的抗腐蚀性能;D是最清洁的燃料;G有毒.图中“﹣”表示两端的物质间能发生化学反应:“→”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去.
(1)、该工艺流程所使用的原料中,属于氧化物的是(填化学式).(2)、反应II可获得海绵钛,化学方程式为 .(3)、该工艺流程中,可以循环使用的物质有氯气和 .20. 图中的A~H表示几种初中化学常见的物质,分别是由H、C、O、Al、S、Cu中的一种或几种元素组成的.其中B、C、D、E、F均属于单质,G、H属于氧化物.B具有恨到的抗腐蚀性能;D是最清洁的燃料;G有毒.图中“﹣”表示两端的物质间能发生化学反应:“→”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去.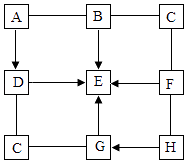 (1)、D的名称是 .(2)、C的化学式为 .(3)、写出B→E反应的化学方程式 .(4)、写出F与H反应的化学方程式 .21. 某化学兴趣小组在一个充满O2的密闭容器中加入一定量的碳粉,在高温条件下使其充分反应,待反应结束后,容器中的碳粉已全部消失.该小组成员对容器中反应后的气体进行如下探究:(1)、【提示】①CO2+2NaOH=Na2CO3+H2O;②浓硫酸能吸水.
(1)、D的名称是 .(2)、C的化学式为 .(3)、写出B→E反应的化学方程式 .(4)、写出F与H反应的化学方程式 .21. 某化学兴趣小组在一个充满O2的密闭容器中加入一定量的碳粉,在高温条件下使其充分反应,待反应结束后,容器中的碳粉已全部消失.该小组成员对容器中反应后的气体进行如下探究:(1)、【提示】①CO2+2NaOH=Na2CO3+H2O;②浓硫酸能吸水.【知识回顾】碳充分燃烧和不充分燃烧的产物是不同的,写出碳不充分燃烧的化学方程式 .
(2)、【提出猜想】(i)小红对容器中气体的组成提出如下四种猜想:A.C和CO B.只有CO C.CO和O2的混合气体 D.只有CO2
你认为上述猜想中明显不合理的有(填字母).
(ii)小明认为容器中的气体还可能是CO和CO2的混合气体;小强认为容器中的气体还可能是 .
(3)、【实验探究1】小明为了验证自己的猜想,按如图所示装置进行探究.
请回答下列问题:
(i)装置B中NaOH溶液的作用是
(ii)若小明的猜想成立,则装置A中的实验现象是 , 反应的化学方程式是 , 装置D玻璃管中的实验现象是 , 反应的化学方程式是 .
(4)、【实验探究2】小强把小明实验中的氧化铁换成了铜丝网,并去掉E装置验证其猜想.若小强的猜想成立,则装置D中的实验现象是 .(5)、【反思交流】有同学认为,小强应先通入容器中气体一段时间后方可加热,你认为这样修改的原因是 .(6)、【拓展延伸】若反应前容器中碳粉的质量为6g且小明的猜想成立,则容器中氧气质量的取值范围是 .