2016-2017学年湖南省常德市澧县九年级上学期期末化学试卷
试卷更新日期:2017-03-20 类型:期末考试
一、选择题
-
1. 有下列现象:①火药爆炸;②蒸发食盐水;③蒸馏石油分离出汽油等物质;④燃放礼花;⑤牛奶变酸;⑥塑料受热变软;⑦碘受热升华,⑧加热胆矾.其中属于化学变化的是( )A、①②③④ B、⑤⑥⑦⑧ C、①④⑤⑧ D、②③⑥⑦2. 科学实验测定,正常情况下人类头发的化学组成为:45%的碳、28%的氧、15%的氮、7%的氢和5%的硫等.这里的碳、氧、氮、氢、硫泛指( )A、元素 B、单质 C、原子 D、分子3. 化学反应前后,肯定没有变化的是( )
①原子的数目
②分子的数目
③元素的种类
④物质的总质量
⑤物质的种类
⑥原子的种类.
A、①③④⑥ B、①③④⑤⑥ C、①④⑥ D、①③⑤4. 下列化学方程式书写正确的是( )A、Mg+O2═MgO2 B、Cu2(OH)2CO3═2CuO+H2O+CO2↑ C、H2O2=H2↑+O2↑ D、CO2+Ca(OH)2═CaCO3↓+H2O5. 以下关于燃烧现象的描述,不正确的是( )A、硫在氧气中燃烧发出蓝紫色火焰 B、铁丝在氧气中燃烧火星四射,形成黑色固体 C、蜡烛在氧气中燃烧产生大量白烟 D、镁带在空气中燃烧发出耀眼白光,形成白色粉末6. 金属元素和人体健康有很大关系.钾元素可以调节体液平衡,维持肌肉和神经的功能代谢.如果人体缺钾会出现肌肉不发达、心律不齐等症状.市场上出售的一种叫做果味钾的补钾药.其主要成分是枸椽酸钾(C6H7K3O8).下列有关对枸椽酸钾的说法正确的是( )A、该物质的一个分子中含有25个原子 B、该物质中碳、氢、钾、氧元素的质量比是6:7:3:8 C、该物质是由原子直接构成的 D、该物质是由碳、氢、钾、氧四种元素组成的7. 下列各有关的叙述,反映物质的物理性质的是( )A、加油站内严禁烟火,严禁接打手机 B、相同条件下,铁的密度比镁的密度大 C、在潮湿的空气中铁易生锈 D、绿色的碱式碳酸铜受热变成黑色8. 根据质量守恒定律,电解氯化钠的水溶液,不可能得到的生成物是( )A、KNO3 B、H2 C、Cl2 D、NaOH9. 下列各组气体中不能用同种方法收集的是( )A、H2和O2 B、CH4和CO C、CO2和H2 D、O2和CO210. 元素周期表是学习化学的重要工具,如图是元素周期表中的一格,以下从该图获取的信息中错误的是( ) A、该元素属于金属元素 B、该元素的原子序数是56 C、该元素的原子核外有56个电子 D、该元素的相对原子质量是137.3g11. 取相对分子质量为46的某有机物4.6g,在足量的氧气中充分燃烧,生成8.8克二氧化碳和5.4克水,据此判断该有机物( )A、只由碳、氢两种元素组成 B、一定含有碳、氢、氧三种元素 C、其分子中C,H,O原子个数比为2:5:1 D、其化学式CH2O212. 把w克CO2通入足量的澄清石灰水中,得到的沉淀为x克.若先将w克CO2经过:CO2→CO→CO2变化(假定无损耗),再通入足量的澄清石灰水中,得到的沉淀为y克.则x与y的关系是( )A、x=y B、x>y C、x<y D、无法确定13. 现将10g A和足量B混合加热,A和B发生化学反应,10g A完全反应后生成8g C和4g D,则参加反应的A和B的质量比是( )A、1:1 B、2:1 C、4:1 D、5:114. 用一块棉布手帕浸泡在盛有质量分数约为70%的酒精溶液中,待均匀湿透后取出.将浸透的手帕舒展开,用镊子夹住两角,用火点燃(如图所示)当手帕上的火焰熄灭后,手帕完好无损.对于这一现象,下面解释正确的是( )
A、该元素属于金属元素 B、该元素的原子序数是56 C、该元素的原子核外有56个电子 D、该元素的相对原子质量是137.3g11. 取相对分子质量为46的某有机物4.6g,在足量的氧气中充分燃烧,生成8.8克二氧化碳和5.4克水,据此判断该有机物( )A、只由碳、氢两种元素组成 B、一定含有碳、氢、氧三种元素 C、其分子中C,H,O原子个数比为2:5:1 D、其化学式CH2O212. 把w克CO2通入足量的澄清石灰水中,得到的沉淀为x克.若先将w克CO2经过:CO2→CO→CO2变化(假定无损耗),再通入足量的澄清石灰水中,得到的沉淀为y克.则x与y的关系是( )A、x=y B、x>y C、x<y D、无法确定13. 现将10g A和足量B混合加热,A和B发生化学反应,10g A完全反应后生成8g C和4g D,则参加反应的A和B的质量比是( )A、1:1 B、2:1 C、4:1 D、5:114. 用一块棉布手帕浸泡在盛有质量分数约为70%的酒精溶液中,待均匀湿透后取出.将浸透的手帕舒展开,用镊子夹住两角,用火点燃(如图所示)当手帕上的火焰熄灭后,手帕完好无损.对于这一现象,下面解释正确的是( )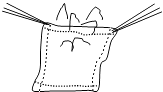 A、这是魔术,你所看到的是一种假象 B、火焰的温度低于棉布的着火点 C、手帕上的水和酒精的汽化吸热,使手帕的温度低于棉布的着火点 D、酒精燃烧后使棉布的着火点升高15. 下列各图所示装置的气密性检查中,漏气的是( )A、
A、这是魔术,你所看到的是一种假象 B、火焰的温度低于棉布的着火点 C、手帕上的水和酒精的汽化吸热,使手帕的温度低于棉布的着火点 D、酒精燃烧后使棉布的着火点升高15. 下列各图所示装置的气密性检查中,漏气的是( )A、 B、
B、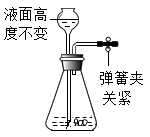 C、
C、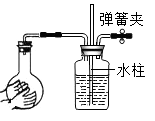 D、
D、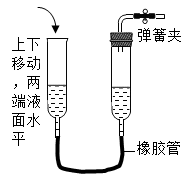 16. 如图所示,烧杯中盛有质量相等、质量分数相等的稀盐酸,天平调平后,同时向其中分别加入等质量的锌片和铁片,则从反应开始到金属完全反应的过程中,天平指针指向的变化是( )
16. 如图所示,烧杯中盛有质量相等、质量分数相等的稀盐酸,天平调平后,同时向其中分别加入等质量的锌片和铁片,则从反应开始到金属完全反应的过程中,天平指针指向的变化是( )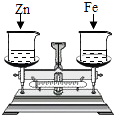 A、向左偏 B、向右偏 C、先向左偏后向右偏 D、先向右偏后向左偏17. 古代炼丹时经常使用红丹,又称铅丹.铅丹与硝酸发生如下反应“铅丹+4HNO3═PbO2+2Pb(NO3)2+2H2O”,则铅丹的化学式是( )A、PbO B、Pb3O4 C、Pb2O3 D、PbO218. 以下生活、学习经验,不能说明分子间有空隙的是( )A、打气筒将气体压缩 B、酒精和水混合后,总体积变小 C、物体有热胀冷缩现象 D、海绵能吸水19. 检验集气瓶中是否收集满CO2 , 正确的操作方法是( )A、倒入澄清的石灰水 B、用燃着的木条接近瓶口 C、把燃着的木条伸入瓶里 D、用带火星的木条接近瓶口20. 如图为某反应的微观示意图,不同的球代表不同元素的原子.下列说法中错误的是( )
A、向左偏 B、向右偏 C、先向左偏后向右偏 D、先向右偏后向左偏17. 古代炼丹时经常使用红丹,又称铅丹.铅丹与硝酸发生如下反应“铅丹+4HNO3═PbO2+2Pb(NO3)2+2H2O”,则铅丹的化学式是( )A、PbO B、Pb3O4 C、Pb2O3 D、PbO218. 以下生活、学习经验,不能说明分子间有空隙的是( )A、打气筒将气体压缩 B、酒精和水混合后,总体积变小 C、物体有热胀冷缩现象 D、海绵能吸水19. 检验集气瓶中是否收集满CO2 , 正确的操作方法是( )A、倒入澄清的石灰水 B、用燃着的木条接近瓶口 C、把燃着的木条伸入瓶里 D、用带火星的木条接近瓶口20. 如图为某反应的微观示意图,不同的球代表不同元素的原子.下列说法中错误的是( )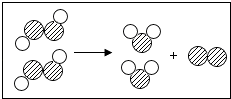 A、不考虑反应条件时,该图示可以表示双氧水制取氧气的反应 B、该反应的反应物可能属于氧化物 C、该反应类型为分解反应 D、该反应生成物都属于化合物21. 某金属A能与硫酸铜溶液发生置换反应但不能跟氯化锌溶液反应,关于A、铜和锌的金属活动性由强到弱排列正确的是( )A、Zn、A、Cu B、Zn、Cu、A C、A,Zn、Cu D、Cu、A,Zn22. 等质量的同一种稀硫酸分别与等质量且足量的镁、铁、锌发生反应,下图中能正确表示产生氢气的质量与反应时间之间关系的是( )A、
A、不考虑反应条件时,该图示可以表示双氧水制取氧气的反应 B、该反应的反应物可能属于氧化物 C、该反应类型为分解反应 D、该反应生成物都属于化合物21. 某金属A能与硫酸铜溶液发生置换反应但不能跟氯化锌溶液反应,关于A、铜和锌的金属活动性由强到弱排列正确的是( )A、Zn、A、Cu B、Zn、Cu、A C、A,Zn、Cu D、Cu、A,Zn22. 等质量的同一种稀硫酸分别与等质量且足量的镁、铁、锌发生反应,下图中能正确表示产生氢气的质量与反应时间之间关系的是( )A、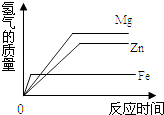 B、
B、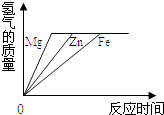 C、
C、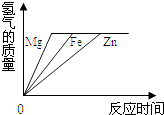 D、
D、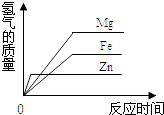
二、填空题
-
23. 用化学式或化学方程式填空:(1)、沼气的主要成分;(2)、铁丝浸入硫酸铜溶液中 .24. 下列各粒子符号中“2”的意义分别是:(1)、 O;(2)、Ca2+;(3)、O2;(4)、2N .25. 生活中处处有化学,请你用所学的化学知识来解释:(1)、在一些食品的包装袋中常装有干燥剂,有的干燥剂的成分是氧化钙,其干燥原理是(用化学方程式表示,下同) .(2)、实验室制取二氧化碳的反应原理 .26. 现有铜与另一种金属R(可能是银、镁、铁中的一种)的混合粉末.欲确定R的成分,请你一起完成:(1)、请将银、镁、铁三种金属的元素符号填写在下列金属活动性顺序表中的相应位置.
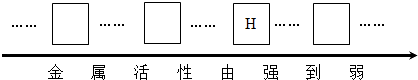 (2)、取少量的金属粉末于试管中,逐滴加入稀硫酸,有气泡产生,则R不可能是(3)、待不再产生气泡时,再进行(填写一种实验操作方法),得到溶液和铜.然后往溶液中加入洁净的锌片,锌片表面有金属析出,则R是 .(4)、写出金属R与稀硫酸反应的化学方程式 . 该反应的基本类型属于(选填“化合”、“分解”、“置换”或“复分解”)反应.27. 已知A、B为两种黑色粉末,D为红色金属.C、F都是无色气体,A、B、C、D、E、F五种物质之间的转化关系如图所示.(部分生成物已省略),请回答:
(2)、取少量的金属粉末于试管中,逐滴加入稀硫酸,有气泡产生,则R不可能是(3)、待不再产生气泡时,再进行(填写一种实验操作方法),得到溶液和铜.然后往溶液中加入洁净的锌片,锌片表面有金属析出,则R是 .(4)、写出金属R与稀硫酸反应的化学方程式 . 该反应的基本类型属于(选填“化合”、“分解”、“置换”或“复分解”)反应.27. 已知A、B为两种黑色粉末,D为红色金属.C、F都是无色气体,A、B、C、D、E、F五种物质之间的转化关系如图所示.(部分生成物已省略),请回答: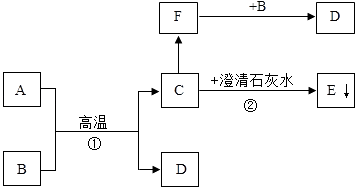 (1)、B的化学式为;D的化学式为 .(2)、反应②的化学方程式为;在上述反应中A、F都具有性.(3)、将两只用于医学研究的小白鼠分别放入盛放C、F的两个瓶中,拧紧瓶盖,结果两只小白鼠很快都死了.造成小白鼠死亡的主要原因(填“相同”或“不同”).28. 自来水消毒过程中通常会发生如下化学反应,其反应的微观过程可用图表示:
(1)、B的化学式为;D的化学式为 .(2)、反应②的化学方程式为;在上述反应中A、F都具有性.(3)、将两只用于医学研究的小白鼠分别放入盛放C、F的两个瓶中,拧紧瓶盖,结果两只小白鼠很快都死了.造成小白鼠死亡的主要原因(填“相同”或“不同”).28. 自来水消毒过程中通常会发生如下化学反应,其反应的微观过程可用图表示: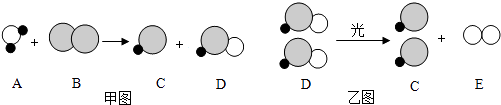
(
 表示氯原子,
表示氯原子,  表示氧原子,
表示氧原子,  表示氢原子)(1)、请写出甲图所示反应的化学方程式;(2)、乙图所示反应的基本反应类型为;(3)、上述物质中,属于单质的有(填化学式);(4)、D物质中氯元素的化合价为;(5)、以甲图为例分析,你能总结出的一条结论是
表示氢原子)(1)、请写出甲图所示反应的化学方程式;(2)、乙图所示反应的基本反应类型为;(3)、上述物质中,属于单质的有(填化学式);(4)、D物质中氯元素的化合价为;(5)、以甲图为例分析,你能总结出的一条结论是三、简答题
-
29. 用三种方法鉴别二氧化碳和一氧化碳.30. 请列举保护金属资源的有效途径三条.
四、实验与探究
-
31. 某兴趣小组的同学要用纯净干燥的一氧化碳测定由铜和氧化铜组成的混合物中氧化铜的质量,实验装置和实验数据如下.
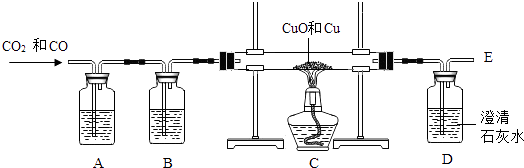 (1)、B装置中的试剂是 , 起作用..(2)、在E处应该点燃,因为 , 化学反应方程式
(1)、B装置中的试剂是 , 起作用..(2)、在E处应该点燃,因为 , 化学反应方程式C处玻璃管+样品的质量
D装置的总质量
反应前
158.2g
246.8g
反应后
156.6g
251.4g
(3)、根据C装置反应前后质量的变化,原混合物中氧元素的质量是 g,原混合物中氧化铜的质量是 g.(4)、根据D装置反应前后质量的变化,生成二氧化碳的质量是 g,原混合物中氧化铜的质量约是 g(结果保留一位小数).(5)、从(3)、(4)两小题中计算得出的氧化铜的质量不同,请分析原因可能 .32. 类比法是化学研究物质的重要方法之一.草酸(H 2C2O 4)的化学性质与碳酸相似,在受热条件下也会分解.某校研究性学习小组对此展开探究:(1)、小明首先根据草酸中含有元素,可推测生成物中含有水.(2)、小明对分解生成的其他产物进行猜测、验证:【假设一】生成物中有二氧化碳
实验一:将生成的气体通入 , 实验现象是 , 小明据此判断生成物中含有二氧化碳.
【假设二】生成物中有一氧化碳
实验二:小明用如图装段进行实验,从而证明生成物中含有一氧化碳.
请回答:A装置中红棕色固体粉末是 (填化学式),A装置中的实验现象是 , 请写出反应方程式: .
(3)、讨论交流:小芳认为,从环保的角度看,“实验二”装置有一个缺陷,请你指出该缺陷: , 处理的方法是 .(4)、根据上述探究结果,请写出草酸受热分解的方程式 .五、计算题
-
33. 某化工厂的金属废料主要成分是铜粉还含有铁粉,需回收此废料中的铜.现取废料样品10.0g,向其中加入足量的稀硫酸完全反应后(反应的化学方程式为:Fe+H2SO4=FeSO4+H2↑)共收集到0.1g 氢气.试求:(1)、废料中铜的质量分数为多少?(2)、现有废料20.0t,共可回收铜的质量为多少?