安徽省宿州市砀山县2017-2018学年九年级上学期化学期末考试试卷
试卷更新日期:2018-11-06 类型:期末考试
一、单选题
-
1. 为纪念化学所取得的成就以及对人类文明的贡献,联合国将2011年定为“国际化学年”。下列活动中,通过化学反应提供能量的是( )
A、 发射火箭
B、
发射火箭
B、 水车汲水灌溉
C、
水车汲水灌溉
C、 太阳能供热
D、
太阳能供热
D、 风力发电
2. 我国航天员成功完成了太空漫步。为解决航天员的呼吸问题,舱外航天服应能提供的物质是( )A、氮气 B、二氧化碳 C、氧气 D、水3. 下列属于纯净物的是
风力发电
2. 我国航天员成功完成了太空漫步。为解决航天员的呼吸问题,舱外航天服应能提供的物质是( )A、氮气 B、二氧化碳 C、氧气 D、水3. 下列属于纯净物的是
A、加碘食盐 B、硬水 C、干冰 D、食醋4. 下列方法可以鉴别空气、氧气、二氧化碳三种气体的是( )A、插入燃烧着的木条 B、闻气体的气味 C、观察气体的颜色 D、倒入澄清的石灰水5. 下列物质不属于空气污染物的是( )A、粉尘 B、二氧化硫 C、氮氧化物 D、二氧化碳6. 工业用盐中含有亚硝酸钠(NaNO2).亚硝酸钠是一种有一种有毒的物质,其中亚硝酸钠中氮元素的化合价是( )A、+5 B、+3 C、+2 D、+47. 下图是元素周期表中硫元素的信息示意图,对图中信息理解错误的是( ) A、原子序数 B、元素名称 C、元素符号 D、中子数8. 大蒜中含有一种有效成分辣素“硫化丙烯”,其化学式为C3H6S,能杀菌,具有一定的抗病功能和食疗价值.下列关于硫化丙烯的说法中正确的是( )A、1个硫化丙烯分子中含有3个氢分子 B、1个硫化丙烯分子由3个碳原子、6个氢原子、1个硫原子构成 C、硫化丙烯由碳、氢、氧三种元素组成 D、硫化丙烯分子中C,H元素原子质量比为9:89. 工业上常用乙炔燃烧产生的高温火焰来切割金属。若用R表示乙炔,其燃烧的化学方程式 ,则乙炔的化学式是( )A、C2H4 B、C2H2 C、CH3COOH D、C2H610. 下图中实验操作正确的是( )A、
A、原子序数 B、元素名称 C、元素符号 D、中子数8. 大蒜中含有一种有效成分辣素“硫化丙烯”,其化学式为C3H6S,能杀菌,具有一定的抗病功能和食疗价值.下列关于硫化丙烯的说法中正确的是( )A、1个硫化丙烯分子中含有3个氢分子 B、1个硫化丙烯分子由3个碳原子、6个氢原子、1个硫原子构成 C、硫化丙烯由碳、氢、氧三种元素组成 D、硫化丙烯分子中C,H元素原子质量比为9:89. 工业上常用乙炔燃烧产生的高温火焰来切割金属。若用R表示乙炔,其燃烧的化学方程式 ,则乙炔的化学式是( )A、C2H4 B、C2H2 C、CH3COOH D、C2H610. 下图中实验操作正确的是( )A、 读取液体体积
B、
读取液体体积
B、 过滤
C、
过滤
C、 倾倒液
D、
倾倒液
D、 制取二氧化碳
11. 2016年1月,中科院兰州化学物理研究所科研人员研究开发了一套具有超强水处理净化能力的装置,下列关于水的净化的说法,错误的是( )
制取二氧化碳
11. 2016年1月,中科院兰州化学物理研究所科研人员研究开发了一套具有超强水处理净化能力的装置,下列关于水的净化的说法,错误的是( )
A、活性炭可除去水中的异味 B、过滤可以除去水中所有的杂物 C、硬水通过煮沸可降低硬度 D、蒸馏对水的净化程度比较高12. 下列对实验现象描述正确的是( )A、木炭在氧气中燃烧,发白光,生成黑色固体 B、硫在氧气中燃烧,火焰呈蓝紫色,放出有刺激性气味的气体 C、红磷在空气中燃烧,产生白雾 D、铁丝在氧气中燃烧,火星四射,生成四氧化三铁13. 物质的性质决定了物质的用途.下列几种常见的物质的性质、用途不一致的是( )
A、金刚石硬度大﹣﹣用于裁玻璃 B、氮气性质稳定﹣﹣作保护气 C、酒精可燃﹣﹣作消毒剂 D、干冰升华吸热﹣﹣用于人工降雨14. 关于碳的单质的组成和用途的说法错误的是( )
A、用铅笔芯的粉末可以使锁的开启变的灵活 B、璀璨夺目的天然钻石是由碳元素组成的 C、活性炭可用作防毒面具的滤毒剂 D、铅笔芯主要用铅和少量碳粉制成15. 2016 年 4 月 15 日是我国首个“全民国家安全教育日”.下列说法中,正确的是( )A、冬天室内用煤炉取暖要严防煤气中毒 B、汽车油箱着火,可以用水浇灭 C、发现厨房天然气泄露,打开抽油烟机排气 D、室内起火,迅速打开所有门窗通风16. 最近科学家发现,无定形碳在利用单脉冲激光冲激下生成Q─碳,硬度比钻石还高。下列关于这种“Q─碳”的说法错误的是( )
A、化学性质与普通碳单质相同 B、Q─碳中原子间没有间隔 C、碳原子的排列方式不同于金刚石 D、Q─碳中原子仍然在不断运动17. 某同学在研究物质燃烧的条件时,做了如图所示的实验:把一条粗金属丝绕成线圈,罩在一支蜡烛的火焰上,火焰很快就熄灭了.对这一实验的说法错误的是( ) A、金属丝有良好的导热性 B、金属线圈内的气体温度升高了 C、可燃物的温度降到了着火点以下 D、若预先将金属丝加热,蜡烛就不会很快熄灭18. 下列现象或事实,用分子的相关知识解释错误的是( )
A、金属丝有良好的导热性 B、金属线圈内的气体温度升高了 C、可燃物的温度降到了着火点以下 D、若预先将金属丝加热,蜡烛就不会很快熄灭18. 下列现象或事实,用分子的相关知识解释错误的是( )
A、水和水蒸气化学性质相同,是因为分子构成相同 B、氧化汞受热分解生成汞和氧气,说明在化学变化中分子可以再分 C、石油气加压后可贮存在钢瓶中,说明分子之间有间隙 D、水沸腾时可掀起壶盖,说明分子大小随温度升高而增大19. 在C+O2 CO2的反应中,反应前后肯定发生变化的是( )
A、元素的种类 B、原子的种类、数目和质量 C、反应前和反应后物质的质量总和 D、各元素的化合价20. 在锥形瓶甲中放入10g块状纯净的碳酸钙,在锥形瓶乙中放入10g粉末状纯净的碳酸钙,分别同时加入等质量、同浓度的稀盐酸(足量).如图中对该实验产生气体的质量与反应时间的关系,描述合理的是( )A、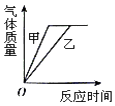 B、
B、 C、
C、 D、
D、
二、填空题
-
21.(1)、化学用语能准确简洁地记录、表达、交流化学信息,请你用正确的化学用语填空:
①2个氮原子;
②过氧化氢中氧元素的化合价为﹣1价;
③地壳中含量最多的金属元素;
④保持水的化学性质的最小微粒
(2)、化学就在我们身边,它与我们的生活息息相关,请从A、氢气 B、氧气 C、二氧化碳 D、一氧化碳 E、金刚石 F、甲烷 G、活性炭这几种物质中,选择适当的字母序号填空。①干冰时固体的 , 可用于人工降雨;
②冬天燃煤取暖时,应注意室内通风,防止“煤气”中毒,“煤气”指的是
③最清洁的能源;
④天然气的主要成分是
⑤安在玻璃刀上的划玻璃;
⑥冰箱除臭剂
三、简答题
-
22. 在宏观、微观和符号之间建立联系,是化学学科的特点,如图是某化学反应的微观过程示意图1(“
 ”表示氧原子,“
”表示氧原子,“  ”表示氢原子)
”表示氢原子) (1)、从宏观角度看,物质B属于(选填“单质”或“化合物”)(2)、从微观角度看,物质A是由构成的(选填“分子”或“原子”或“离子”)(3)、参加反应的A与B的粒子个数比为(4)、从图你可以得出的正确结论是(填序号)
(1)、从宏观角度看,物质B属于(选填“单质”或“化合物”)(2)、从微观角度看,物质A是由构成的(选填“分子”或“原子”或“离子”)(3)、参加反应的A与B的粒子个数比为(4)、从图你可以得出的正确结论是(填序号)①分子是由原子构成的 ②化学反应中,分子可以分成原子,原子不能再分 ③反应前后分子种类不变
(5)、请写出能用该图示表示的化学方程式(6)、如下图中钠元素在元素周期表中的相关信息,B是钠原子结构示意图。
①钠的相对原子质量为;
②钠元素属于元素(选填“金属”或“非金属”)
③钠原子在化学反应中容易电子(选填“得到”或“失去”)
23. 今年入冬以来,我国北方大部分地区遭遇几十年未见的特大旱灾,缓解灾情,有些地区使用了干冰进行人工增雨,但二氧化碳也是温室效应的元凶之一因此,有科学家设想:将排放到空气中的二氧化碳压缩使其液化,然后将其压入到冰的深海中,但也有科学家担心海水中富含二氧化碳后酸度会增加,可能会杀死一些海生物,甚至会溶解掉部分海床,从而造成灾难性的后果。
(1)、为减少二氧化碳这种温室气体的排放,我们可以采取的措施有:。(写一种即可)(2)、二氧化碳使海水酸度增加的原理用化学方程式表示为:;(3)、能用来鉴别CO和CO2的方法是_____(不定项选择)。A、通入紫色石蕊试液 B、通入澄清石灰水 C、闻气味(4)、为减少大气中二氧化碳含量,将过多的二氧化碳和氢气在催化剂和加热的条件下反应,转化为水和甲烷(CH4)这个反应的化学方程式为。24. 水是生命的源泉,也是不可缺少的资源。
(1)、某矿泉水的主要矿物质成分及含量如表:成分
Ca
K
Zn
F
含量(mg/L)
20
3
0.06
0.02
这里Ca、K、Zn、F是指 (填“单质、元素、分子或原子”)。
(2)、水污染日益严重,水资源的保护和合理利用已受到人们的普遍关注。请参与讨论下列有关问题:(Ⅰ)检验某地下水是硬水还是软水,可用的物质是;实验室常用的方法来降低水的硬度
(Ⅱ)某学校饮水处可以将自来水净化为饮用水,其中处理步骤如图所示:

①对应的作用是(填字母序号)③对应的作用是。
A.杀菌消毒
B.吸附杂质
C.沉淀过滤
D.蒸馏
(Ⅲ)下列做法会造成水体污染的有。
A.工业废水直接排放
B.工业废气处理后排放
C.禁止使用含磷洗衣粉
D.大量使用化肥、农药
四、综合题
-
25. 请根据如图A、B所示的化学实验(装置B铁架台已略去),回答以下问题。
 (1)、装置A中,对比现象①③说明燃烧需要条件;实验中水在其中的作用是、。(2)、装置B是二氧化碳的制备和性质实验。实验进行一段时间后,“人”字管右端可以观察到的现象是 , 该反应的化学方程式为。(3)、装置B的干燥管中被石蕊溶液浸湿的纸质小花的颜色变化为。26. 下列装置可制取有关气体,请回答
(1)、装置A中,对比现象①③说明燃烧需要条件;实验中水在其中的作用是、。(2)、装置B是二氧化碳的制备和性质实验。实验进行一段时间后,“人”字管右端可以观察到的现象是 , 该反应的化学方程式为。(3)、装置B的干燥管中被石蕊溶液浸湿的纸质小花的颜色变化为。26. 下列装置可制取有关气体,请回答 (1)、仪器a、b的名称是:a;b;(2)、实验室用高锰酸钾制取氧气的化学方程式为 , 该反应的基本反应类型是(填“分解”或“化合”)反应;如用E装置收集氧气,当观察到时,再把导管口伸入盛满水的集气瓶中。(3)、实验室制取二氧化碳的化学方程式为 , 应选用的收集装置是(4)、如图装置可用来测量生成的O2的体积,检验该装置气密性的方法是:当把针筒里的活塞内推时,若看到 , 说明气密性良好。
(1)、仪器a、b的名称是:a;b;(2)、实验室用高锰酸钾制取氧气的化学方程式为 , 该反应的基本反应类型是(填“分解”或“化合”)反应;如用E装置收集氧气,当观察到时,再把导管口伸入盛满水的集气瓶中。(3)、实验室制取二氧化碳的化学方程式为 , 应选用的收集装置是(4)、如图装置可用来测量生成的O2的体积,检验该装置气密性的方法是:当把针筒里的活塞内推时,若看到 , 说明气密性良好。 27. 某兴趣小组在制取氧气的实验过程中,有同学联想到了渔民用过氧化钙(CaO2)增加鱼池中的含氧量,于是做出猜想:过氧化钙与水反应可制取氧气。
27. 某兴趣小组在制取氧气的实验过程中,有同学联想到了渔民用过氧化钙(CaO2)增加鱼池中的含氧量,于是做出猜想:过氧化钙与水反应可制取氧气。实验装置
实验主要过程

①检查装置气密性。
②加入过氧化钙和水后,有少量细小气泡缓慢放出,在导管口几乎收集不到气体。该装置放置到第二天,集气瓶中只收集到极少量气体,震荡试管后仍有少量细小气泡缓慢放出。
(1)、实验结论:过氧化钙与水反应(填“能”或“不能”)用于实验室制取氧气。(2)、【分析与反思】小林希望对此实验进行改进,使该反应加快,请你帮他提出合理化建议。
(3)、同学们对过氧化钙与水反应的生成物猜想如下:①氢氧化钙和氧气②碳酸钙和氧气。你认为猜想(填序号)一定是错误的,理由是五、计算题
-
28. 以CO2和NH3合成尿素CO(NH2)2是固定和利用CO2的成功范例,该反该反应的化学方程式为CO2+2NH3=CO(NH2)2+H2O.请计算:若按上述方法生产120t尿素,可固定的CO2的质量为多少.
-