2016-2017学年山东省潍坊市诸城市九年级上学期期末化学试卷
试卷更新日期:2017-03-16 类型:期末考试
一、选择题
-
1. 下列变化属于化学变化的是:①电灯通电发光②煤制成焦炭③干冰升华④石油分馏⑤烧制瓷器⑥铁钉生锈⑦用氢氧化钙配制澄清石灰水⑧粮食酿酒( )A、①⑤⑥⑦ B、②④⑤⑥ C、②⑤⑥⑧ D、①④⑥⑧2. 下列实验操作中错误的是( )A、
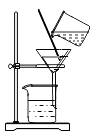 过滤
B、
过滤
B、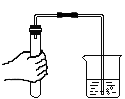 检查装置气密性
C、
检查装置气密性
C、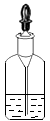 滴管用毕即插回
D、
滴管用毕即插回
D、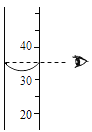 量取一定体积的液体
3. 砷化镓(GaAs)是一种“LED”绿色节能光源材料,镓元素的相关信息如图.下列有关镓的说法错误的是( )
量取一定体积的液体
3. 砷化镓(GaAs)是一种“LED”绿色节能光源材料,镓元素的相关信息如图.下列有关镓的说法错误的是( )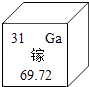 A、原子的核电荷数是31 B、元素符号是Ga C、属于金属元素 D、相对原子质量为69.72g4. 下列图象分别与各选项中的说法相对应(图中○和●分别表示不同的原子),其中不正确的是( )A、
A、原子的核电荷数是31 B、元素符号是Ga C、属于金属元素 D、相对原子质量为69.72g4. 下列图象分别与各选项中的说法相对应(图中○和●分别表示不同的原子),其中不正确的是( )A、 可能是氧化物
B、
可能是氧化物
B、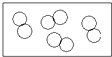 可能是金属
C、
可能是金属
C、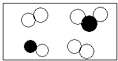 一定是混合物
D、
一定是混合物
D、 包含组成元素相同的不同物质
5. 下列关于物质性质及用途的描述中,错误的是( )A、氧气具有氧化性,可作为燃料 B、碳具有还原性,可冶炼金属 C、氮气的化学性质稳定,可作为保护气 D、石灰石受热分解,可用于制备生石灰6. 中国科学院某研究小组设计了一种高性能锂空气电池,其反应原理可表示为:2Li+O2 Li2O2 , 已知锂元素在化合物中显+1价,下列说法错误的是( )A、反应物锂是金属单质 B、该反应中MnO2是催化剂 C、Li2O2中氧元素的化合价显﹣2价 D、该反应是化合反应7. 2022年北京、张家口将联合举办冬奥会,为办成绿色奥运会,下列措施不可行的是( )A、将纸质垃圾焚烧处理 B、增加使用太阳能,核能等新能源 C、废旧电池集中回收处理 D、改进燃煤技术,减少SO2与粉尘排放8. 下列物质或方式中的“碳”,主要不是针对碳单质的是( )A、低碳生活 B、打印碳粉 C、碳素墨水 D、石墨碳棒9. 下列与水有关的说法错误的是( )A、活性炭可以除去水中的异味和色素 B、肥皂水可以使硬水软化 C、电解水时在负极得到氢气 D、水分子是由氢原子和氧原子构成10. 下列关于金属的说法正确的是( )A、铁是地壳中含量最高的金属元素 B、铜的性能优良,是很纯的铁 C、铁制品生锈产生的铁锈是一种疏松多孔的物质,它的主要成分是Fe3O4 D、波尔多液不可以在铁制容器中配制
包含组成元素相同的不同物质
5. 下列关于物质性质及用途的描述中,错误的是( )A、氧气具有氧化性,可作为燃料 B、碳具有还原性,可冶炼金属 C、氮气的化学性质稳定,可作为保护气 D、石灰石受热分解,可用于制备生石灰6. 中国科学院某研究小组设计了一种高性能锂空气电池,其反应原理可表示为:2Li+O2 Li2O2 , 已知锂元素在化合物中显+1价,下列说法错误的是( )A、反应物锂是金属单质 B、该反应中MnO2是催化剂 C、Li2O2中氧元素的化合价显﹣2价 D、该反应是化合反应7. 2022年北京、张家口将联合举办冬奥会,为办成绿色奥运会,下列措施不可行的是( )A、将纸质垃圾焚烧处理 B、增加使用太阳能,核能等新能源 C、废旧电池集中回收处理 D、改进燃煤技术,减少SO2与粉尘排放8. 下列物质或方式中的“碳”,主要不是针对碳单质的是( )A、低碳生活 B、打印碳粉 C、碳素墨水 D、石墨碳棒9. 下列与水有关的说法错误的是( )A、活性炭可以除去水中的异味和色素 B、肥皂水可以使硬水软化 C、电解水时在负极得到氢气 D、水分子是由氢原子和氧原子构成10. 下列关于金属的说法正确的是( )A、铁是地壳中含量最高的金属元素 B、铜的性能优良,是很纯的铁 C、铁制品生锈产生的铁锈是一种疏松多孔的物质,它的主要成分是Fe3O4 D、波尔多液不可以在铁制容器中配制二、选择题
-
11. 下列说法中正确的是( )A、生物体中含量较多的前四种元素是氧、碳、氢、氮 B、氯化钠固体中混有少量硝酸钾固体,可用降温结晶的方法除去硝酸钾 C、NaOH和NaCl两种固体溶于水都会使溶液温度升高 D、饱和石灰水露置一段时间表面形成一层白膜(若水没有减少),该溶液仍是氢氧化钙的饱和溶液12. 2016年10月17日,神舟十一号载人飞船发射成功,飞行期间,将验证货物运输和推进剂在轨补加,10月19日凌晨,神舟十一号飞船与天宫二号自动交会对接成功,推进剂可分固体和液体两大类,其中硝酸甲酯是一种液体推进剂,化学式为CH3NO3 , 下列关于硝酸甲酯的说法正确的是( )A、硝酸甲酯属于氧化物 B、硝酸甲酯中碳、氢、氮、氧四种元素的质量比为12:3:14:48 C、硝酸甲酯是由8个原子构成的 D、硝酸甲酯中碳元素的质量分数最高13. 根据下列实验方案进行实验,能达到相应实验目的是( )A、
 比较Zn和Fe的金属活动性强弱
B、
比较Zn和Fe的金属活动性强弱
B、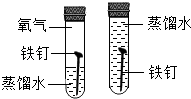 探究铁钉生锈时O2是否参与反应
C、
探究铁钉生锈时O2是否参与反应
C、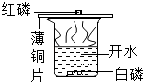 比较红磷和白磷的着火点
D、
比较红磷和白磷的着火点
D、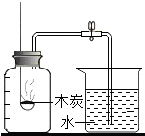 测定空气中O2的含量
14. 某有机物6.0g在空气中完全燃烧,共得到17.6g二氧化碳和10.8g水,则该化合物的组成元素是( )A、一定只含有碳元素 B、一定只含有碳、氢两种元素 C、一定含有碳、氢、氧三种元素 D、一定含有碳、氢元素,可能含有氧元素15. 已知:“
测定空气中O2的含量
14. 某有机物6.0g在空气中完全燃烧,共得到17.6g二氧化碳和10.8g水,则该化合物的组成元素是( )A、一定只含有碳元素 B、一定只含有碳、氢两种元素 C、一定含有碳、氢、氧三种元素 D、一定含有碳、氢元素,可能含有氧元素15. 已知:“ ”“
”“  ”“
”“  ”分别代表不同种元素的原子,两种物质在一定条件下能发生化学反应,用微观示意图表示为:则下列说法正确的是( )
”分别代表不同种元素的原子,两种物质在一定条件下能发生化学反应,用微观示意图表示为:则下列说法正确的是( ) 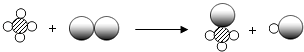 A、如图所示中的反应物都是单质 B、该反应属于置换反应 C、如图所示中共有3种化合物分子 D、该图所示变化过程中原子发生了变化16. 甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )
A、如图所示中的反应物都是单质 B、该反应属于置换反应 C、如图所示中共有3种化合物分子 D、该图所示变化过程中原子发生了变化16. 甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )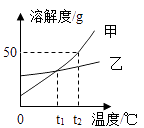 A、甲物质的溶解度大于乙物质的溶解度 B、t1℃时,甲、乙两物质的溶解度相等 C、t2℃时,乙的饱和溶液降温至t1℃,乙溶液变为不饱和溶液 D、t2℃时,甲物质的饱和溶液降温至t2℃,溶液中溶质质量分数不变17. 下列图象分别与选项中的实验现象及结果相对应,其中正确的是( )A、
A、甲物质的溶解度大于乙物质的溶解度 B、t1℃时,甲、乙两物质的溶解度相等 C、t2℃时,乙的饱和溶液降温至t1℃,乙溶液变为不饱和溶液 D、t2℃时,甲物质的饱和溶液降温至t2℃,溶液中溶质质量分数不变17. 下列图象分别与选项中的实验现象及结果相对应,其中正确的是( )A、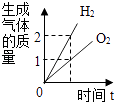 电解水
B、
电解水
B、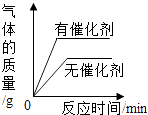 等体积、等溶质质量分数的过氧化氢溶液制取氧气
C、
等体积、等溶质质量分数的过氧化氢溶液制取氧气
C、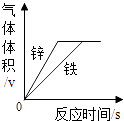 将等质量的锌和铁分别投入到盛有足量同种稀硫酸的两个容器中
D、
将等质量的锌和铁分别投入到盛有足量同种稀硫酸的两个容器中
D、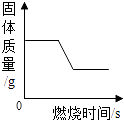 煅烧石灰石
18. 下列客观事实的微观解释正确的是( )
煅烧石灰石
18. 下列客观事实的微观解释正确的是( )选项
客观事实
微观解释
A
搅拌能加快蔗糖在水中的溶解
搅拌使蔗糖分子在水中溶解更多
B
品红在热水中扩散更快
水分子间有空隙
C
湿衣服在阳光下晾晒变干
水分子受热变成了氧分子和氢分子
D
H2O在通电条件下产生H2
水分子中含有氢原子
A、A B、B C、C D、D19. 推理和归纳是化学学习和研究中常用的思维方法,下列推理正确的是( )A、稀有气体可作保护气,可作保护气的一定是稀有气体 B、单质是由一种元素组成的物质,由一种元素组成的物质一定是单质 C、物质都是由元素组成的,同种元素可以组成纯净物,不同种元素也可以组成纯净物 D、性质活泼的金属在空气中易被腐蚀,铅在空气中不易被腐蚀是因为其性质不活泼20. 用实验探究Al和Cu的金属活动性强弱.若提供的试剂只有:CuCl2溶液、AlCl3溶液、Al、Cu和稀盐酸.对此下列说法正确的是( )A、最多只能设计一种实验方案 B、CuCl2溶液是不可或缺的试剂 C、选用两种合适的试剂即可实现实验目的 D、AlCl3溶液中加入Cu不能探究金属活动性强弱三、综合题
-
21. 请沿用科学家认识事物的方式认识“空气”.(1)、从分类的角度:空气属于(填“混合物”或“纯净物”).(2)、从微观的角度,用“
 ”表示氮原子,“
”表示氮原子,“  ”表示氧原子.
”表示氧原子. ①用“
 ”可表示的微粒是(填名称).
”可表示的微粒是(填名称).②如图1(氧原子结构示意图)获得的信息,正确的是(填标号).
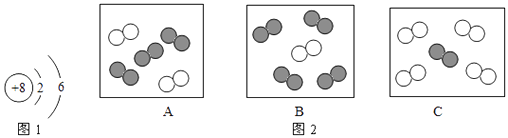
a.表示原子核,带8个单位正电荷
b.氧原子核外有2个电子层,有8个电子在核外作高速运动
c.氧原子在化学反应中易失去电子形成离子(O2﹣)
③同温同压下,气体的体积比等于分子数目比,若空气中其他成分忽略不计,如图2可表示空气微观模型的是(填序号).
(3)、从变化的角度:已知:常压下,氮气沸点﹣196℃,氧气的沸点﹣183℃.将燃着的木条置于盛满液态空气的烧杯口,观察到的现象是 . 该烧杯放置一段时间后,液态物质剩余约 体积,其主要成分是(4)、从环保角度,下列保护空气措施合理的有 (填标号)A、工厂通过加高烟囱直接排放废气 B、推广使用乙醇汽油代替普通汽油 C、提倡步行,骑自行车等“低碳”出行方式.22. 2015年第21届联合国气候变化大会的核心议题是碳排放及全球气候变暖.(1)、自然界中二氧化碳的消耗主要有以下两个过程:①绿色植物光合作用吸收二氧化碳和水生成葡萄糖(C6H12O6)和氧气.②自然界中的水体吸收二氧化碳生成碳酸.从物质转化的角度看,上述两个反应的反应物相同,而产物却完全不同,其原因是 . 光合作用的化学方程式是 .(2)、二氧化碳可被压缩成液态,封存在地质结构中.从微观角度解释二氧化碳能够压缩成液态的原因是 . 如果CO2被封存在含氢氧化钙的地下咸水层中,则可转化为固态碳酸盐,该反应的化学方程式是 .(3)、科学家利用太阳能可将二氧化碳和水转化为“合成气”(H2和CO的混合气体).用“合成气”为原料生产甲醇(CH4O)时,按照“绿色化学”原则,应调节“合成气”中H2和CO的分子个数比为23. A、B、C三种固体物质的溶解度曲线如图所示,据图回答问题.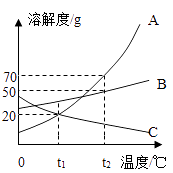 (1)、t1℃时,A、B、C三种物质的溶解度由大到小的顺序为 .(2)、当A物质中混有少量B时,可用(填“降温结晶”或“蒸发结晶”)方法提纯A;(3)、将t1℃时A,B,C三种物质的饱和溶液升温到t2℃,没有晶体析出的是(填字母代号);(4)、t1℃时,将30gA物质放入盛有100g水的烧杯中,最终所得溶液的质量为 . 若将烧杯内物质升温到t2℃时(不考虑水蒸发),溶液中不变的是(填序号);
(1)、t1℃时,A、B、C三种物质的溶解度由大到小的顺序为 .(2)、当A物质中混有少量B时,可用(填“降温结晶”或“蒸发结晶”)方法提纯A;(3)、将t1℃时A,B,C三种物质的饱和溶液升温到t2℃,没有晶体析出的是(填字母代号);(4)、t1℃时,将30gA物质放入盛有100g水的烧杯中,最终所得溶液的质量为 . 若将烧杯内物质升温到t2℃时(不考虑水蒸发),溶液中不变的是(填序号);A溶剂的质量 B溶液的质量 C.溶质的质量分数 D.以上都不变
(5)、t2℃时,把A、B物质各30g加到50g水中,不能形成饱和溶液的是(填字母代号),若要使之达到饱和状态,还需要向溶液中加入 g该溶质.24. 我国古代将炉甘石(主要成分:ZnCO3)、赤铜矿(主要成分:Cu2O)和木炭粉为原料制得了黄铜(铜和锌的合金,外观似黄金),其生产流程如下: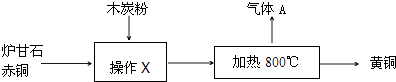
回答下列问题:
(1)、赤铜矿中铜元素的化合价 .(2)、黄铜的硬度比铜和锌都(填“大”或“小”)(3)、加热时,发生的主要反应化学方程式为:①ZnCO3 ZnO+CO;②2ZnO+C 2Zn+CO2↑;
③(赤铜和木炭粉反应).
(4)、气体A中,除二氧化碳外还有另一种生成气体,它的化学式是 , 该气体的一种用途是(用化学方程式表示).(5)、鉴别黄铜和黄金有多种方法,用灼烧法鉴别产生的现象及结论是 .四、探究题
-
25. 如图是初中化学常见气体的发生和收集装置,请根据要求回答下列问题:
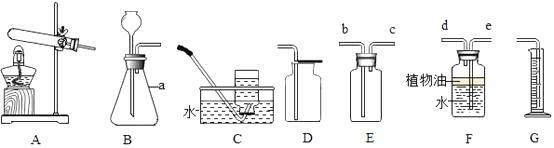 (1)、仪器a的名称是 .(2)、实验室制取二氧化碳所选用的发生装置是(填序号),若用F和G装置连接测量生成的二氧化碳体积,气体应从(选填“d”或“c”)端通入,广口瓶内有一定量空气对测量结果是否有影响(填“有”或“无”),在水面上放一层植物油的目的是 .(3)、实验室用过氧化氢溶液和二氧化锰混合制取氧气反应的化学方程式为: . 用E装置收集氧气时,气体应从(选填“b”或“c”)端通入,用C装置收集氧气时,观察到导管口的气泡 , 再把导管口伸入盛满水的集气瓶.(4)、若用氯酸钾和二氧化锰制取氧气,并进行铁丝燃烧的实验,选用最佳的制取装置组合为(填序号).26. 久置的铜制品表面能生成绿色的铜锈[主要成分为Cu2(OH)2CO3],某化学兴趣小组对铜生锈的条件进行了以下探究.
(1)、仪器a的名称是 .(2)、实验室制取二氧化碳所选用的发生装置是(填序号),若用F和G装置连接测量生成的二氧化碳体积,气体应从(选填“d”或“c”)端通入,广口瓶内有一定量空气对测量结果是否有影响(填“有”或“无”),在水面上放一层植物油的目的是 .(3)、实验室用过氧化氢溶液和二氧化锰混合制取氧气反应的化学方程式为: . 用E装置收集氧气时,气体应从(选填“b”或“c”)端通入,用C装置收集氧气时,观察到导管口的气泡 , 再把导管口伸入盛满水的集气瓶.(4)、若用氯酸钾和二氧化锰制取氧气,并进行铁丝燃烧的实验,选用最佳的制取装置组合为(填序号).26. 久置的铜制品表面能生成绿色的铜锈[主要成分为Cu2(OH)2CO3],某化学兴趣小组对铜生锈的条件进行了以下探究.【提出猜想】根据铜锈的组成元素推测,铜生锈可能是铜与空气中的二氧化碳、水等物质反应的结果.
【实验设计】兴趣小组同学取打磨光量的铜丝,设计了如图所示的四个实验.
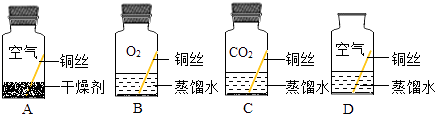 (1)、【现象分析】若干天后,发现只有D瓶中的铜丝出现绿色的铜锈,其他瓶中的铜丝均无铜锈出现.
(1)、【现象分析】若干天后,发现只有D瓶中的铜丝出现绿色的铜锈,其他瓶中的铜丝均无铜锈出现.①实验B、C瓶中所使用的蒸馏水是经煮沸后迅速冷却的蒸馏水,其目的是 .
②B瓶与D瓶中的现象对比,可以得出的结论是
(2)、【实验结论】由上述四个实验可分析得出,铜生锈是铜与空气中的共同作用的结果.(3)、【拓展探究】以锈蚀严重的废铜屑为原料,回收制取纯铜.查阅资料:Cu2(OH)2CO3+2H2SO4═2CuSO4+3H2O+CO2↑
Cu2(OH)2CO3 2CuO+H2O+CO2↑
如图是该兴趣小组设计的两种回收铜的实验方案:
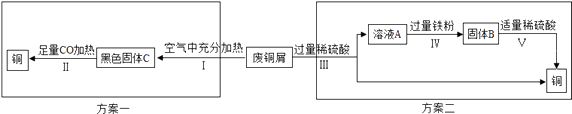
【分析评价】①步骤Ⅱ反应过程中发生了还原反应的物质是(填化学式).
②步骤Ⅲ、Ⅳ、Ⅴ都需要进行的实验操作是 .
③步骤Ⅴ过程发生反应的化学方程式为 .
④同一份废铜屑分别通过上述两种方案最终得到的铜的质量:方案一(填“>”或“=”或“<”)方案二.以上两种方案中,方案二优越于方案一,理由是(任答一点).
五、计算题
-
27. 某兴趣小组为探究铝镁合金的组成,取16g铝镁合金样品,将60g氢氧化钠溶液平均分成三份依次加入样品中(镁与氢氧化钠溶液不反应,铝与氢氧化钠溶液反应的化学方程式为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑),充分反应后,过滤出固体,将其洗涤、干燥、称量,得实验数据如下:计算:
所加氢氧化钠溶液的次数
第一次
第二次
第三次
所加氢氧化钠溶液的质量/g
20
20
20
剩余固体的质量/g
10.6
5.2
4.0
(1)、该合金中,铝元素与镁元素的质量比为 .(2)、所用氢氧化钠溶液中溶质的质量分数.