浙江省嘉兴市2018-2019学年九年级上学期科学教学质量检测(一)
试卷更新日期:2018-11-02 类型:月考试卷
一、选择题
-
1. 下列各组内物质名称表示同一种物质是( )A、氢氧化钠 烧碱 苛性钠 B、氢氧化钙 消石灰 生石灰 C、盐酸 氯化氢 食盐 D、冰 干冰 水2. 用碱性溶液浸泡蔬菜能有效除去蔬菜上的残留农药,从而降低对人体的损害,学校食堂从市场上买回来的蔬菜,你认为应浸泡在( )
A、食盐溶液 B、烧碱溶液 C、纯碱溶液 D、食醋溶液3. 固体氢氧化钠和氧化钙的混合物叫做碱石灰,常用作干燥剂。下列气体不能用碱石灰干燥的是( )A、CO B、CO2 C、H2 D、O24. 下列肥料中含营养元素种类最少的是( )A、K2SO4 B、(NH4)2HPO4 C、NH4H2PO4 D、KNO35. 盐酸是一种重要的酸,下列关于盐酸的性质、用途及检验的说法正确的是( )A、稀盐酸能与锌、铁、铜等许多金属反应 B、稀盐酸常用于去除金属锈蚀及水垢 C、浓盐酸瓶盖打开时可观察到冒白烟现象 D、能与硝酸银溶液反应生成白色沉淀的是盐酸6. 氢氧化钾与氢氧化钠都是常见的碱,有一些相似的化学性质。下列有关氢氧化钾的说法正确的是( )A、氢氧化钾固体露置在空气中易变质 B、氢氧化钾溶液能使石蕊溶液变红 C、氢氧化钾溶液与氧化铜反应生成蓝色沉淀 D、2mL 氢氧化钾溶液与 1mL 硫酸溶液恰好完全反应7. “五水共治”是指治污水、防洪水、排涝水、保供水、抓节水,某造纸厂因违规排放废水被相关部门责令关停、整改,经测定该厂废水的 pH=1,则在该废水中还能大量检测出的离子可能是( )A、Ag+、 、Cl-、Na+ B、OH-、K+、 、Ba2+ C、Mg2+、 、Al3+、 D、Na+、 、Ca2+、Cl-8. 不用指示剂,将含有盐酸的氯化钙溶液由酸性变为中性,应选用的试剂是( )A、澄清石灰水 B、硝酸银溶液 C、生石灰粉末 D、石灰石9. 从微观构成方面来看,稀盐酸、稀硫酸中因为含有相同的某种微粒而具有相似的化学性质,下列变化不能体现不同酸溶液相似的化学性质的是( )A、稀盐酸能与碳酸盐反应产生二氧化碳 B、稀盐酸能使紫色石蕊溶液变红色 C、稀硫酸能与氢氧化钠反应 D、稀硫酸能与氯化钡反应10. 如图,在滴有酚酞的氢氧化钠溶液中逐滴加入稀盐酸,对该过程描述正确的是( ) A、温度计读数持续上升 B、测其 pH 逐渐变小 C、溶液呈红色时,反应没发生 D、溶液呈无色时,溶液中的溶质一定只有氯化钠11. 下列各组物质的溶液,不另加试剂就能鉴别出来的一组是( )A、Na2CO3、HCl、H2SO4 B、KCl、NaCl、Na2SO4 C、HCl、NaOH、Ca(OH)2 D、FeCl3、NaOH、KNO312. 稀释浓硫酸时,正确操作是( )A、将水缓缓倒入盛有浓硫酸的烧杯中,边倒边搅拌 B、将浓硫酸缓缓倒入盛有水的量筒中,边倒边搅拌 C、将浓硫酸缓缓和水一起倒入烧杯中,边倒边搅拌 D、将浓硫酸缓缓倒入盛有水的烧杯中,边倒边搅拌13. 除去下列物质中的少量杂质,所用试剂和方法正确的是( )
A、温度计读数持续上升 B、测其 pH 逐渐变小 C、溶液呈红色时,反应没发生 D、溶液呈无色时,溶液中的溶质一定只有氯化钠11. 下列各组物质的溶液,不另加试剂就能鉴别出来的一组是( )A、Na2CO3、HCl、H2SO4 B、KCl、NaCl、Na2SO4 C、HCl、NaOH、Ca(OH)2 D、FeCl3、NaOH、KNO312. 稀释浓硫酸时,正确操作是( )A、将水缓缓倒入盛有浓硫酸的烧杯中,边倒边搅拌 B、将浓硫酸缓缓倒入盛有水的量筒中,边倒边搅拌 C、将浓硫酸缓缓和水一起倒入烧杯中,边倒边搅拌 D、将浓硫酸缓缓倒入盛有水的烧杯中,边倒边搅拌13. 除去下列物质中的少量杂质,所用试剂和方法正确的是( )选项
物质
杂质
试剂和方法
A
NaNO3
Na2CO3
滴入足量稀盐酸至不再产生气泡
B
KCl
K2SO4
滴入适量Ba(NO3)2溶液、过滤
C
CO
CO2
通过灼热的氧化铜粉末
D
H2
HCl
先通过NaOH溶液,再通过浓硫酸
A、A B、B C、C D、D14. 将一定质量的 Ba(OH)2 溶液与 Na2CO3 溶液混合恰好完全反应,向反应后的混合物中加入稀盐酸,产生气体的体积与加入稀盐酸的体积的关系如图所示,下列说法中正确的是( )
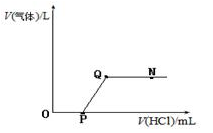 A、N 点时,所得溶液的 pH=7 B、Q 点时,所得溶液中的溶质只含有 BaCl2 C、O 至 P 段发生反应的化学方程式为 NaOH+HCl=NaCl+H2O D、P 至 Q 段发生反应的化学方程式为 Ba(OH)2+2HCl=BaCl2+2H2O15. 有一包白色固体,可能含有 BaCl2、KCl、K2SO4、K2CO3 中的一种或几种。取样溶于水,有白色沉淀产生;过滤后向沉淀中滴加稀盐酸,沉淀的量与加入盐酸体积的关系如图所示,由此推断白色固体中( )
A、N 点时,所得溶液的 pH=7 B、Q 点时,所得溶液中的溶质只含有 BaCl2 C、O 至 P 段发生反应的化学方程式为 NaOH+HCl=NaCl+H2O D、P 至 Q 段发生反应的化学方程式为 Ba(OH)2+2HCl=BaCl2+2H2O15. 有一包白色固体,可能含有 BaCl2、KCl、K2SO4、K2CO3 中的一种或几种。取样溶于水,有白色沉淀产生;过滤后向沉淀中滴加稀盐酸,沉淀的量与加入盐酸体积的关系如图所示,由此推断白色固体中( )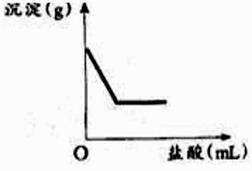 A、肯定只存在 BaCl2 B、可能存在 K2SO4 C、可能存在 KCl D、肯定不存在 K2CO316. 下列物质的转化,不能一步实现的是( )A、Cu→Cu(OH)2 B、Ba(NO3)2→BaSO4 C、Zn→ZnCl2 D、Ca(OH)2→NaOH17. 对于复分解反应,X+2NaOH═2Y+Cu(OH)2↓,下列分析中正确的是( )A、X 一定是 CuCl2 B、相对分子质量大小:X>Y C、Y 可能是 H2O D、Y 可能是 Na2SO418. 推理是学习化学的一种重要方法,下列推理正确的是( )A、氧化物中含有氧元素,所以含有氧元素的化合物都是氧化物 B、溶液中有晶体析出时,溶质质量减小,所以溶质的质量分数一定减小 C、碱性溶液能使紫色石蕊试液变蓝,所以能使石蕊试液变蓝的溶液一定呈碱性 D、碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐19. 下列图象能正确反映其对应关系的是( )
A、肯定只存在 BaCl2 B、可能存在 K2SO4 C、可能存在 KCl D、肯定不存在 K2CO316. 下列物质的转化,不能一步实现的是( )A、Cu→Cu(OH)2 B、Ba(NO3)2→BaSO4 C、Zn→ZnCl2 D、Ca(OH)2→NaOH17. 对于复分解反应,X+2NaOH═2Y+Cu(OH)2↓,下列分析中正确的是( )A、X 一定是 CuCl2 B、相对分子质量大小:X>Y C、Y 可能是 H2O D、Y 可能是 Na2SO418. 推理是学习化学的一种重要方法,下列推理正确的是( )A、氧化物中含有氧元素,所以含有氧元素的化合物都是氧化物 B、溶液中有晶体析出时,溶质质量减小,所以溶质的质量分数一定减小 C、碱性溶液能使紫色石蕊试液变蓝,所以能使石蕊试液变蓝的溶液一定呈碱性 D、碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐19. 下列图象能正确反映其对应关系的是( )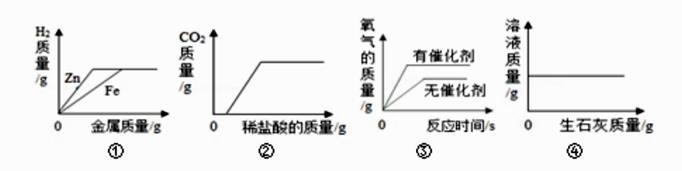 A、①向等质量、等浓度的稀硫酸中分别加入过量的 Zn 和 Fe B、②向含有少量 NaOH 的 Na2CO3 溶液中逐滴加入稀盐酸 C、③用等质量、等浓度的过氧化氢溶液在有、无催化剂条件下制取氧气 D、④一定温度时,向一定量的饱和石灰水中加入生石灰20. 根据下列实验得出的结论,正确的是( )A、某固体加入稀盐酸,产生了无色气体,证明该固体一定含有 B、某溶液中滴加 BaCl2 溶液,生成不溶于稀硝酸的白色沉淀,该溶液中一定有 C、某无色溶液滴入酚酞溶液后显红色,该溶液不一定是碱溶液 D、验证某烧碱样品中是否含有 Cl- , 先加入稀盐酸除去 OH- , 再加入 AgNO3 溶液,有不溶于稀硝酸的白色沉淀出现,证明含有 Cl-
A、①向等质量、等浓度的稀硫酸中分别加入过量的 Zn 和 Fe B、②向含有少量 NaOH 的 Na2CO3 溶液中逐滴加入稀盐酸 C、③用等质量、等浓度的过氧化氢溶液在有、无催化剂条件下制取氧气 D、④一定温度时,向一定量的饱和石灰水中加入生石灰20. 根据下列实验得出的结论,正确的是( )A、某固体加入稀盐酸,产生了无色气体,证明该固体一定含有 B、某溶液中滴加 BaCl2 溶液,生成不溶于稀硝酸的白色沉淀,该溶液中一定有 C、某无色溶液滴入酚酞溶液后显红色,该溶液不一定是碱溶液 D、验证某烧碱样品中是否含有 Cl- , 先加入稀盐酸除去 OH- , 再加入 AgNO3 溶液,有不溶于稀硝酸的白色沉淀出现,证明含有 Cl-二、填空题
-
21. 人类的日常生活离不开酸、碱、盐三类物质,请回答下列问题:(1)、山药中含有碱性皂角素,皮肤沾上会奇痒难忍。你认为可涂厨房中的来止痒;
(2)、①酸奶;②肥皂水;③食盐水;是生活中常见的三种物质。酸奶能使紫色石蕊试液变红,肥皂水显碱性,食盐水的 pH=7,它们的 pH 由小到大的顺序为;(填序号)
(3)、服用含有氢氧化铝的药物可以治疗胃酸过多症,反应的化学方程式为:。
22. 有一固体物质可能含有硫酸钾、硝酸铵、氯化钡中的一种或几种。现需要对此物质成分进行检测。甲同学向固体中加入足量的水,形成无色容液;乙同学向固体中加入足量氢氧化钡溶液,产生白色沉淀,放出刺激性气体。
(1)、该气体为(写化学式)。
(2)、根据两同学的实验现象可推定此物质的组成是。
23. 同学们在学习酸碱的化学性质时构建了如图知识网,A、B、C、D 是不同类别的化合物。请回答:
反应①的化学方程式为;反应②后生成蓝色溶液,则 B 的化学式为;反应④可用于制取烧碱,化学方程式为。
24. 化学实验室常见的酸有盐酸、硫酸、硝酸等,它们既有相似之处又有不同之点。(1)、稀盐酸、稀硫酸、稀硝酸具有相似的化学性质,原因是它们;
(2)、稀盐酸、稀硫酸、稀硝酸都能与氢氧化钠反应,这类反应的实质是(请用离子方程式来表示);(3)、若分别往稀盐酸和稀硫酸中加入少量硝酸钡溶液,观察到的现象为。
25. 利用以下装置对酸的化学性质进行探究。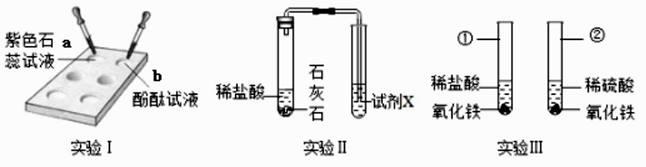 (1)、实验 I 中,在点滴板的 a、b 穴中滴入酸溶液后,溶液变红的是(填“a”或“b”)。使用点滴板的优点之一是。(2)、实验Ⅱ中,为了验证石灰石中含有碳酸根离子,试剂 X 的名称是。(3)、实验Ⅲ中,在仪器①、②中均可观察到的现象是。仪器②中发生反应的化学方程式是。26. 小金通过图示装置验证 CO2 能与 NaOH 发生化学反应。推注射器活塞向充满 CO2 的集气瓶中注入过量20%的 NaOH 溶液,振荡集气瓶后打开止水夹。
(1)、实验 I 中,在点滴板的 a、b 穴中滴入酸溶液后,溶液变红的是(填“a”或“b”)。使用点滴板的优点之一是。(2)、实验Ⅱ中,为了验证石灰石中含有碳酸根离子,试剂 X 的名称是。(3)、实验Ⅲ中,在仪器①、②中均可观察到的现象是。仪器②中发生反应的化学方程式是。26. 小金通过图示装置验证 CO2 能与 NaOH 发生化学反应。推注射器活塞向充满 CO2 的集气瓶中注入过量20%的 NaOH 溶液,振荡集气瓶后打开止水夹。 (1)、打开止水夹后观察到的现象是。
(1)、打开止水夹后观察到的现象是。
(2)、反应后将集气瓶中混合物过滤,所得溶液中除CaCl2 外,还存在的溶质有。
三、实验探究题
-
27. 实验室有五瓶失去标签的溶液,分别是:稀硫酸、氢氧化钠溶液、氯化钠溶液、碳酸钾溶液、硝酸钡溶液,为了鉴别它们,对它们编号并进行实验,实验现象如表。(注“①白色沉淀”指 A 与 B 反应产生白色沉淀,其它依次类推)
B
C
D
E
A
①白色沉淀
②无色气体
③无明显现象
④无明显现象
(1)、A、C 反应的化学方程式是;
(2)、B 物质是;(3)、若将 C 加入①中白色沉淀时有无色气体产生,则 C 是;
(4)、取 D、E 分别加入氯化镁溶液,在 D 中产生白色沉淀,E 中无明显现象,则 D 参与的反应的化学方程式是。
28. 用海水“晒盐”的方法得到的粗盐中,除氯化钠外,还含有氯化镁、氯化钙、硫酸钠等杂质。将此粗盐提纯的部分实验方案如下:
(1)、加入 BaCl2 溶液的目的是(用化学方程式表示);
(2)、D 中含离子有;
(3)、E 的主要成分的化学式是;(4)、某同学认为加入过量 K2CO3 溶液与加入过量 Na2CO3 溶液同样可以达到实验目的,这种说法是否合理,请说明理由。29. 构建模型和构建知识网络是科学学习中重要的学习方法,李华同学利用左手构建酸的性质知识网络,如图所示,请结合图示回答下列问题: (1)、如用湿润的 pH 试纸测定盐酸的 pH,则结果会(填“偏大”、“偏小”、“无影响”)。(2)、写出一个符合图中③的化学方程式。(3)、图中性质④属于反应(填基本反应类型)。30. 为探究一瓶久置的氢氧化钠固体样品是否全部变质,小柯取少量样品配制成溶液,再取少量溶液分别装入两支试管中,进行了如甲、乙两图所示实验。(注:BaCl2 溶液呈中性)(1)、小柯认为“甲图实验说明了氢氧化钠固体部分变质”。你认为小柯的观点是否正确,并说明理由。(2)、分析乙图实验的现象,可以确定样品的变质情况为。(3)、进一步探究:另取少量样品溶液,加入一定质量分数的稀盐酸,直至过量。请在丙图中画出“生成 CO2 的质量随加入稀盐酸质量变化”的大致图象。
(1)、如用湿润的 pH 试纸测定盐酸的 pH,则结果会(填“偏大”、“偏小”、“无影响”)。(2)、写出一个符合图中③的化学方程式。(3)、图中性质④属于反应(填基本反应类型)。30. 为探究一瓶久置的氢氧化钠固体样品是否全部变质,小柯取少量样品配制成溶液,再取少量溶液分别装入两支试管中,进行了如甲、乙两图所示实验。(注:BaCl2 溶液呈中性)(1)、小柯认为“甲图实验说明了氢氧化钠固体部分变质”。你认为小柯的观点是否正确,并说明理由。(2)、分析乙图实验的现象,可以确定样品的变质情况为。(3)、进一步探究:另取少量样品溶液,加入一定质量分数的稀盐酸,直至过量。请在丙图中画出“生成 CO2 的质量随加入稀盐酸质量变化”的大致图象。
四、解答题
-
31. 土壤的盐渍化是导致我国耕地减少的一个重大威胁,因为盐渍化之后土壤的 pH 会远高于 7(成为盐碱地),导致大多数植物难以生存。某科技攻关小组已尝试在一盐碱地上种植某种农作物,欲使农作物生长更好须采用多种措施,其中一种措施就是用碳酸水浇灌农作物,请运用所学知识解释采用碳酸水浇灌农作物的道理。32. 向碳酸钠和氯化钠的固体混合物 15.6 克中加入 100 克稀盐酸,恰好完全反应后得到 111.2克溶液。试计算:(1)、产生二氧化碳多少克?
(2)、原固体混合物中碳酸钠的质量是多少?(3)、所得溶液中溶质的质量分数是多少?(计算结果精确到 1%)33. 实验室有一瓶碳酸钙和氯化钙粉末组成的均匀混合物,小科用相同溶质质量分数的稀盐酸和该混合物反应(所得溶液均为不饱和溶液),四组实验数据记录如表,请分析计算:实验组别
一
二
三
四
稀盐酸质量/g
100.0
100.0
100.0
100.0
混合物质量/g
3.0
6.0
9.0
12.0
所得溶液质量/g
101.9
103.8
105.0
a
剩余固体质量/g
0
0
m
n
(1)、反应后,稀盐酸还有剩余的是第组;(2)、求混合物中碳酸钙和氯化钙质量之比;(3)、表中 a 的值为多少。(请写出计算过程)