第5讲:钠及其化合物
试卷更新日期:2018-09-30 类型:一轮复习
一、单选题
-
1. 关于钠的叙述中,正确的是( )A、钠是银白色金属,硬度很大 B、将金属钠放在坩埚里用酒精灯加热,金属钠剧烈燃烧,产生黄色火焰,生成淡黄色固体过氧化钠 C、金属钠在空气中燃烧,生成氧化钠 D、金属钠的熔点很高2. 下列物质与指定物质的主要成分对应正确的是( )A、赤铁矿—Fe2O3 B、漂白粉—NaClO C、纯碱—NaOH D、大理石—Ca(OH)23. 下列钠的化合物中,可用于呼吸面具作为O2来源的是( )A、Na2O B、Na2O2 C、NaCl D、Na2CO34. 将一小块金属钠放在坩埚里加热,实验现象描述正确的是( )
①钠在燃烧之前先熔化 ②钠燃烧的火焰呈紫色 ③钠燃烧后得到白色固体 ④钠燃烧的火焰呈黄色 ⑤钠燃烧后生成物为淡黄色固体
A、①④⑤ B、只有⑤ C、只有① D、②③5. 少量金属钠投入下列试剂中,反应最缓慢的是( )
A、蒸馏水 B、0.1mol/L盐酸 C、0.1mol/L NaOH溶液 D、无水乙醇6. 化学与生产生活密切相关,下列说法错误的是( )A、Na2O2可与CO2反应放出氧气,可用于制作呼吸面具 B、SiO2具有导电性,可用于制作光导纤维和光电池 C、聚四氟乙烯耐酸碱腐蚀,可用作化工反应器的内壁涂层 D、氯水具有较强的氧化性,可用于漂白纸张、织物等7. 下列关于钠与水反应的说法中,不正确的有( )项。①将小块的钠投入滴有紫色石蕊试液的水中,反应后溶液变红
②将钠投入稀盐酸中,钠先与水反应,后与HCl反应
③钠在水蒸气中反应(密闭)时因温度高会发生燃烧现象
④将两小块质量相等的金属钠,一块直接投入水中,另一块用锡箔包住,在锡箔上刺些小孔,然后按入水中,两者放出的氢气质量相等
A、1 B、2 C、3 D、48. 下列离子方程式书写不正确的是( )A、铁与氯化铁溶液反应:Fe+2Fe3+=3Fe2+ B、钠与水反应:2Na + 2H2O =2Na+ + 2OH- + H2↑ C、氯气与氢氧化钠溶液反应:Cl2+2OH﹣=Cl﹣+ClO﹣+H2O D、碳酸氢钠溶液与稀盐酸反应:2H++CO32﹣=CO2↑+H2O9. 在空气中长时间放置少量金属钠,最终的产物是( )A、Na2O B、NaOH C、Na2CO3 D、Na2O210. 将一小粒钠投入盛有硫酸铜溶液的小烧杯中,不可能观察到的现象是( )A、溶液中出现蓝色絮状沉淀 B、有红色的铜被置换出来 C、钠粒熔成小球浮在水面四处游动 D、有气体产生11. 把4.48 LCO2通过一定量的固体过氧化钠后收集到3.36L气体(标况下),则这3.36L气体的质量是( )A、3.8g B、4.8g C、5.6g D、6.0g12. 通过测定混合气中O2含量可计算已变质的Na2O2 (含Na2CO3) 纯度,实验装置如图(Q为弹性良好的气囊)。下列分析错误的是( )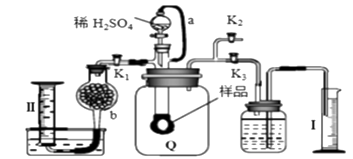 A、干燥管b中装入碱石灰 B、Q气球中产生的气体主要成分O2、CO2 C、测定气体总体积必须关闭K1、K2 , 打开K3 D、读完气体总体积后,关闭K3 , 缓缓打开K1;可观察到Q气球慢慢缩小13. 某实验小组通过下图所示实验探究Na2O2与水的反应:
A、干燥管b中装入碱石灰 B、Q气球中产生的气体主要成分O2、CO2 C、测定气体总体积必须关闭K1、K2 , 打开K3 D、读完气体总体积后,关闭K3 , 缓缓打开K1;可观察到Q气球慢慢缩小13. 某实验小组通过下图所示实验探究Na2O2与水的反应: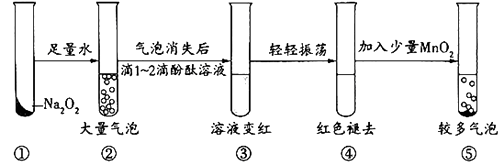
下列说法不正确的是( )
A、②中的大量气泡主要成分是氧气 B、③中溶液变红,说明有碱性物质生成 C、④中现象可能是由于溶液中含有强氧化性物质造成的 D、⑤中MnO2的主要作用是降低了水中氧气的溶解度14. 下面关于Na2CO3和NaHCO3性质的叙述,正确的是( )A、受热时NaHCO3比Na2CO3稳定 B、往Na2CO3和NaHCO3溶液中滴加酚酞都变红,说明Na2CO3和NaHCO3都是碱 C、NaHCO3能转化成Na2CO3 , 但Na2CO3不能转化成NaHCO3 D、物质的量相等的Na2CO3和NaHCO3分别与足量盐酸反应,放出的CO2的物质的量相等二、填空题
-
15. 金属钠在实验室通常保存在中,切下一小块钠进行化学实验,要用到的实验用品有 , 金属钠失火时,应该用灭火.过氧化钠与水反
应,(填化学式)作还原剂,反应后的溶液中加入酚酞的现象是 .
16. 某银白色固体A在空气中点燃,火焰呈黄色,并生成淡黄色固体B;将A在空气中露置,最后变成白色固体C.将A、B投入水中都生成D;B与D分别与二氧化碳反应.则A是;B是;C是;D是 . B与H2O反应的化学方程式 , B与CO2反应的化学方程式为 A与H2O反应的化学方程式 .17. 将金属钠放入盛有下列溶液的小烧杯中,既有气体,又有白色沉淀产生的是①MgSO4溶液②NaCl溶液③Na2SO4溶液④饱和澄清石灰水⑤Ca(HCO3)2溶液⑥CuSO4溶液 ⑦饱和NaCl溶液.
三、实验探究题
-
18. 现有一定量含有Na2O杂质的Na2O2试样,用如图的实验装置测定Na2O2试样的纯度。(可供选用的反应物只有CaCO3固体、6 mol·L-1盐酸、6 mol·L-1硫酸和蒸馏水)
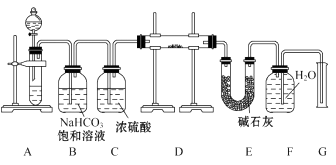
回答下列问题:
(1)、装置A中液体试剂选用(2)、装置B的作用是 , 装置C的作用是 , 装置E中碱石灰的作用是。(3)、装置D中发生反应的化学方程式是。(4)、若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为224 mL(标准状况),则Na2O2试样的纯度为。19. 如图实验装置用于验证某些物质的性质.在试管A中装入足量的固体NaHCO3.试回答下列问题: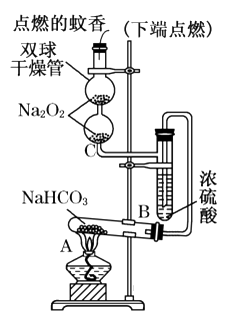 (1)、在A试管内发生反应的化学方程式是 .(2)、B装置的作用是 .(3)、在双球干燥管内发生反应的化学方程式为 .(4)、双球干燥管内观察到的实验现象是 . 上述实验现象说明 .(5)、若将干燥管内的Na2O2换成Na2O,则双球干燥管内观察到的实验现象是 .20. 有人设计了如图所示的实验装置来探究钠与水反应(铁架台等仪器略去).实验前在橡胶塞下端打一个小孔穴,将一大小适中的钠块固定于针头下端,向上抽动针头使钠块藏于孔穴内.在玻璃反应管内装入适量水(使钠块不与水接触).实验时,拔去橡胶乳头,按住橡胶塞,将针头缓缓向上拔起使钠与水接触,反应管内的液体被产生的气体压出,流入置于下方的烧杯中,气体则被收集在反应管内.
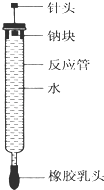
(1)、在A试管内发生反应的化学方程式是 .(2)、B装置的作用是 .(3)、在双球干燥管内发生反应的化学方程式为 .(4)、双球干燥管内观察到的实验现象是 . 上述实验现象说明 .(5)、若将干燥管内的Na2O2换成Na2O,则双球干燥管内观察到的实验现象是 .20. 有人设计了如图所示的实验装置来探究钠与水反应(铁架台等仪器略去).实验前在橡胶塞下端打一个小孔穴,将一大小适中的钠块固定于针头下端,向上抽动针头使钠块藏于孔穴内.在玻璃反应管内装入适量水(使钠块不与水接触).实验时,拔去橡胶乳头,按住橡胶塞,将针头缓缓向上拔起使钠与水接触,反应管内的液体被产生的气体压出,流入置于下方的烧杯中,气体则被收集在反应管内.(1)钠与水反应的离子方程式为 .
(2)实验中“钠块熔化为闪亮的小球”说明 ;向烧杯中的溶液中滴加 ,溶液变红,说明钠与水反应生成碱性物质.
(3)如果实验前加入反应管内水的体积为a mL,欲使水最终全部被排出,则所取金属钠的质量至少为 g.(设当时实验条件下气体摩尔体积为V mL/mol,写出简要步骤)
四、综合题
-
21. 现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。

请根据以上信息回答下列问题:
(1)、写出下列物质的化学式:A: B: F: 丙:(2)、说出黄绿色气体乙的一种用途:。(3)、若除去F溶液中含有的少量G,需加入 , 实验室检验G中所含的金属离子时,常在G的溶液中加入溶液。(4)、反应①的离子方程式为。(5)、反应⑦涉及的化学方程式有。