北京市房山区2017-2018学年中考化学二模考试试卷
试卷更新日期:2018-09-26 类型:中考模拟
一、单选题
-
1. 铜是人类广泛使用的金属。下列铜制品中利用其导热性的是( )A、
 铜导线
B、
铜导线
B、 铜火锅
C、
铜火锅
C、 黄铜饰品
D、
黄铜饰品
D、 青铜宝剑
2. 下列房山美食中,富含蛋白质的是( )A、十渡鲟鱼 B、蒲洼蘑菇 C、张坊磨盘柿 D、上方山香椿3. 下列物质中,属于溶液的是( )A、冰水 B、糖水 C、牛奶 D、小米粥4. 下列化学实验操作错误的是( )A、
青铜宝剑
2. 下列房山美食中,富含蛋白质的是( )A、十渡鲟鱼 B、蒲洼蘑菇 C、张坊磨盘柿 D、上方山香椿3. 下列物质中,属于溶液的是( )A、冰水 B、糖水 C、牛奶 D、小米粥4. 下列化学实验操作错误的是( )A、 倾倒液体
B、
倾倒液体
B、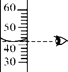 读液体体积
C、
读液体体积
C、 点燃酒精灯
D、
点燃酒精灯
D、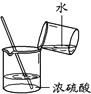 稀释浓硫酸
5. 下列物质中,含有氧分子的是( )A、O2 B、CO2 C、H2O2 D、KMnO46. 配制100 g溶质质量分数为10%的硝酸钾溶液,不需要的仪器是( )
稀释浓硫酸
5. 下列物质中,含有氧分子的是( )A、O2 B、CO2 C、H2O2 D、KMnO46. 配制100 g溶质质量分数为10%的硝酸钾溶液,不需要的仪器是( )
A、量筒 B、烧杯 C、酒精灯 D、玻璃棒7. 实验室里用向上排空气法收集CO2 , 依据CO2的性质是( )A、无色无味 B、能溶于水 C、密度比空气小 D、密度比空气大8. 下列安全图标中,表示“禁止吸烟”的是( )A、 B、
B、 C、
C、 D、
D、 9. 下列是健康人体内几种体液的pH范围,其中呈酸性的是( )
9. 下列是健康人体内几种体液的pH范围,其中呈酸性的是( )
A、胃液(0.8~1.5) B、血液(7.35~7.45) C、胆汁(7.1~7.3) D、小肠液(7.8~8.0)10. 下列关于物质用途的描述中,正确的是( )A、氧气用于灭火 B、二氧化碳作燃料 C、碳酸钙作补钙剂 D、烧碱用于改良酸性土壤11. 下表是6种富钙食品每100克中的钙含量。食品名称
木耳
芝麻酱
牛奶
山楂
黄豆
海带
钙含量/g
0.295
1.170
0.135
0.162
0.169
0.445
每天饮用500g牛奶,能为人体补充钙元素的质量为( )
A、0.675g B、5.85g C、13.5g D、67.5g12. 甲、乙两种物质的溶解度曲线如图所示。下列说法正确的是( )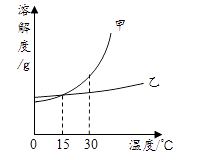 A、甲的溶解度比乙大 B、升温能使甲的不饱和溶液变成饱和溶液 C、15℃时,甲、乙饱和溶液的质量一定相同 D、将30℃时的甲、乙饱和溶液降温至15℃,甲、乙溶液中溶质的质量分数相等
A、甲的溶解度比乙大 B、升温能使甲的不饱和溶液变成饱和溶液 C、15℃时,甲、乙饱和溶液的质量一定相同 D、将30℃时的甲、乙饱和溶液降温至15℃,甲、乙溶液中溶质的质量分数相等二、简答题
-
13. 化学就在我们身边,请从A或B两题中任选1个作答,若两题均作答,按A计分。
A
B
馒头,中国特色传统面食之一。
⑴蒸馒头的过程中常常需要加入发酵粉(主要成分是碳酸氢钠),使馒头更加松软。碳酸氢钠的俗称是。
⑵碳酸氢钠(NaHCO3)中氢、氧元素的质量比为。
生活中将自来水煮沸会出现水垢,可以用白醋除掉水垢。
⑴自来水属于(填“纯净物”或“混合物”)
⑵白醋中含有醋酸(CH3COOH),醋酸中氢元素质量分数的计算式为。
14. 平昌冬奥会闭幕式上,“北京8分钟”表演中滑冰的“熊猫”木偶惊艳亮相。(1)、熊猫木偶使用的材料中包括铝合金管材,铝属于(填“金属”或“非金属”)元素。 (2)、冰是水的固态,水变成冰,其分子种类(填“改变”或“不变”)。(3)、冰鞋下的冰刀主要成分是铁,保养时要避免接触酸性物质,其原因是。15. 阅读下面科普短文。
(2)、冰是水的固态,水变成冰,其分子种类(填“改变”或“不变”)。(3)、冰鞋下的冰刀主要成分是铁,保养时要避免接触酸性物质,其原因是。15. 阅读下面科普短文。豆制品是以大豆等豆类为原料,经加工而成的食品。
资料一:豆制品的制备
中国是大豆的故乡,中国古代劳动人民利用豆类创制了许多广为流传的豆制品,以下为几种豆制品的主要制作流程:

资料二:豆制品的营养
豆制品的营养主要体现在丰富的蛋白质含量上, 另外还含有钙、磷、铁等矿物质,以及维生素B1、B2等。豆制品中富含胆固醇,所含胆固醇与不饱和脂肪酸有较好的祛脂作用,且热量很低。因此,肥胖和高血脂、高血压等心脑血管疾病患者可多吃豆制品。豆制品还可预防便秘、骨质疏松和增强免疫力。
资料三:豆制品的弊端
豆制品具有丰富的营养,色香味俱佳,但摄入过多,也会损害身体健康。首先,豆制品含有较多非必需氨基酸,肾病患者应尽量禁食。其次,豆制品含有较多嘌呤,痛风病人应少食或不食。另外,胃病患者也应尽量少食用豆制品,以免刺激胃液分泌、产生肠道胀气等。
总之,适量食用豆制品,才是科学饮食之道。
依据文章内容回答下列问题。
(1)、由豆腐脑制得豆腐的过程属于(填“物理”或“化学”)变化。(2)、豆制品中含有蛋白质、矿物质、等营养物质。(3)、提倡肥胖和心脑血管疾病患者多吃豆制品的理由是。(4)、由于豆制品中含有元素,因此可预防骨质疏松、佝偻病等。(5)、下列关于豆制品的说法正确的是_____________(填序号)。A、豆制品是以豆类为主要原料,加工而成的食品 B、豆浆经过点浆、压制后可制成腐竹 C、肾病患者应该尽量禁食豆制品 D、豆制品营养丰富,因此人人皆宜、多多益善16. 利用下图所示实验验证铁、铜、银的金属活动性顺序。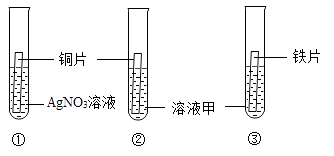 (1)、实验①的目的是。(2)、为了验证三种金属的活动性顺序,溶液甲可以是(写出一种即可)。
(1)、实验①的目的是。(2)、为了验证三种金属的活动性顺序,溶液甲可以是(写出一种即可)。三、填空题
-
17. 随着经济的发展,能源与环境成为人们日益关注的问题。(1)、目前人们使用的燃料大多来自化石燃料,如、石油、天然气等,天然气主要成分燃烧的化学方程式为。(2)、开发和利用太阳能、潮汐能和等新能源是解决能源问题的重要途径。
四、流程题
-
18. 海水素有“液体工业原料”之美誉。工业“从海水中提取镁”的主要流程如下:
 (1)、煅烧炉中,发生反应的化学方程式为:CaCO3 CaO+CO2↑,此反应属于基本类型中的反应。(2)、反应沉淀池中发生如下反应:
(1)、煅烧炉中,发生反应的化学方程式为:CaCO3 CaO+CO2↑,此反应属于基本类型中的反应。(2)、反应沉淀池中发生如下反应:①CaO+H2O=Ca(OH)2;
②Ca(OH)2+ MgSO4= CaSO4 + Mg(OH)2↓,
操作Ⅰ为。
(3)、电解槽中,能生成镁的反应物为。(4)、从海水中提取镁的过程中,镁元素的化合价变化为。五、实验题
-
19. 请从A或B两题中任选一个作答,若两题均作答,按A计分。
A 木炭燃烧
B铁丝燃烧

⑴木炭在氧气中燃烧时,可观察到的实验现象为。
⑵若验证生成物,需向集气瓶中加入的药品为。

⑴铁丝在氧气中燃烧的化学方程式为。
⑵实验时,预先在集气瓶里装少量水的作用是。
20. 如图所示,在白色点滴板1~6的孔穴中,分别滴加2滴稀盐酸。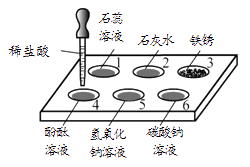 (1)、无明显变化的孔穴有(填孔穴序号)。(2)、孔穴3中发生反应的化学方程式为。(3)、孔穴5反应后溶液中的溶质是(写出所有可能)。21. 利用下图装置测定空气中氧气含量,燃烧匙中盛有足量红磷,左右管中盛有等量水。点燃红磷迅速放入左管中,并盖紧胶塞。
(1)、无明显变化的孔穴有(填孔穴序号)。(2)、孔穴3中发生反应的化学方程式为。(3)、孔穴5反应后溶液中的溶质是(写出所有可能)。21. 利用下图装置测定空气中氧气含量,燃烧匙中盛有足量红磷,左右管中盛有等量水。点燃红磷迅速放入左管中,并盖紧胶塞。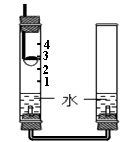 (1)、红磷燃烧的化学方程式为。(2)、若红磷量不足将导致的结果是。(3)、整个实验过程中,左管中的水面变化情况为。
(1)、红磷燃烧的化学方程式为。(2)、若红磷量不足将导致的结果是。(3)、整个实验过程中,左管中的水面变化情况为。六、科学探究题
-
22. 维生素C又名抗坏血酸,它能增强人体对疾病的抵抗能力。某化学学习小组对其进行如下研究:
(查阅资料)维生素C常温下为白色晶体,易与氧气、高锰酸钾等物质反应。
Ⅰ.探究维生素C的性质
(进行实验)
实验序号
1-1
1-2
1-3
1-4
操作

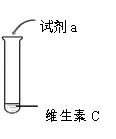

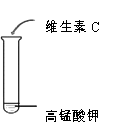
现象
白色固体消失,形成溶液
溶液变为红色
……
紫色溶液褪色
结论
……
维生素C溶液为酸性
维生素C能与
碳酸氢钠反应
维生素C能与高锰酸钾反应使其溶液褪色
(1)、由实验1-1现象推测维生素C具有的物理性质是。(2)、实验1-2中使用的试剂a为_________(填序号,下同)。A、紫色石蕊试液 B、无色酚酞试液 C、氢氧化钠溶液(3)、实验1-3中实验现象为。(4)、Ⅱ.测定食品中维生素C的含量【进行实验】
实验序号
2-1
2-2
2-3
2-4
2-5
实验操作
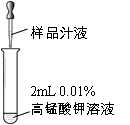
鲜榨的猕猴桃汁
鲜榨的橙汁
鲜榨的西红柿汁
加热后冷却至室温的鲜榨西红柿汁
放置12小时的西红柿汁
紫色溶液褪色时所滴加的样品滴数
6
8
11
14
……
【解释与结论】
实验2-1至2-4中,维生素C的含量最高的是。
(5)、由实验2-1至2-4可知,影响食品中维生素C含量的因素有。(6)、请你推测实验2-5中,紫色溶液褪色时的样品滴数可能为_________。A、9 B、11 C、15
-
-