陕西省咸阳市2017-2018学年高考理综-化学二模考试试卷
试卷更新日期:2018-08-16 类型:高考模拟
一、单选题
-
1. 化学与人类的生活、生产息息相关,下列叙述正确的是( )A、“青蒿一握,以水二升渍,绞取计”,提取青蒿素的过程属于化学变化 B、《本草纲目》中“冬月灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣”中的碱是K2CO3 C、日常生活中常用汽油去除衣物上的油污,用热的纯碱溶液洗涤炊具上的油污,两者的原理完全相同 D、“84消毒液”的有效成分为NaClO,“洁厕灵”的有效成分为HCl,若将两者混合使用,其杀菌效果和去除厕所污溃的效果都将加强2. 设NA为阿伏加德罗常数的值,下列叙述正确的是( )A、所含共价键数均为0.2NA的白磷(P4)和甲烷的物质的量相等 B、1L 1mol/LH2O2的水溶液中含有的氧原子数为2NA C、将1molFe 与一定量的稀硝酸充分反应,转移的电子数可能为2NA D、1L0.1mol/LCH3COONa溶液中含有的Na+和CH3COO-的总数为0.2NA3. 下列实验操作能达到实验目的的是( )
选项
实验目的
实验操作
A
测定NaClO溶液的pH
用玻璃棒蘸取NaClO溶液点在pH试纸上,与标准比色卡对照
B
非金属性Cl>C
将稀盐酸滴入碳酸钠溶液中
C
稀硫酸有氧化性
向硝酸亚铁溶液中加入稀硫酸,充分反应后滴加KSCN溶液
D
比较乙醇中羟基氢原子与水中氢原子的活泼性
分别将少量钠投入到盛有水和乙醇的烧杯中
A、A B、B C、C D、D4. 有机物M、N、Q的转化关系为 ,下列说法错误的是( ) A、M的名称为异丁烷 B、N的同分异构体有7种(不考虑立体异构,不包括本身) C、M N、N Q的反应类型分别为取代反应和消去反应 D、M、N、Q均能使溴水层褪色,但原理不同5. 下列各选项中,物质之间通过一步反应就能实现如图所示变化的是( )
,下列说法错误的是( ) A、M的名称为异丁烷 B、N的同分异构体有7种(不考虑立体异构,不包括本身) C、M N、N Q的反应类型分别为取代反应和消去反应 D、M、N、Q均能使溴水层褪色,但原理不同5. 下列各选项中,物质之间通过一步反应就能实现如图所示变化的是( )
选项
甲
乙
丙
丁
A
Al
AlCl3
Al2O3
NaAlO2
B
S
H2S
SO2
SO3
C
Na
Na2O
NaOH
Na2O2
D
N2
NH3
NO
NO2
A、A B、B C、C D、D6. 常温下,取浓度均为0.1mol/L的HX溶液和ROH溶液各20mL,分别用0.1mol/LNaOH溶液、0.1mol·L-1盐酸进行滴定。滴定过程中溶液的pH随滴加溶液的体积变化关系如图所示。下列说法正确的是( ) A、HX为强酸,ROH为弱碱 B、滴定前,ROH溶液中存在c(ROH)>c(OH-)>c(R+)>c(H+) C、曲线Ⅱ:滴定至V=10mL时存在2c(OH-)-c(H+)=c(HX)-c(X-) D、滴定至V=40mL的过程中,两种溶液中由水电离出的c(H+)·c(OH-)不变7. “软电池”采用一张薄层纸片作为传导体,一面为锌,另一面为二氧化锰,纸层中水和氧化锌组成电解液。电池总反应为:Zn+2MnO2+H2O=2MnO(OH)+ZnO。下列说法正确的是( )A、该电池的正极为氧化锌 B、锌电极附近溶液的pH不变 C、电池正极反应式:2MnO2+2e-+2H2O=2MnO(OH)+2OH- D、当0.1molZn完全溶解时,流经电解液的电子的物质的量为0.2mol
A、HX为强酸,ROH为弱碱 B、滴定前,ROH溶液中存在c(ROH)>c(OH-)>c(R+)>c(H+) C、曲线Ⅱ:滴定至V=10mL时存在2c(OH-)-c(H+)=c(HX)-c(X-) D、滴定至V=40mL的过程中,两种溶液中由水电离出的c(H+)·c(OH-)不变7. “软电池”采用一张薄层纸片作为传导体,一面为锌,另一面为二氧化锰,纸层中水和氧化锌组成电解液。电池总反应为:Zn+2MnO2+H2O=2MnO(OH)+ZnO。下列说法正确的是( )A、该电池的正极为氧化锌 B、锌电极附近溶液的pH不变 C、电池正极反应式:2MnO2+2e-+2H2O=2MnO(OH)+2OH- D、当0.1molZn完全溶解时,流经电解液的电子的物质的量为0.2mol二、综合题
-
8. 某学习小组为探究镁及其化合物的性质,查阅资料知:
ⅰ
Mg3N2遇水发生水解反应
ⅱ
2NO2+2NaOH=NaNO2+NaNO3+H2O
NO2+NO+2NaOH=2NaNO2+H2O
ⅲ
常温下,NH3·H2O、CH3COOH的电离常数均为1.8×10-5
(1)、I.探究镁的性质。为探究镁与二氧化氮反应的产物,设计如图所示实验装置。

简述检查该装置气密性的方法;B装置的作用是.
(2)、实验时,当A装置中充满红棕色气体时点燃酒精灯,这样操作的目的是。(3)、确定有N2生成的实验现象是。(4)、实验完毕,为确认产物中有Mg3N2 , 取少量A中固体于试管中,滴加蒸馏水, , 则产物中有氮化镁。(5)、经测定,Mg与NO2反应生成MgO、Mg3N2和N2 , 其中Mg3N2和N2的物质的量相等。请写出A中发生反应的化学方程式:
(6)、Ⅱ.探究Mg(OH)2在氯化铵溶液中溶解的原因。供选试剂有:氢氧化镁、蒸馏水、硝酸铵溶液、盐酸、醋酸铵溶液。
取少量氢氧化镁粉末于试管中,向其中加入足量饱和氯化氨溶液,振荡,白色粉末全部溶解。为了探究其原因,他们依据Mg(OH)2(s)==Mg2+(aq)+2OH-(aq)提出两种假设。
假设1:氯化铵溶液呈酸性,H++OH-=H2O,促进Mg(OH)2溶解;
假设2:NH4++OH-=NH3·H2O,促进Mg(OH)2溶解。
请你帮他们设计实验验证哪一种假设正确:.
9. 以方铅矿(主要成分是PbS,含少量ZnS、Fe、Ag)为原料提炼铅及其化合物的工艺流程如下:
请回答下列问题:
(1)、流程中“趁热过滤”的目的是 , 滤渣的主要成分是。(2)、该工艺流程中可循环利用的物质是。(3)、浊液1中通入适量氯气时,发生反应的离子方程式为。(4)、《药性论》中有关铅丹(Pb3O4)的描述是:“治惊悸狂走,呕逆,消渴。”向铅丹中滴加浓盐酸时,产生黄绿色气体,请写出发生反应的化学方程式。(5)、取一定量含有Pb2+、Cu2+的工业废水,向其中滴加Na2S溶液,当PbS开始沉淀时,溶液中c(Pb2+)/c(Cu2+)=。[已知Kp(PbS)=3.4×10-28 , Kp(CuS)=1.3×10-36](6)、炼铅和用铅都会使水体因重金属铅的含量增大而造成严重污染。水溶液中铅的存在形态主要有Pb2+、Pb(OH)+、Pb(OH)2、Pb(OH)3-、Pb(OH)42-。各形态的浓度分数x与溶液PH变化的关系如下图所示:
①探究Pb2+的性质:向含Pb2+的溶液中逐滴滴加NaOH溶液,溶液变浑浊,继续滴加NaOH溶液又变澄清;pH>13时,溶液中发生的主要反应的离子方程式为。
②除去溶液中的Pb2+:科研小组用一种新型试剂可去除水中的铅和其他杂质离子,实验结果记录如下:
离子
Pb2+
Ca2+
Fe3+
Mn2+
处理前浓度(mg/L)
0.100
29.8
0.12
0.087
处理后浓度(mg/L)
0.004
22.6
0.04
0.053
由表可知该试剂去除Pb2+比Fe3+效果好,请用表中有关数据说明.
10. 研究化学反应原理对于生产、生活及环境保护具有重要意义。请回答下列问题:(1)、常温下,物质的量浓度均为0.1mol/L的四种溶液:①NH4I;②CH3COONa;③(NH4)2SO4;④ Na2CO3 , pH从大到小排列顺序为(填序号)。(2)、苯乙烯是工业上合成树脂、离子交换树脂及合成橡胶等的重要单体,工业上可用乙苯催化脱氢方法制备苯乙烯: 。
。①已知乙苯(g)、苯乙烯(g)的燃烧热分别为akJ/mol,bkJ/mol,则氢气的燃烧热为kJ/mol(用含有Q、a、b的表达式表示,其中Q、a、b均大于0)。
②在实际生产中,在恒压条件下常以高温水蒸气作为反应体系的稀释剂(水蒸气不参加反应),此时乙苯的平衡转化率与水蒸气的用量、压强(p)的关系如下图所示。

Ⅰ.加入水蒸气稀释剂能提高乙苯转化率的原因是
Ⅱ.用平衡分压代替平衡浓度计算平衡常数(Kp),其中,分压=总压×物质的量分数,则900K时的平衡常数Kp=.
Ⅲ.改变下列条件,能使乙苯的反应速率和转化率一定增大的是 (填字母)。
A.恒容时加入稀释剂水蒸气
B.压强不变下,温度升至1500K
C.在容积和温度不变下充入Ar
D.选用催化效果更好的催化剂
(3)、利用“Na-CO2”电池将CO2变废为宝。我国科研人员研制出的可充电“Na-CO2”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为4Na+3CO2 2Na2CO3+C。放电时该电池“吸入”CO2 , 其工作原理如图所示:
①放电时,正极的电极反应式为。
②若生成的Na2CO3和C全部沉积在电极表面,当转移0.2mol 电子时,两极的质量差为g。(假设放电前两电极质量相等)
11. 根据要求回答下列问题:(1)、基态氮原子最高能级上电子的自旋方向有种,硒原子的电子排布式为[Ar]。(2)、铁的一种配合物Fe(CO)5熔点为-20.5℃,沸点为103℃,易溶于CCl4 , 据此可以判断Fe(CO)5晶体属于(填晶体类型)。(3)、与BF3互为等电子体的分子和离子分别为(各举1例);已知分子中的大π键可用符号Ⅱnm表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Ⅱ66),则BF3中的大π键应表示为。(4)、金属晶体的四种堆积如下图,金属钠的晶体堆积模型为(填字母)。 (5)、砷化硼(BAs)晶体结构与金刚石相似,则:
(5)、砷化硼(BAs)晶体结构与金刚石相似,则:①BAs晶体中,As的杂化形式为.
②已知B原子的电负性比As原子的电负性大,则As与B之间存在的化学键有(填字母)。
A.离子键
B.金属键
C.极性键
D.氢键 E.配位键 F.σ键 G.π键
③BAs晶体的晶胞参数为bpm,则其晶体的密度为(列出表达式,设NA为阿伏加德罗常数的数值)g/cm3。
12. 具有抗菌作用的白头翁素衍生物M的合成路线如下图所示: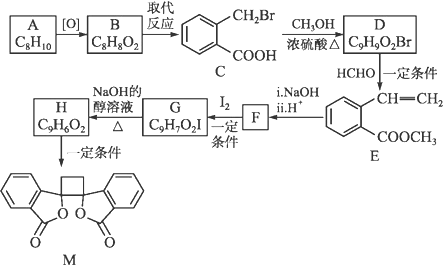
已知:ⅰ.RCH2Br R—HC=CH—R'
ⅱ.R—HC=CH—R'
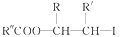
ⅲ.R—HC=CH—R'
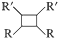 (以上R、R'、R″代表氢、烷基或芳基等)(1)、D中官能团名称为 , A的化学名称为。(2)、F的结构简式为 , 则与F具有相同官能团的同分异构体共种(考虑顺反异构,不包含F)。(3)、由G生成H的化学方程式为 , 反应类型为。(4)、下列说法错误的是(选填字母序号)。
(以上R、R'、R″代表氢、烷基或芳基等)(1)、D中官能团名称为 , A的化学名称为。(2)、F的结构简式为 , 则与F具有相同官能团的同分异构体共种(考虑顺反异构,不包含F)。(3)、由G生成H的化学方程式为 , 反应类型为。(4)、下列说法错误的是(选填字母序号)。a.可用硝酸银溶液鉴别B、C两种物质
b.由H生成M的反应是加成反应
c.1 mol E最多可以与4 mol H2发生加成反应
d.1 mol M与足量NaOH溶液反应,消耗4 mol NaOH
(5)、以乙烯为起始原料,结合已知信息选用必要的无机试剂,写出合成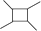 的路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
的路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。