湖北省恩施州2018年中考化学试题
试卷更新日期:2018-08-16 类型:中考真卷
一、单选题
-
1. 下列生活中常见的现象。其中与另外三种有本质区别的是( )A、酒精挥发 B、气球爆炸 C、食物腐烂 D、湿衣服晒干2. 下列叙述正确的是( )A、利用肥皂水可以将硬水软化 B、电解水的实验中,正极与负极产生的气体的质量比为1:2 C、冬天取暖时,煤炉上一盆水可以防止煤气中毒 D、由于氮气的化学性质不活泼,因此常用作保护气3. 下列关于氢氧化钠的描述中错误的是( )A、可用于改良酸性土壤 B、易溶于水,溶解时放出大量的热 C、能去除油污,可作炉具清洁剂 D、对皮肤有强烈的腐独作用4. 某工地发生多人食物中毒,经化验为误食工业用盐亚硝酸钠(NaNO2)所致。NaNO2中氮元素的化合价是( )A、+4 B、+3 C、+2 D、+55. 现将10gA和足量的B混合加热,A和B发生化学反应。10gA完全反应后生成8gC和4gD,则参加反应的A和B的质量比是A、1:1 B、2:1 C、5:1 D、4:16. 下列说法中错误的是( )A、氧化钙的俗名是熟石灰 B、氯化钾属于钾肥 C、甲烷属于有机物 D、气体可压缩储存在钢瓶中,是因为分子之间有间隔7. 造成酸雨的主要物质是( )A、二氧化硫和二氧化氮 B、二氧化硫和一氧化碳 C、一氧化碳和二氧化碳 D、一氧化碳和甲烷8. 元素周期表是学习和研究化学的重要工具,如图是元素周期表的一部分,其中X、Y、Z代表三种不同的元素。下列说法中正确的是( )
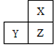 A、原子序数:X>Y B、核外电子数:X=Z C、Y和Z处于同一周期 D、X和Z的电子层数相同9. A,B,C三种固体物质的溶解度曲线如图所示,下列说法正确的是( )
A、原子序数:X>Y B、核外电子数:X=Z C、Y和Z处于同一周期 D、X和Z的电子层数相同9. A,B,C三种固体物质的溶解度曲线如图所示,下列说法正确的是( ) A、t1℃时,三种物质的溶解度由大到小的顺序是A>B>C B、t2℃时,A和C的溶解度相等 C、将B的饱和溶液变为不饱和溶液可采用升高温度的方法 D、A,B,C三种物质的溶解度都随温度的升高而增大10. 甲、乙、丙、丁表示四种粒子的结构示意图。下列说法错误的是( )
A、t1℃时,三种物质的溶解度由大到小的顺序是A>B>C B、t2℃时,A和C的溶解度相等 C、将B的饱和溶液变为不饱和溶液可采用升高温度的方法 D、A,B,C三种物质的溶解度都随温度的升高而增大10. 甲、乙、丙、丁表示四种粒子的结构示意图。下列说法错误的是( )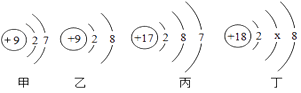 A、甲、乙属于同种元素 B、甲、乙、丙具有相似的化学性质 C、丁中x=8 D、乙表示阴离子
A、甲、乙属于同种元素 B、甲、乙、丙具有相似的化学性质 C、丁中x=8 D、乙表示阴离子二、填空题
-
11. 宏观—微观—符号是学习化学的基本思维方法。用意义、化学符号、名称完成下列各题:(1)、3Hg;(2)、氨气;(3)、钠离子;(4)、KMnO4。
三、简答题
-
12. 根据物质结构—性质—用途之间的内在联系,回答下列问题:(1)、金刚石比石墨的硬度大得多,原因是;(2)、灯泡里的灯丝材料是钨而不是锡,原因是。
四、计算题
-
13. 近日两家美国采购商控告我国企业制造的维生素C(C6H8O6)涉嫌垄断,中国商务部首次现身美最高法口头辩论,维护我国企业权益。彰显中国力量。维生素C中碳、氢、氧元素的质量比为 , 如图是某品牌维生素C咀嚼片的部分包装说明。其中每片维生素C咀嚼片中含碳g(精确到0.01)。

五、综合题
-
14. 化学与人类生活,生产息息相关。请回答下列问题:(1)、近日,武汉市氢能产业发展规划建议方案提出,将在武汉打造“氢能汽车之都”。氢能汽车使用的是氢燃料电池,其化学原理是利用催化剂使氢气和氧气反应,将化学能直接转化为电能,其化学方程式为 。(2)、油锅着火用锅盖盖灭的原理是。(3)、老年人缺钙易患的疾病是。15. 某化学兴趣小组用一定浓度的稀盐酸和含杂质5%(杂质不与盐酸反应)的石灰石制备CO2 , 他们选择的制取和收集装置如图所示。请按要求回答问题和探究:
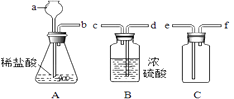 (1)、装置A中仪器a的名称是 , 若要制取并收集干燥的CO2 , 导管的连接顺序是。(2)、若消耗的石灰石为100g,理论上可得到CO2g(精确到0.1),但实际收集到的CO2质量与理论值不符,原因可能是(填一种)。(3)、探究装置A中残留液的溶质成分。
(1)、装置A中仪器a的名称是 , 若要制取并收集干燥的CO2 , 导管的连接顺序是。(2)、若消耗的石灰石为100g,理论上可得到CO2g(精确到0.1),但实际收集到的CO2质量与理论值不符,原因可能是(填一种)。(3)、探究装置A中残留液的溶质成分。【提出问题】残留液中含有哪些溶质?
【查阅资料】CaCl2溶液呈中性。
【思考判断】残留液中一定含有的溶质是(填物质名称),可能含有的溶质是HCl。
【实验验证】同学们通过多种实验方法,均验证了残留液中的溶质有HCl,请完成下表。
实验操作
现象(数据或化学方程式)
结论
方法一
用酸碱指示剂测定溶液的酸碱性,所选择的指示剂为。
现象:
残留液中的溶质有HCl
方法二
用pH试纸测定溶液的pH。
pH 7
(填“>”“=”或“<”)
方法三
用化学药品检测,且发生了复分解反应,可能选用的药品为(填一种物质的化学式)。
现象:
化学方程式:
16. 今年春节期间播出的《舌尖3》,让籍籍无名的章丘铁锅名声大振,章丘手工铁锅制造需要历经十二道工序,再过十八遍火候,一千度高温锤炼,经受三万六千次锻打,其炉渣中主要含FeO、Fe2O3 , 还有一定量既不溶于水,也不与稀酸反应的杂质。现按如图工艺流程,用炉渣制备绿矾(FeSO4•7H2O)。请按要求回答问题: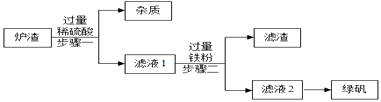
查阅资料:氧化亚铁与稀硫酸、铁与硫酸铁反应均可生成硫酸亚铁。
(1)、步骤一中,发生反应的化学方程式为、 。(2)、步骤一中的操作名称是 , 为提高步骤一的反应速率,可采取的措施有增大硫酸的浓度,升高反应物的温度、还可以采取(写1条,不考虑“搅拌”和“使用催化剂”)。(3)、步骤二中无气体生成的化学反应方程式为 , 测得滤液2的pH明显大于滤液1,其原因是。(4)、滤液2得到绿矾可以采取的方法是。(5)、某化学兴趣小组在实验室中利用该炉渣按照上述工艺流程制取绿矾。现取100g炉渣,得到干燥杂质5g,步骤二中加入15.6g铁粉,得到滤渣5.6g。要计算理论上制得绿矾的质量,除要利用上述给定的全部数据外,在实验过程中,还需测定的一个数据是。
-
-
-