2016年湖北省武汉市江岸区中考化学三模试卷
试卷更新日期:2017-02-17 类型:中考模拟
一、选择题
-
1. 下列变化属于化学变化的是( )A、车胎爆炸 B、高粱酿酒 C、玻璃破碎 D、干冰升华2. 下列说法或做法正确的是( )A、煤气指的是CO B、“二手烟”对人体健康没有影响,因为香烟的烟气中不含对人体有害物质 C、乙醇汽油中添加的乙醇属于可再生能源 D、室内起火,迅速打开所有门窗通风3. 下列有关微粒的说法错误的是( )A、原子、分子、离子都是构成物质的微粒 B、钠原子失去1个电子形成钠离子 C、水电解生成氢气和氧气,说明水中含有氢分子和氧分子 D、空气中的氮气、氧气等分子均匀地混合在一起4. 武汉民生热词:“舌尖上的安全”.下列说法正确的是( )A、为保障食品安全,杜绝使用任何食品添加剂 B、食用“地沟油”对人体有害 C、用亚硝酸钠代替食盐烹调食物 D、用工业酒精勾兑饮用白酒5. 一种焰火火药中所含的硝酸铜在燃放时产生绿色火焰,发生如下反应:2Cu(NO3)2=2CuO+O2↑+4X↑.下列有关说法错误的是( )A、X属于氧化物 B、该反应的基本反应类型为分解反应 C、该反应前后元素的化合价没有发生改变 D、X中氮、氧元素的质量比为7:166. 下列各组变化中,每个转化在一定条件下均能一步实现的是( )
 A、①② B、①③ C、②③ D、①②③7. 将一定量的锌粉加入到硫酸亚铁、硫酸铜和硫酸镁的混合溶液中,过一段时间后过滤,向滤渣中加入稀盐酸有气泡产生,则下列叙述正确的是( )
A、①② B、①③ C、②③ D、①②③7. 将一定量的锌粉加入到硫酸亚铁、硫酸铜和硫酸镁的混合溶液中,过一段时间后过滤,向滤渣中加入稀盐酸有气泡产生,则下列叙述正确的是( )①滤渣中一定含有锌 ②滤渣中一定含有铜,可能含有锌 ③向滤渣中加入稀盐酸,最后溶液一定变成浅绿色 ④滤液中溶质一定含有硫酸锌和硫酸镁
⑤滤液的颜色不可能为浅绿色.
A、①④⑤ B、②④ C、②③④ D、②③④⑤8. 已知碳化铝(固体)与水在常温下剧烈反应Al4C3+12H2O=4Al(OH)3↓+3CH4↑,某同学为了探究甲烷的还原性并检验产物,设计出如下实验: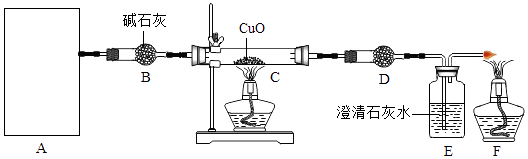
①用碳化铝制取甲烷,可以选择实验室制二氧化碳的装置
②在点燃C中酒精灯前,先要通甲烷气体
③如果D中装无水硫酸铜,可以通过D装置反应前后颜色变化,判断有没有水生成
④由于甲烷无味无毒,所以在该实验中可以不处理尾气
⑤若将D中装碱石灰,在每步充分反应的情况下,可以推断甲烷组成
⑥甲烷与氧化铜在一定条件下反应,产物可能是铜、水和二氧化碳
以上正确说法的是( )
A、①②③⑥ B、①③④⑥ C、①②③⑤ D、②③④⑥二、非选择题
-
9. 根据所学知识填空:(1)、图1是元素周期表中铝元素的相关信息,图2是该元素形成某种微粒的结构示意图.
铝元素原子核外电子数=;图2所表示微粒符号为 .
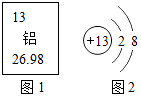 (2)、金属铝在常温下空气中表面能生成一层致密的薄膜,铝具有很好的抗腐蚀性能,该反应的化学方程式为 .10. 如图1所示,A、B、C为三种物质的溶解度曲线,请根据图示信息回答下列问题.
(2)、金属铝在常温下空气中表面能生成一层致密的薄膜,铝具有很好的抗腐蚀性能,该反应的化学方程式为 .10. 如图1所示,A、B、C为三种物质的溶解度曲线,请根据图示信息回答下列问题.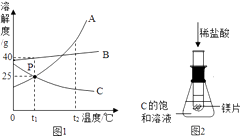 (1)、t1℃时,100克A的饱和溶液中含溶质的质量是 .(2)、t1℃时,将30g B物质投入100g水中,充分溶解,温度不变,所得溶液为溶液(填“饱和”或“不饱和”)(3)、下列说法正确的是 .A、t2℃时,将A和C的混合溶液(两者均已达到饱和),降温至t1℃,析出晶体含有A和C B、t2℃,将A,B,C的饱和溶液分贝降温至t1℃,所得溶液中溶质质量分数的大小关系是B>A>C C、从混有少量A的C物质中提取较纯净的C,可通过升温结晶的方法来实现 D、t1℃时,欲用A的饱和溶液配制10%的A溶液,只需要烧杯、量筒、胶头滴管三种玻璃仪器(4)、如图2所示,向放有镁片的试管中滴加稀盐酸后,锥形瓶中C中的饱和溶液变浑浊,请解释原因 .11. 某无色溶液可能由氯化钙、氢氧化钠、氯化钠、碳酸钠、硫酸钠溶液中的一种或几种混合而成,为探究其组成,小明同学进行了如下实验:
(1)、t1℃时,100克A的饱和溶液中含溶质的质量是 .(2)、t1℃时,将30g B物质投入100g水中,充分溶解,温度不变,所得溶液为溶液(填“饱和”或“不饱和”)(3)、下列说法正确的是 .A、t2℃时,将A和C的混合溶液(两者均已达到饱和),降温至t1℃,析出晶体含有A和C B、t2℃,将A,B,C的饱和溶液分贝降温至t1℃,所得溶液中溶质质量分数的大小关系是B>A>C C、从混有少量A的C物质中提取较纯净的C,可通过升温结晶的方法来实现 D、t1℃时,欲用A的饱和溶液配制10%的A溶液,只需要烧杯、量筒、胶头滴管三种玻璃仪器(4)、如图2所示,向放有镁片的试管中滴加稀盐酸后,锥形瓶中C中的饱和溶液变浑浊,请解释原因 .11. 某无色溶液可能由氯化钙、氢氧化钠、氯化钠、碳酸钠、硫酸钠溶液中的一种或几种混合而成,为探究其组成,小明同学进行了如下实验:①取适量样品放入试管中,滴加酚酞溶液,溶液变成红色,再向试管中逐滴加入过量的氢氧化钡溶液,观察到有白色沉淀A产生,过滤,所得滤液B为红色.
②取白色沉淀A加入过量的稀盐酸,观察到有气泡产生,并且有不溶物.
③取滤液B加入过量的稀硝酸和过量的硝酸银溶液,得到溶液C和白色沉淀
(1)、由实验可知:该样品中一定含有的物质(写化学式,下同),一定不含有的物质是 .(2)、在实验③中加入过量的稀硝酸的目的是;(3)、溶液C中,除了酚酞以外,一定含有的溶质有;(4)、为了进一步探究样品中可能含有的物质确实存在,可以补充实验操作和现象(选其中一种可能含有的物质)。12. 某工厂生产产品Na2CO3中含有少量NaHCO3样品,为了测定产品中Na2CO3质量分数,取20.0g样品进行如图实验,反应的化学方程式为:2NaHCO3 Na2CO3+CO2↑+H2O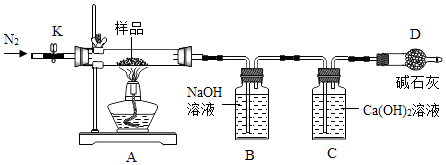
实验步骤如下:①打开K,缓慢通入干燥N2一段时间;
②关闭K,加热至一定温度使之反应.
③实验后,观察到C中的溶液不变浑浊,测得各装置质量如下:
实验前
实验后
玻璃管及样品质量/g
45.5
42.4
B装置质量/g
100.5
103.6
问:
(1)、B中发生反应的化学方程式为:(2)、D装置的作用是(3)、实验过程中,观察到 , 说明A中已反应完全;停止加热后,在冷却过程中要注意的问题 .(4)、根据实验所给数据,可测得Na2CO3质量分数为 .13. 小丽同学取铜和氧化铜的混合物mg置于烧杯中,并向烧杯中逐滴加入稀硫酸溶液,不断搅拌,测得烧杯中溶液的质量与加入稀硫酸的质量关系如图所示.求: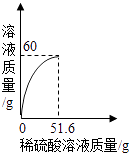 (1)、mg混合物中,氧化铜的质量是克;(2)、当加入51.6g稀硫酸溶液时恰好完全反应,此时溶液中溶质的质量分数.
(1)、mg混合物中,氧化铜的质量是克;(2)、当加入51.6g稀硫酸溶液时恰好完全反应,此时溶液中溶质的质量分数.