2018年高考化学真题分类汇编专题07:原电池与电解池
试卷更新日期:2018-08-01 类型:二轮复习
一、单选题
-
1. 验证牺牲阳极的阴极保护法,实验如下(烧杯内均为经过酸化的3%NaCl溶液)。
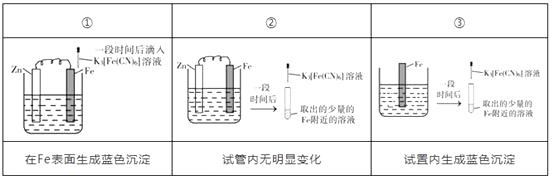
下列说法错误的是( )
A、对比②③,可以判定Zn保护了Fe B、对比①②, k3[Fe(CN)6]可能将Fe氧化 C、验证Zn保护Fe时不能用①的方法 D、将Zn换成Cu,用①的方法可判断Fe比Cu活泼2. 硫酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一,采用湿法冶金工艺回收废旧硫酸亚铁锂电池正极片中的金属,其流程如下:
下列叙述错误的是( )
A、合理处理废旧电池有利于保护环境和资源再利用 B、从“正极片”中可回收的金属元素有Al、Fe、Li C、“沉淀”反应的金属离子为Fe3+ D、上述流程中可用硫酸钠代替碳酸钠3. 我国科学家研发了一种室温下“可呼吸”的Na-CO2二次电池,将NaClO4溶于有机溶剂作为电解液,钠和负载碳纳米管的镍网分别作为电极材料,电池的总反应为:3CO2+4Na 2Na2CO3+C,下列说法错误的是()
 A、放电时,ClO4-向负极移动 B、充电时释放CO2 , 放电时吸收CO2 C、放电时,正极反应为:3CO2+4e-=2CO32-+C D、充电时,正极反应为:Na+ + e- =Na4. 一种可充电锂-空气电池如图所示。当电池放电时,O2与Li+在多孔碳材料电极处生成Li2O2-x(x=0或1)。下列说法正确的是
A、放电时,ClO4-向负极移动 B、充电时释放CO2 , 放电时吸收CO2 C、放电时,正极反应为:3CO2+4e-=2CO32-+C D、充电时,正极反应为:Na+ + e- =Na4. 一种可充电锂-空气电池如图所示。当电池放电时,O2与Li+在多孔碳材料电极处生成Li2O2-x(x=0或1)。下列说法正确的是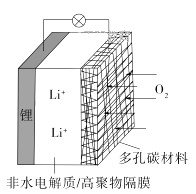 A、放电时,多孔碳材料电极为负极 B、放电时,外电路电子由多孔碳材料电极流向锂电极 C、充电时,电解质溶液中Li+向多孔碳材料区迁移 D、充电时,电池总反应为Li2O2-x=2Li+(1- )O25. 最近我国科学家设计了一种,CO₂+H₂S协同转化装置,实现对天然气中CO₂和H₂S的高效去除。示意图如右所示,其中电极分别为ZnO@石墨烯(石墨烯包裹的ZnO)和石墨烯,石墨烯电极区发生反应为:
A、放电时,多孔碳材料电极为负极 B、放电时,外电路电子由多孔碳材料电极流向锂电极 C、充电时,电解质溶液中Li+向多孔碳材料区迁移 D、充电时,电池总反应为Li2O2-x=2Li+(1- )O25. 最近我国科学家设计了一种,CO₂+H₂S协同转化装置,实现对天然气中CO₂和H₂S的高效去除。示意图如右所示,其中电极分别为ZnO@石墨烯(石墨烯包裹的ZnO)和石墨烯,石墨烯电极区发生反应为: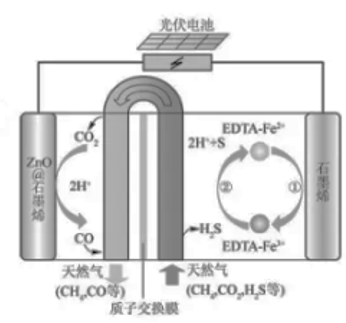
①EDTA-Fe2+-e-=EDTA-Fe3+
②2EDTA-Fe3++H₂S=2H++S+2EDTA+Fe²+
该装置工作时,下列叙述错误的是( )
A、阴极的电极反应:CO₂+2H++2e-=CO+H₂O B、协同转化总反应:CO₂+H₂S=CO+H₂O+S C、石墨烯上的电势比ZnO@石墨烯上的低 D、若采用Fe²+/Fe3+取代EDTA-Fe²+/EDTA-Fe3+ , 溶液需为酸性二、多选题
-
6. 一种镁氧电池如图所示,电极材料为金属镁和吸附氧气的活性炭,电解液为KOH浓溶液。下列说法错误的是( )
 A、电池总反应式为:2Mg + O2 +2H2O =Mg(OH)2 B、正极反应式为:Mg -e- =Mg2 + C、活性炭可以加快O2在负极上的反应速率 D、电子的移动方向由a经外电路到b
A、电池总反应式为:2Mg + O2 +2H2O =Mg(OH)2 B、正极反应式为:Mg -e- =Mg2 + C、活性炭可以加快O2在负极上的反应速率 D、电子的移动方向由a经外电路到b三、综合题
-
7. KIO3是一种重要的无机化合物,可作为食盐中的补碘剂。回答下列问题:(1)、KIO3的化学名称是。(2)、利用“KClO3氧化法”制备KIO3工艺流程如下图所示:
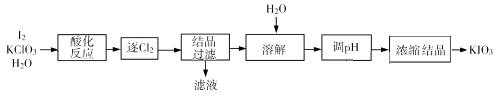
“酸化反应”所得产物有KH(IO3)2、Cl2和KCl。“逐Cl2”采用的方法是。“滤液”中的溶质主要是。“调pH”中发生反应的化学方程式为。
(3)、KClO3也可采用“电解法”制备,装置如图所示。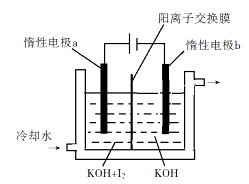
①写出电解时阴极的电极反应式。
②电解过程中通过阳离子交换膜的离子主要为 , 其迁移方向是。
③与“电解法”相比,“KClO3氧化法”的主要不足之处有(写出一点)。
8. CO2是一种廉价的碳资源,其综合利用具有重要意义。回答下列问题:(1)、CO2可以被NaOH溶液捕获。若所得溶液pH=13,CO2主要转化为(写离子符号);若所得溶液c(HCO3−)∶c(CO32−)=2∶1,溶液pH=。(室温下,H2CO3的K1=4×10−7;K2=5×10−11)(2)、CO2与CH4经催化重整,制得合成气:CH4(g)+ CO2(g) 2CO (g)+ 2H2(g)
①已知上述反应中相关的化学键键能数据如下:
化学键
C—H
C=O
H—H
C
 O(CO)
O(CO)键能/kJ·mol−1
413
745
436
1075
则该反应的ΔH=。分别在VL恒温密闭容器A(恒容)、B(恒压,容积可变)中,加入CH4和CO2各1 mol的混合气体。两容器中反应达平衡后放出或吸收的热量较多的是(填“A” 或“B ”)。
②按一定体积比加入CH4和CO2 , 在恒压下发生反应,温度对CO和H2产率的影响如图3所示。此反应优选温度为900℃的原因是。
 (3)、O2辅助的Al~CO2电池工作原理如图4所示。该电池电容量大,能有效利用CO2 , 电池反应产物Al2(C2O4)3是重要的化工原料。
(3)、O2辅助的Al~CO2电池工作原理如图4所示。该电池电容量大,能有效利用CO2 , 电池反应产物Al2(C2O4)3是重要的化工原料。电池的负极反应式:。
电池的正极反应式:6O2+6e−=6O2−
6CO2+6O2−=3C2O42−
反应过程中O2的作用是。
该电池的总反应式:。
9. 焦亚硫酸钠(Na2S2O5)在医药、橡胶、印染、食品等方面应用广泛,回答下列问题:(1)、生产Na2S2O5 , 通常是由NaHSO3过饱和溶液经结晶脱水制得,写出该过程的化学方程式。(2)、利用烟道气中的SO2生产Na2S2O3的工艺为: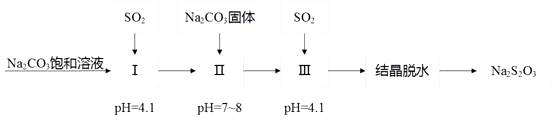 ①pH=4.1时,1中为溶液(写化学式)。
①pH=4.1时,1中为溶液(写化学式)。②工艺中加入Na2CO3 , 固体,并再次充入SO2的目的是。
(3)、制备Na2S2O3 , 也可采用三室膜电解技术,装置如图所示,其中SO2碱吸收液中含有NaHSO2和Na2SO3阳极的电极反应式为 , 电解后,室的NaHSO3浓度增加,将该室溶液进行结晶脱水,可得到Na2S2O3。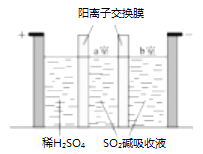 (4)、Na2S2O5可用作食品的抗氧化剂,在测定某葡萄酒中Na2S2O5残留量时,取50.00mL葡萄酒样品,用0.01000mol-L-1的碘标准液滴定至终点,消耗10.00mL,滴定反应的离子方程式为 , 该样品中Na2S2O5的残留量为g·L-1(以SO3计)。
(4)、Na2S2O5可用作食品的抗氧化剂,在测定某葡萄酒中Na2S2O5残留量时,取50.00mL葡萄酒样品,用0.01000mol-L-1的碘标准液滴定至终点,消耗10.00mL,滴定反应的离子方程式为 , 该样品中Na2S2O5的残留量为g·L-1(以SO3计)。
-