2018年高考化学真题分类汇编专题06:化学反应速率和化学平衡
试卷更新日期:2018-08-01 类型:二轮复习
一、多选题
-
1. 一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入反应物,发生反应2SO2(g)+ O2(g) 2SO3(g)(正反应放热),测得反应的相关数据如下:
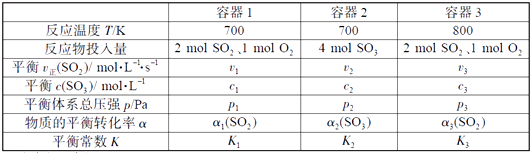
下列说法正确的是( )
A、v1< v2 , c2< 2c1 B、K1> K3 , p2> 2p3 C、v1< v3 , α1(SO2 ) >α3(SO2 ) D、c2> 2c3 , α2(SO3 )+α3(SO2 )<1二、综合题
-
2. 催化重整不仅可以得到合成气(CO和 )。还对温室气体的减排具有重要意义。回答下列问题:(1)、 催化重整反应为: 。
已知:
该催化重整反应的 。有利于提高 平衡转化率的条件是(填标号)。
A.高温低压 B.低温高压 C.高温高压 D.低温低压
某温度下,在体积为2L的容器中加入 以及催化剂进行重整反应。达到平衡时 的转化率是50%,其平衡常数为 。
(2)、反中催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳量减少。相关数据如下表:积碳反应
消碳反应
75
172
活化能/
催化剂X
33
91
催化剂Y
43
72
①由上表判断,催化剂XY(填“优于或劣于”),理由是.在反应进料气组成,压强及反应时间相同的情况下,某催化剂表面的积碳量随温度的变化关系如右图所示,升高温度时,下列关于积碳反应,消碳反应的平衡常数(K)和速率(v)的叙述正确的是(填标号)
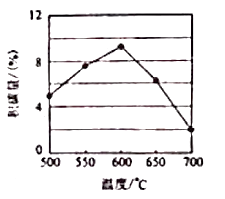
A.K积、K消均增加
B.V积减小、V消增加
C.K积减小、K消增加
D.v消增加的倍数比v积增加的倍数大
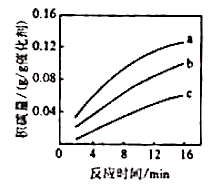
②在一定温度下,测得某催化剂上沉积碳的生成速率方程为 (k为速率常数)。在 一定时,不同 下积碳量随时间的变化趋势如右图所示,则Pa(CO2)、Pb(CO2)、Pc(CO2)从大到小的顺序为
 3. 三氯氢硅(SiHCl3)是制备硅烷、多晶硅的重要原料。回答下列问题:(1)、SiHCl3在常温常压下为易挥发的无色透明液体,遇潮气时发烟生成(HSiO)2O等,写出该反应的化学方程式。(2)、SiHCl3在催化剂作用下发生反应:
3. 三氯氢硅(SiHCl3)是制备硅烷、多晶硅的重要原料。回答下列问题:(1)、SiHCl3在常温常压下为易挥发的无色透明液体,遇潮气时发烟生成(HSiO)2O等,写出该反应的化学方程式。(2)、SiHCl3在催化剂作用下发生反应:2SiHCl3(g)=SiH2Cl2(g)+ SiCl4(g) ΔH1=48 kJ·mol−1
3SiH2Cl2(g)=SiH4(g)+2SiHCl3 (g) ΔH2=−30 kJ·mol−1
则反应4SiHCl3(g)=SiH4(g)+ 3SiCl4(g)的ΔH= kJ·mol−1。
(3)、对于反应2SiHCl3(g)=SiH2Cl2(g)+SiCl4(g),采用大孔弱碱性阴离子交换树脂催化剂,在323 K和343 K时SiHCl3的转化率随时间变化的结果如图所示。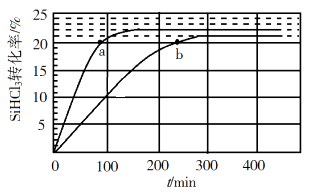
①343 K时反应的平衡转化率α=%。平衡常数K343 K=(保留2位小数)。
②在343 K下:要提高SiHCl3转化率,可采取的措施是;要缩短反应达到平衡的时间,可采取的措施有、。
③比较a、b处反应速率大小:vavb(填“大于”“小于”或“等于”)。反应速率v=v正−v逆= − ,k正、k逆分别为正、逆向反应速率常数,x为物质的量分数,计算a处 =(保留1位小数)。
-