湖北省孝感市2018年中考理综化学试题
试卷更新日期:2018-07-24 类型:中考真卷
一、选择题
-
1. 精准扶贫是当前一项非常重要的工作。下列帮扶措施中主要发生化学变化的是( )A、建立销售网络 B、腐熟农家肥 C、架设电线 D、清理池塘2. 下列实验操作正确的是( )A、熄灭酒精灯
 B、滴加液体
B、滴加液体  C、读取液体体积
C、读取液体体积  D、取用固体药品
D、取用固体药品  3. 下列说法错误的是( )A、熟石灰常用于改良酸性土壤 B、炒菜时油锅着火,可用锅盖盖灭 C、用灼烧的方法可区分羊毛纤维和棉纤维 D、水由液体变为水蒸气其体积变大,是因为水分子本身体积变大4. 食醋是厨房中常用的调味品,它的主要成分是乙酸(CH3COOH)。下列有关乙酸的说法中,正确的是( )A、乙酸是一种化合物 B、乙酸中碳元素的质量分数最大 C、乙酸中共含有8个原子 D、乙酸中碳、氢,氧三种元素的质量比为1:2:15. 下表中对部分知识的归纳完全正确的一组是( )
3. 下列说法错误的是( )A、熟石灰常用于改良酸性土壤 B、炒菜时油锅着火,可用锅盖盖灭 C、用灼烧的方法可区分羊毛纤维和棉纤维 D、水由液体变为水蒸气其体积变大,是因为水分子本身体积变大4. 食醋是厨房中常用的调味品,它的主要成分是乙酸(CH3COOH)。下列有关乙酸的说法中,正确的是( )A、乙酸是一种化合物 B、乙酸中碳元素的质量分数最大 C、乙酸中共含有8个原子 D、乙酸中碳、氢,氧三种元素的质量比为1:2:15. 下表中对部分知识的归纳完全正确的一组是( )A.玻璃棒的作用
B.化学与人体健康
过滤时,引流蒸发时:搅拌,防止液体飞溅
缺乏钙——会引起老年人骨质蔬松
缺乏维生素A——会引起坏血病
C.化学与生活
D.化学与能源
汽油去油污与洗涤剂去油污——原理相同
合金与纯金属——硬度相同
太阳能是清洁能源
石油是可再生的能源
A、A B、B C、C D、D6. 在一定条件下,甲和乙反应生成丙的微观示意图如下。下列说法错误的是( ) A、丙的化学式为C2H6O B、乙和丙都属于氧化物 C、乙是最常用的溶剂 D、该反应的的基本反应类型是化合反应7. 如图是甲、乙、两三种固体物质(均不含结晶水)的溶解度曲线。下列说法正确的是( )
A、丙的化学式为C2H6O B、乙和丙都属于氧化物 C、乙是最常用的溶剂 D、该反应的的基本反应类型是化合反应7. 如图是甲、乙、两三种固体物质(均不含结晶水)的溶解度曲线。下列说法正确的是( )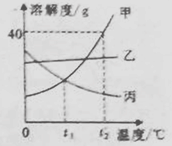 A、甲和丙的溶解度相等 B、在t2℃时,将28g甲物质加入到50g水中,充分溶解后所得溶液的质量为78g C、将t2℃时,甲的饱和溶液降温到t1℃,有晶体析出 D、将t1℃时,甲、乙、丙三种物质的饱和溶液升温至t2℃(不考虑水的蒸发),所得溶液中溶质的质量分数由大到小的顺序是甲>乙>丙8. 除去下列物质中的少量杂质所选的试剂正确的是( )
A、甲和丙的溶解度相等 B、在t2℃时,将28g甲物质加入到50g水中,充分溶解后所得溶液的质量为78g C、将t2℃时,甲的饱和溶液降温到t1℃,有晶体析出 D、将t1℃时,甲、乙、丙三种物质的饱和溶液升温至t2℃(不考虑水的蒸发),所得溶液中溶质的质量分数由大到小的顺序是甲>乙>丙8. 除去下列物质中的少量杂质所选的试剂正确的是( )选项
物质(括号内物质为杂质)
除杂试剂
A
FeCl2溶液(CuCl2)
过量铁粉
B
CO2(CO)
适量氧气
C
盐酸﹙硫酸﹚
适量Ba(NO3)2溶液
D
NaCl (NaOH)
适量稀硫酸
A、A B、B C、C D、D9. 下列图像能正确反映对应变化关系的是( )A、 在一定量的硝酸银和硝酸铜的混合溶液中加入铁粉至过量
B、
在一定量的硝酸银和硝酸铜的混合溶液中加入铁粉至过量
B、 用胃舒平[主要成分Al(OH)3]治疗胃酸过多时胃液pH的情况
C、
用胃舒平[主要成分Al(OH)3]治疗胃酸过多时胃液pH的情况
C、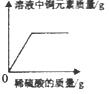 向盛有一定量氧化铜粉末的烧杯中不断加入稀硫酸至过量
D、
向盛有一定量氧化铜粉末的烧杯中不断加入稀硫酸至过量
D、 加热一定量氯酸钾和二氧化锰固体混合物
10. 某固体混合物由硫化钠(Na2S)和亚硫酸钠(Na2SO3)两种物质组成。已知该固体混合物中氧元素的质量分数为22%。则该固体混合物中钠元素的质量分数为( )A、23% B、46% C、50% D、78%
加热一定量氯酸钾和二氧化锰固体混合物
10. 某固体混合物由硫化钠(Na2S)和亚硫酸钠(Na2SO3)两种物质组成。已知该固体混合物中氧元素的质量分数为22%。则该固体混合物中钠元素的质量分数为( )A、23% B、46% C、50% D、78%二、非选择题部分
-
11. 化学与我们的生产和生活密切相关。请用下列五种物质的字母代号填空:
A.活性炭 B.糖类 C.氧气 D. 硝酸钾 E.二氧化碳
(1)、能供给人呼吸的气体是;(2)、大米中含有的主要营养素是;(3)、属于复合肥料的是;(4)、常用于灭火的是;(5)、能除去水中有臭味的物质是。12. 根据下图,回答下列问题: (1)、图A所示中溴的相对原子质量是;(2)、与B的化学性质相似的粒子是(填字母序号);(3)、 D的粒子符号为;(4)、 B与C形成化合物的化学式为。13. 根据如图所示装置,回答有关问题:
(1)、图A所示中溴的相对原子质量是;(2)、与B的化学性质相似的粒子是(填字母序号);(3)、 D的粒子符号为;(4)、 B与C形成化合物的化学式为。13. 根据如图所示装置,回答有关问题: (1)、装置B中,仪器X的名称为;(2)、实验室用大理石和稀盐酸来制取二氧化碳,则选取的发生装置为(填字母序号);
(1)、装置B中,仪器X的名称为;(2)、实验室用大理石和稀盐酸来制取二氧化碳,则选取的发生装置为(填字母序号);
(3)、若用装置C收集氧气,则氧气应从(填“m”或“n”)端导管口通入;
(4)、利用实验室制取二氧化碳的发生装置,还可以制取初中化学常见的气体是(填化学式,任写一种)。14. A、B、C为初中化学常见的三种物质,它们之间有如图所示的转化关系(“→”表示某一种物质经一步反应可转化为另一种物质,部分反应物、生成物及反应条件已略去)。请回答下列问题: (1)、若A为黑色固体,A、B、C的相对分子质量依次增大,目B与C是组成元素相同的两种气体,则C的化学式为;B→C的反应类型(填“一定”或“不一定”)是化合反应。(2)、若A、B、C均为碱,且C为白色沉淀,写出A→B反应的化学方程式:。(3)、若A、B、C是三种不同类别的物质,都含有同一种元素,且组成元素分别为三种、两种和一种,常温下C为气态,则B的化学式为。15. 溶洞都分布在石灰岩组成的山洞中,石灰岩的主要成分是碳酸钙,当遇到溶有二氧化碳的水时,会反应生成溶解性较大的碳酸氢钙: CaCO3+ CO2+ H2O=Ca(HCO3)2。某化学兴趣小组同学们思考:若向碳酸钠溶液中通入一定量二氧化碳,是否能生成碳酸氢钠(NaHCO3)?于是他们开始实验探究。(不考虑二氧化碳和碳酸作为溶质的情况)(1)、[提出问题]所得溶液中所含溶质成分是什么?
(1)、若A为黑色固体,A、B、C的相对分子质量依次增大,目B与C是组成元素相同的两种气体,则C的化学式为;B→C的反应类型(填“一定”或“不一定”)是化合反应。(2)、若A、B、C均为碱,且C为白色沉淀,写出A→B反应的化学方程式:。(3)、若A、B、C是三种不同类别的物质,都含有同一种元素,且组成元素分别为三种、两种和一种,常温下C为气态,则B的化学式为。15. 溶洞都分布在石灰岩组成的山洞中,石灰岩的主要成分是碳酸钙,当遇到溶有二氧化碳的水时,会反应生成溶解性较大的碳酸氢钙: CaCO3+ CO2+ H2O=Ca(HCO3)2。某化学兴趣小组同学们思考:若向碳酸钠溶液中通入一定量二氧化碳,是否能生成碳酸氢钠(NaHCO3)?于是他们开始实验探究。(不考虑二氧化碳和碳酸作为溶质的情况)(1)、[提出问题]所得溶液中所含溶质成分是什么?[查阅资料]碳酸氢钠溶液呈碱性。
[提出猜想]猜想一,溶质为Na2CO3;
猜想二:溶质为NaHCO3;
猜想三:溶质为。
(2)、[设计实验]实验步骤
实验现象
实验结论
①取所得溶液少许于试管中, 向其中滴加过量的CaCl2溶液
有白色沉淀生成
猜想二(填“成立”或“不成立”)
②取实验步骤①中上层清液,滴加适量稀盐酸
有气泡冒出
猜想一不成立
(3)、[得出结论]猜想三成立,证明二氧化碳通入碳酸钠溶液生成了碳酸氢钠。写出实验步骤②中发生反应的化学方程式:。
(4)、[讨论交流]碳酸氢钠的俗名叫。小明同学认为,向碳酸钠溶液中通入一定量二氧化碳后,再向所得溶液中滴加几滴酚酞溶液。溶液变红就能证明一定有碳酸氢钠生成;小红同学对小明同学的结论产生质疑,其理由是。
(5)、[拓展应用]同学们回忆超实验室用澄清石灰水检验二氧化碳的情景,结合上述知识,如果向一定量的澄清石灰水中不断通入二氧化碳气体,下列哪一个图像能正确反映生成的碳酸钙沉淀与二氧化碳的质量之间的变化关系(填字母序号)。 16. 某化学兴趣小组同学们与老师一起探究铝的化学性质时发现, 铝还能与氢氧化钠溶液反应,其反应的化学方程式为:2Al+ 2NaOH+ 2H2O=2NaAlO2 +3H2↑。现取某氢氧化钠溶液样品50g例入烧杯中,再向其中放入足量打磨好的铝片,生成气体质量与加入铝片质量的变化关系如图所示。
16. 某化学兴趣小组同学们与老师一起探究铝的化学性质时发现, 铝还能与氢氧化钠溶液反应,其反应的化学方程式为:2Al+ 2NaOH+ 2H2O=2NaAlO2 +3H2↑。现取某氢氧化钠溶液样品50g例入烧杯中,再向其中放入足量打磨好的铝片,生成气体质量与加入铝片质量的变化关系如图所示。
试回答下列问题:
(1)、反应完成后生成氢气的质量为g。(2)、求原氢氧化钠溶液中氢氧化钠的质量分数为多少。(请写出计算过程)