2018年内蒙古呼和浩特市中考化学试卷试题
试卷更新日期:2018-07-24 类型:中考真卷
一、选择题
-
1. 下列碳单质的用途与其化学性质有关的是( )A、用石墨制作干电池的电极 B、用碳素笔书写档案文件 C、用活性炭做饮水机的净水剂 D、用铅笔芯粉末使生锈的锁头容易开启2. 铷元素在元素周期表中的信息与铷原子结构示意图如图所示,下列说法错误的是( )
 A、m=37,n=1 B、铷原子的相对原子质量是85.468 C、氧化铷的化学式为RbO D、铷原子的质量主要由构成其原子核的质子和中子的质量决定3. 下列说法正确的是( )A、军事上用镁粉制作照明弹 B、煤的干馏与石油的分馏化学原理相同 C、用石蕊试纸测定橙汁的pH D、在实验室用稀硫酸和块状大理石制取二氧化碳4. 下列对客观事实的解释正确的是( )
A、m=37,n=1 B、铷原子的相对原子质量是85.468 C、氧化铷的化学式为RbO D、铷原子的质量主要由构成其原子核的质子和中子的质量决定3. 下列说法正确的是( )A、军事上用镁粉制作照明弹 B、煤的干馏与石油的分馏化学原理相同 C、用石蕊试纸测定橙汁的pH D、在实验室用稀硫酸和块状大理石制取二氧化碳4. 下列对客观事实的解释正确的是( )选项
事实
解释
A
Fe、Fe2+、Fe3+化学性质不同
微粒中的质子数不同
B
水通电产生氢气和氧气
在化学变化中分子可分,原子不可分
C
稀盐酸、稀硫酸均显酸性
溶液中都含有氢元素
D
冰水混合物属于纯净物
冰和水都含有相同原子
A、A B、B C、C D、D5. 甲、乙、丙是初中化学常见的三种物质,其相互转化关系如图,通常甲为固态单质,乙、丙为两种气体,且所含元素种类相同,乙易与血液中的血红蛋白结合。下列说法错误的是( ) A、丙能产生温室效应 B、①②④三个转化的反应中有一种相同的反应物 C、③的转化只能通过和氧气反应来实现 D、乙和丙化学性质不同是由于其分子构成不同6. 甲和乙可以合成清洁燃料丙,微观过程如图所示。下列说法错误的是( )
A、丙能产生温室效应 B、①②④三个转化的反应中有一种相同的反应物 C、③的转化只能通过和氧气反应来实现 D、乙和丙化学性质不同是由于其分子构成不同6. 甲和乙可以合成清洁燃料丙,微观过程如图所示。下列说法错误的是( )

A、丙物质中碳元素的质量分数最大 B、丙物质属于有机物,可用作溶剂和消毒剂 C、该反应中共有三种氧化物 D、该反应中参加反应的甲乙两种物质的分子个数比为1:27. 下列实验设计不能达到实验目的是( )选项
A
B
C
D
实验目的
除去CO中的CO2 , 并回收CO
探究可燃物燃烧所需的条件
除去氧化铜粉末中的铜粉
鉴别NH4NO3、CuSO4和NaCl三种白色粉末
实验设计

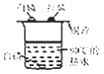
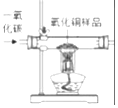
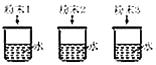 A、A B、B C、C D、D8. 黄铁矿的主要成分为二硫化亚铁(FeS2),工业上可利用黄铁矿煅烧的产物冶炼铁和生产浓硫酸,其工业流程如图:
A、A B、B C、C D、D8. 黄铁矿的主要成分为二硫化亚铁(FeS2),工业上可利用黄铁矿煅烧的产物冶炼铁和生产浓硫酸,其工业流程如图:
下列说法错误的是( )
A、反应②不是置换反应,反应③④为化合反应 B、反应①中各元素的化合价均发生了改变 C、该工业生产过程产生的废气中的SO2可以用熟石灰溶液吸收 D、向制得的100克98%的浓硫酸中加入100克蒸馏水,配制49%的稀硫酸9. 下列四个图象不能正确反映对应变化关系的是( )A、 向一定量的氧化铜粉末中逐渐加入稀硫酸至过量
B、
向一定量的氧化铜粉末中逐渐加入稀硫酸至过量
B、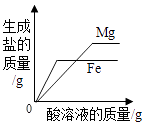 向等质量的镁粉和铁粉中分别逐滴加入同浓度的稀盐酸至过量
C、
向等质量的镁粉和铁粉中分别逐滴加入同浓度的稀盐酸至过量
C、 在饱和石灰水中加入少量生石灰
D、
在饱和石灰水中加入少量生石灰
D、 在密闭容器中用红磷测定空气中氧气的含量
10. 实验室中同学们进行了如图所示实验,成功探究出了久置氢氧化钠固体的变质情况。下列说法正确的是( )
在密闭容器中用红磷测定空气中氧气的含量
10. 实验室中同学们进行了如图所示实验,成功探究出了久置氢氧化钠固体的变质情况。下列说法正确的是( ) A、甲溶液可以选择稀盐酸或CaCl2溶液(查阅资料得知:CaCl2溶液显中性) B、若Ⅱ、Ⅲ均有明显现象,则说明样品部分变质 C、D物质可能是气体,也可能是沉淀 D、溶液B中的溶质一定只含有NaOH和甲
A、甲溶液可以选择稀盐酸或CaCl2溶液(查阅资料得知:CaCl2溶液显中性) B、若Ⅱ、Ⅲ均有明显现象,则说明样品部分变质 C、D物质可能是气体,也可能是沉淀 D、溶液B中的溶质一定只含有NaOH和甲二、填空题
-
11. 生活中处处有化学。请用下列物质的序号填空:
①氮气②氢气③氯气④明矾⑤小苏打⑥烧碱
(1)、用于自来水杀菌消毒的是;(2)、填充探空气球的理想气体是;(3)、用于治疗胃酸过多的是。12. 古往今来,金属材料和制品在我们的社会生活中一直起者非常重要的作用。(1)、考古工作者发现铁质的出土文物往往锈蚀严重,铁生锈的条件是。在实验室常用稀盐酸清除铁锈,化学方程式为。(2)、近年来,我国高铁建设促进了经济、社会的快速发展。制造铁轨的材料是合金钢,主要原因是合金钢具有的优越性能(要求只答一条)。(3)、某同学在实验室进行了两个有关金属性质的实验:实验Ⅰ:硫酸铝溶液和铁粉混合
实验Ⅱ:硫酸铜溶液与铁粉混合
在上述两个实验结束后,该同学将实验Ⅰ和Ⅱ的物质全部倒入同一个烧杯中,发现烧杯内的红色固体明显增多,原因是(用文字说明)。一段时间后过滤,向滤渣中滴加盐酸,结果没有气泡产生。那么,滤液中所含金属离子的情况可能是(填写序号)。
①Al3+②Al3+、Fe2+③Al3+、Fe3+④Fe2+、Cu2+⑤Al3+、Fe2+、Cu2+
13. 某同学将甲乙固体各30克分别加入100克水中后,进行了如图1所示的实验。甲乙两种固体的溶解度曲线如图2所示。
请回答:
(1)、10℃时,甲乙两种物质的溶解度大小关系:甲乙〔填“<““>”或“=”)。(2)、m的取值范围。(3)、40℃时,取等质量的甲乙两种物质的饱和溶液分别蒸发等量的水后,恢复到40℃.下列说法正确的是 (填字母)。A、恢复到原温度后,溶液中溶剂的质量:甲=乙 B、恢复到原温度后,析出晶体的质量:乙>甲 C、若再降温到20℃时,溶液的质量:甲>乙 D、若再降温到20℃时,溶液的溶质质量分数:甲=乙三、实验题
-
14. 如图为实验室中常用装置。

请回答下列问题:
(1)、仪器①的名称。(2)、实验室用氯酸钾和二氧化锰制取并收集较纯净的氧气,所选用的装置是(填装置字母),该反应的化学方程式为。若要从充分加热后的剩余固体中回收二氧化锰,正确的实验操作顺序是。(3)、通常状况下,氨气是一种无色、有强烈刺激性气味的污染性气体,极易溶解于水形成氨水,相同条件下密度比空气小。实验室中可以用浓氨水与生石灰制取氨气。请从如图中选出合适的仪器连接成一套制备并收集氨气的装置。则装置的接口连接顺序是→f.上述实验中,E装置的作用是。15. 根据大量的实验总结得出酸碱盐之间相互发生复分解反应的条件是:生成物中有沉淀、气体或水。依据该条件,某化学小组的同学推断稀硫酸和氯化镁溶液不能发生复分解反应。为了进一步确认该推断的可靠性,该小组同学将一定量稀硫酸和一定量氯化镁溶液在烧杯中混合后,进行了如下探究活动。(1)、甲同学取烧杯中混合溶液分别进行以下两个实验,记录实验现象如下。请依据实验现象填写实验结论:实验
实验现象
实验结论

溶液变红
溶液中含有(写离子符号)

产生白色沉淀
溶液中含有(写离子符号)
【甲同学的结论】稀硫酸与氯化镁溶液没有发生反应
(2)、乙同学看到甲同学的实验报告后,认为甲同学的结论错误,原因是。为了进一步确认两者没发生反应,还需检验烧杯内的混合液中是否含有氯化镁。于是,乙同学设计了如下两个实验:①取少量烧杯内的混合液于试管中,逐滴加入过量的溶液,证明了混合液中含有Mg2+ . 整个实验过程中乙同学观察到的实验现象是。
②乙同学另取少量烧杯内的混合液,通过实验成功地检验出混合液中含有Cl﹣ . 他设计的方案为
(写出操作和现象)。
【总结】通过上述实验,该小组同学证明了稀硫酸和氯化镁溶液确实没有发生反应。
四、计算题
-
16. 实验室中发现一瓶因长期放置而被氧化的铝粉。取6.0克铝粉样品,将100克稀硫酸逐滴加入其中,固体质量随加入硫酸溶液质量的变化情况如图所示,实验过程中测得产生氢气0.1克。请计算:

(1)、样品中铝单质的质量。(写出计算过程)。(2)、硫酸溶液的溶质质量分数为