江苏省苏州市2018年中考化学试卷
试卷更新日期:2018-07-24 类型:中考真卷
一、 选择题
-
1. 2018世界环境日中国确定的主题是“美丽中国,我是行动者”,下列做法符合这一主题的是( )A、作物秸秆露天焚烧 B、废旧塑料随意丢弃 C、 废旧电池就地填埋 D、生活垃圾分类回收2. 新能源的开发利用是人类社会可持续发展的重要课题。下列属于新能源的是( )A、天然气 B、石油 C、氢气 D、煤3. 下列物质属于纯净物的是( )A、空气 B、生铁 C、硬水 D、氧气4. 下列化学仪器对应的名称正确的是( )A、
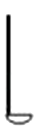 燃烧匙
B、
燃烧匙
B、 分液漏斗
C、
分液漏斗
C、 试管夹
D、
试管夹
D、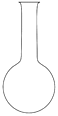 烧杯
5. 下列变化属于化学变化的是( )A、冰雪融化 B、光合作用 C、汽油挥发 D、铁丝弯曲6. 下列过程吸收热量的是( )A、氢氧化钠固体溶于水 B、硝酸铵固体溶于水 C、把水加入生石灰中 D、氡氧化钠溶液与稀硫酸反应7. 下列有关化学用语表示正确的是( )A、氯原子结构示意图:
烧杯
5. 下列变化属于化学变化的是( )A、冰雪融化 B、光合作用 C、汽油挥发 D、铁丝弯曲6. 下列过程吸收热量的是( )A、氢氧化钠固体溶于水 B、硝酸铵固体溶于水 C、把水加入生石灰中 D、氡氧化钠溶液与稀硫酸反应7. 下列有关化学用语表示正确的是( )A、氯原子结构示意图: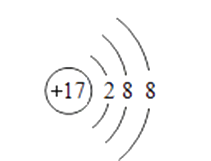 B、2个氢离子: 2H2+
C、酒精的化学式C2H6O
D、氧化钠中氧元素是-2价:
8. 化学让我们的生活更美好,科学家为此作出了很大的努力,其中在制碱工业作出巨大贡献的是( )A、拉瓦锡 B、门捷列夫 C、汤姆生 D、侯德榜9. 下列人体所缺元素与引起的健康问题关系正确的是( )
B、2个氢离子: 2H2+
C、酒精的化学式C2H6O
D、氧化钠中氧元素是-2价:
8. 化学让我们的生活更美好,科学家为此作出了很大的努力,其中在制碱工业作出巨大贡献的是( )A、拉瓦锡 B、门捷列夫 C、汤姆生 D、侯德榜9. 下列人体所缺元素与引起的健康问题关系正确的是( )
A、缺铁会引起贫血 B、缺碘会引起龋齿 C、缺锌会导致甲状腺疾病 D、缺钙会引起坏血病10. 水是生命之源,下列物质的化学式可用"H2O"表示的是( )A、冰 B、可燃冰 C、干冰 D、水银11. 下列气体的排放会导致酸雨形成的是( )A、N2 B、CO C、SO2 D、O212. 下列标志属于中国节能标志的是( )A、 B、
B、 C、
C、 D、
D、 13. 下列关于浓硫酸的说法正确的是A、易挥发 B、有腐蚀性 C、无吸水性 D、密度比水小14. 下列有关物质用途的说法正确的是( )A、明矾可用作净水剂 B、聚氯乙烯可用来包装食品 C、氢氧化钠可用来治疗胃酸过多 D、铝制容器可用来长期存放酸性食物15. 下列有关实验现象的描述正确的是( )A、红磷在空气中燃烧,产生大量白色烟雾 B、用粗砂纸打磨后的铝片放入硫酸铜溶液中,一段时间后,划痕处出现红色物质 C、铁丝在氧气中剧烈燃烧,火星四射,生成红色固体 D、向滴有石蕊的稀盐酸中滴加氢氧化钠溶液至过量,溶液有蓝色变紫色再变红色16. 下列实验操作正确的是( )A、
13. 下列关于浓硫酸的说法正确的是A、易挥发 B、有腐蚀性 C、无吸水性 D、密度比水小14. 下列有关物质用途的说法正确的是( )A、明矾可用作净水剂 B、聚氯乙烯可用来包装食品 C、氢氧化钠可用来治疗胃酸过多 D、铝制容器可用来长期存放酸性食物15. 下列有关实验现象的描述正确的是( )A、红磷在空气中燃烧,产生大量白色烟雾 B、用粗砂纸打磨后的铝片放入硫酸铜溶液中,一段时间后,划痕处出现红色物质 C、铁丝在氧气中剧烈燃烧,火星四射,生成红色固体 D、向滴有石蕊的稀盐酸中滴加氢氧化钠溶液至过量,溶液有蓝色变紫色再变红色16. 下列实验操作正确的是( )A、 闻气体气味
B、
闻气体气味
B、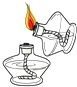 点燃酒精灯
C、
点燃酒精灯
C、 过滤
D、
过滤
D、 移走蒸发皿
17. 下列关于糖类、蛋白质、油脂和维生素的说法正确的是( )A、淀粉没有甜味,因此不属于糖类 B、维生素是人体不可缺少的营养物质 C、油脂属于有机高分子化合物 D、蛋白质中只含有碳、氢、氧三种元素18. 《茉莉花》是一首脍炙人口的苏南民歌。茉莉花香气的成分有多种,乙酸苯甲酯(C9H10O2)是其中的一种。下列关于乙酸苯甲酯的说法正确的是( )
移走蒸发皿
17. 下列关于糖类、蛋白质、油脂和维生素的说法正确的是( )A、淀粉没有甜味,因此不属于糖类 B、维生素是人体不可缺少的营养物质 C、油脂属于有机高分子化合物 D、蛋白质中只含有碳、氢、氧三种元素18. 《茉莉花》是一首脍炙人口的苏南民歌。茉莉花香气的成分有多种,乙酸苯甲酯(C9H10O2)是其中的一种。下列关于乙酸苯甲酯的说法正确的是( )
A、乙酸苯甲酯的相对分子质量为150g B、乙酸苯甲酯由碳、氢、氧三种元素组成 C、乙酸苯甲酯中碳、氢、氧三种元素质量比为9: 10: 2 D、乙酸苯甲酯分子由碳原子、氢原子、氧分子构成19. 下列说法正确的是( )A、空气中氧气的体积分数约为21% B、洗涤油污可用汽油乳化 C、电解水实验说明水是由氢气和氧气组成的 D、可燃物只要与氧气充分接触就能燃烧20. 某溶液中存在较多的H+、SO42-、 Cl- , 该溶液中还可能大量存在的离子是( )A、OH- B、Ba2+ C、NH4+ D、Ag+21. 高锰酸钾和浓盐酸发生如下反应: 2KMnO4 + 16HCl = 2KCl +2MnCl2 + 5X↑+8H2O根据质量守恒定律,推测X应是( )
A、HClO B、ClO2 C、O2 D、Cl222. 下列实验方案能达到目的的是( )A、用氢氧化钠溶液除去二氧化碳中的氯化氢 B、用硫酸铜溶液检验葡萄糖的存在 C、用稀硫酸除去铜屑中的少量铁屑 D、用碳酸钾溶液去区别石灰水和氯化钙溶液23. 下图所示的化学反应基本类型是( )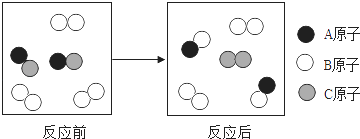 A、化合反应 B、分解反应 C、置换反应 D、复分解反应24. 下列选项所示的物质间转化均能一步实现的是( )A、Cu CuSO4 Cu(OH)2 B、S SO2 H2SO4 C、Fe FeCl3 AgCl D、C CO2 CaCO325. 一定质量的某有机化合物完全燃烧,生成2.2gCO2和1.8gH2O,另取3.2g该有机化合物在O2中完全燃烧,消耗4.8g O2 , 该有机化合物的化学式可能是( )
A、化合反应 B、分解反应 C、置换反应 D、复分解反应24. 下列选项所示的物质间转化均能一步实现的是( )A、Cu CuSO4 Cu(OH)2 B、S SO2 H2SO4 C、Fe FeCl3 AgCl D、C CO2 CaCO325. 一定质量的某有机化合物完全燃烧,生成2.2gCO2和1.8gH2O,另取3.2g该有机化合物在O2中完全燃烧,消耗4.8g O2 , 该有机化合物的化学式可能是( )
A、C2H4 B、CH4O C、CH4 D、C2H4O26. 请用线段连接有对应关系的相邻两行间的点(每个点只能连接1次)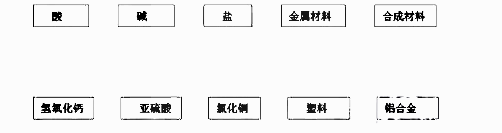 27. 生活中处处有化学,化学已渗透到我们的“衣、食、住、行、医”中。(1)、衣:区分羊毛线和棉纱线的方法是灼烧,羊毛线燃烧时能闻到(2)、食:维生素C能增强人体对疾病的抵抗能力,中学生每天要补充60mg的维生素C,‘下 列物质富含维生素C的是 _ (填字母)。A、橙子 B、猪肉 C、面粉(3)、住:下列属于直接利用太阳能辐射加热物体而获得热能的是 _ (填字母)。A、石蜡燃烧 B、太阳能热水器 C、燃料电池(4)、行:城市交通中大力推广新能源汽车对于改善空气质量的好处是_ _ _ _(5)、医:出现低血糖症状时需要尽快补充葡萄糖,葡萄糖的化学式 _ _ _ _28. 根据下列反应事实写出相应的化学方程式。(1)、稀硫酸与锌粒反应制氢气: ,(2)、金属铝与氧气反应生成氧化膜:;(3)、碳酸钙在高温下分解:;(4)、石灰水与硫酸铜溶液反应:;(5)、甲烷在足量氧气中充分燃烧:;29. 硝酸钾是实验室常见的一种试剂。
27. 生活中处处有化学,化学已渗透到我们的“衣、食、住、行、医”中。(1)、衣:区分羊毛线和棉纱线的方法是灼烧,羊毛线燃烧时能闻到(2)、食:维生素C能增强人体对疾病的抵抗能力,中学生每天要补充60mg的维生素C,‘下 列物质富含维生素C的是 _ (填字母)。A、橙子 B、猪肉 C、面粉(3)、住:下列属于直接利用太阳能辐射加热物体而获得热能的是 _ (填字母)。A、石蜡燃烧 B、太阳能热水器 C、燃料电池(4)、行:城市交通中大力推广新能源汽车对于改善空气质量的好处是_ _ _ _(5)、医:出现低血糖症状时需要尽快补充葡萄糖,葡萄糖的化学式 _ _ _ _28. 根据下列反应事实写出相应的化学方程式。(1)、稀硫酸与锌粒反应制氢气: ,(2)、金属铝与氧气反应生成氧化膜:;(3)、碳酸钙在高温下分解:;(4)、石灰水与硫酸铜溶液反应:;(5)、甲烷在足量氧气中充分燃烧:;29. 硝酸钾是实验室常见的一种试剂。
(1)、硝酸钾是由和构成的(填写微粒符号)。
(2)、硝酸钾中钾元素的质量分数是(结果用百分数表示,保留到0.1%)。(3)、如图是硝酸钾的溶解度曲线,由图可以总结出硝酸钾的溶解度随温度变化的趋势是。60℃时110g硝酸钾溶于100g水中形成的溶液是 ( 选填“饱和“或“不饱和”)溶液,将此时配得的溶液降温至20℃,析出硝酸钾晶体的质量是g。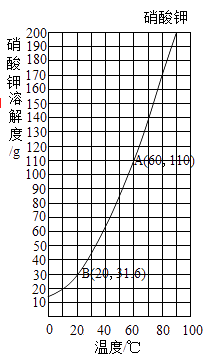
温度/℃
(4)、列式计算:用100g10%的硝酸钾溶液配制5%的硝酸钾溶液。需要加水多少亳升? (水的密度为1.0g·mL-1)30. 从大理石(主要杂质是氧化铁)中提纯碳酸钙的一种实验流程如下: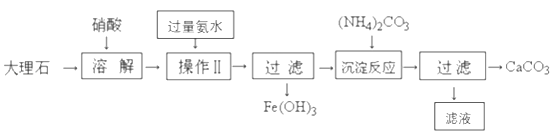 (1)、反应池I中用硝酸不用稀硫酸的主要原因是(2)、反应池II中加入氨水的日的是
(1)、反应池I中用硝酸不用稀硫酸的主要原因是(2)、反应池II中加入氨水的日的是
(3)、反应池II生成碳酸钙的化学方程式是
(4)、过滤II中所得滤液在农业生产中的一种用途是31. 化学是一门以实验为基础的科学,化学实验和科学探究离不开实验装置。制取气体的常用
装置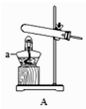


收集气体的常用
装置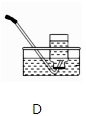
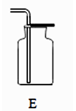
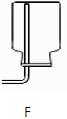
干燥气体的常用
装置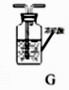
 (1)、制取气体实验时,首先要对发生的装置进行气密性检查,确保装置不漏气,装置C气密性检查的方法是(2)、收集某种气体的方法,主要取决于这种气体的性质,装置E所示的收集方法是_被收集的气体密度空气密度(选填*>”,“<”,“=”)(3)、实验室用大理石与稀盐酸制取并收集一 瓶干燥的二氧化碳,所选装置符合题意的连接顺序是→→→(填装置编号),(4)、、下图所以一氧化碳与氧化铁的反应装置中,虚线方框内装置的作用有。
(1)、制取气体实验时,首先要对发生的装置进行气密性检查,确保装置不漏气,装置C气密性检查的方法是(2)、收集某种气体的方法,主要取决于这种气体的性质,装置E所示的收集方法是_被收集的气体密度空气密度(选填*>”,“<”,“=”)(3)、实验室用大理石与稀盐酸制取并收集一 瓶干燥的二氧化碳,所选装置符合题意的连接顺序是→→→(填装置编号),(4)、、下图所以一氧化碳与氧化铁的反应装置中,虚线方框内装置的作用有。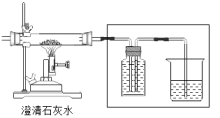 32.(1)、控制变量,设计对比试验是实验探究的重要方法。
32.(1)、控制变量,设计对比试验是实验探究的重要方法。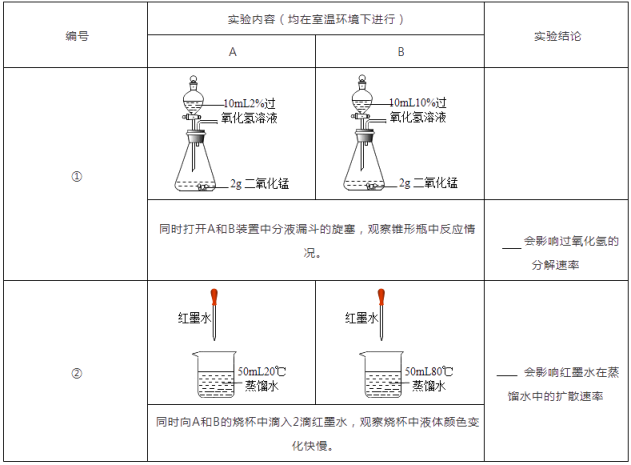 (2)、观察是学习化学的重要方法。
(2)、观察是学习化学的重要方法。探究小组进行如下实验,发现均有红棕色二氧化氮气体产生。
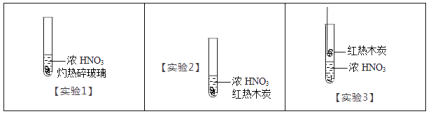
查阅资料:
①【实验一】中所用水玻璃与浓硝酸不发生化学反应,灼热的碎玻璃在实验中起到的作用是
②【实验二】中有红棕色气体产生,能否证明实验二】中木炭与浓硝酸发生了反应?氢做出判断,并说明理由
③【实验三】中发现红热的木炭表面有红棕色气体产生,且生成的气体产物中检测出二氧化碳(体积分数大于0.03%),能否证明【实验三】中木炭与浓硝酸发生了反应?请做出判断,并说明理由
33. 探究碳酸氢钠、碳酸钠分别与稀盐酸反应,研究小组进行如下两个实验:(1)、【实验一】同时将足量的稀盐酸倒入锥形瓶甲和锥形瓶乙中。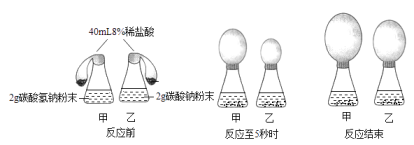
反应至5s生成气体的速率:碳酸氢钠碳酸钠(选填“>”、“<”或“=”)
(2)、【实验二】分别将足量的稀盐酸逐滴滴入试管甲和试管乙中,边滴边震荡
现象为:
①试管甲中的溶液开始时显浅红色,逐滴滴加稀盐酸立即产生大量气泡,浅红色逐渐消失。
②试管乙中的溶液开始时显红色,滴入稀盐酸没有气泡产生,溶液颜色逐渐变为浅红色后,继续滴加稀盐酸有大量气泡产生,浅红色逐渐消失。
【反思1】在【实验二】碳酸钠溶液中逐滴滴加入稀盐酸,为何刚开始没有大量气泡产生?研究小组查阅资料,绘制出微观示意图。
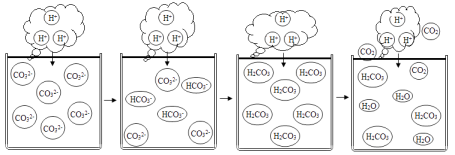
①碳酸钠溶液中逐滴滴加稀盐酸,一次发生反应的化学方程式为:、
②相同浓度的碳酸氢钠溶液和碳酸钠溶液的碱性:碳酸氢钠碳酸钠(选填“>”、“<”或“=”)
(3)、【反思2】为何【实验一】中碳酸氢钠最终产生气体的体积较大?请你列式计算:【实验一】中两种固体完全反应后产生气体的质量各是多少?(写出计算过程,结果保留到0.1g)