湖南省岳阳市2018年中考化学试题
试卷更新日期:2018-07-10 类型:中考真卷
一、选择题
-
1. 下列属于化学变化的是( )A、汽油挥发 B、酒精燃烧 C、胆矾破碎 D、干冰升华
-
2. 地壳中含量最多的元素是( )A、Si B、Al C、O D、Fe
-
3. 化学是一门以实验为基础的科学。下列实验操作正确的是( )A、
 倾倒液体
B、
倾倒液体
B、 塞紧橡胶塞
C、
塞紧橡胶塞
C、 配置溶液
D、
配置溶液
D、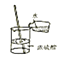 稀释浓硫酸
稀释浓硫酸
-
4. 下列各图中“●”和“○”分别表示不同元素的原子,其中表示混合物的是( )A、
 B、
B、 C、
C、 D、
D、
-
5. 汨罗长乐甜酒,香醇扑鼻。我们能闻到甜酒香的原因是( )A、分子的质量和体积都很小 B、分子是由原子构成的 C、分子间有间隔 D、分子在不断运动
-
6. 下列有关实验现象的描述,正确的是( )A、红磷在空气中燃烧产生大量白雾 B、木炭在空气中燃烧生成二氧化碳 C、硫在空气中燃烧发出蓝紫色火焰 D、铁丝在氧气中燃烧生成黑色固体
-
7. 市售的加碘盐是在食盐中加入一定量的碘酸钾(KIO3),在碘酸钾中碘元素的化合价是( )A、+5 B、+1 C、﹣1 D、+7
-
8. 空气是一种宝贵的自然资源。下列有关空气的说法错误的是( )A、氮气的化学性质不活泼,可用于食品的防腐 B、燃烧法测定空气中氧气的含量,不能用硫代替红磷 C、空气的成分按质量计算,氧气大约占21% D、禁止燃放烟花爆竹,可以减少空气污染
-
9. 硒是人体必需的一种微量元素,严重缺硒可能诱发皮肤病和癌症。硒的原子结构示意图及其在元素周期表中的某些信息如图所示,下列分析正确的是( )
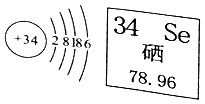 A、硒属于金属元素 B、硒的相对原子质量为78.96g C、硒原子的核电荷数为34 D、硒原子的核外有6个电子
A、硒属于金属元素 B、硒的相对原子质量为78.96g C、硒原子的核电荷数为34 D、硒原子的核外有6个电子 -
10. 下列探究燃烧条件的实验中,只能得出“燃烧需要温度达到可燃物的着火点”的是( )
A、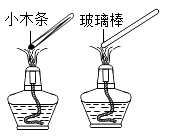 B、
B、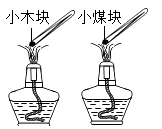 C、
C、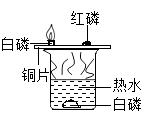 D、
D、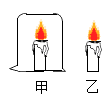
-
11. 推理是化学学习中常用的思维方法。下列推理判断正确的是( )A、某物质在空气中燃烧生成水,所以该物质中一定含有氢元素 B、中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 C、氧化物都含有氧元素,所以含有氧元素的化合物一定是氧化物 D、碱溶液定呈碱性,所以呈碱性的溶液一定是碱溶液
-
12. 甲、乙、丙三种固体物质的溶解度曲线如图所示。下列说法正确的是( )
 A、a2℃时,三种物质的溶解度由大到小的顺序是:甲=乙>丙 B、乙中含有少量甲时,可用冷却热饱和溶液的方法提纯乙 C、a1℃时,将30g乙加入50g水中充分溶解,所得溶液中溶质与溶剂的质量比为3:5 D、将a3℃甲、乙、丙三种物质的饱和溶液分别降温至a2℃,所得溶液的溶质质量分数由大到小的顺序是:甲>丙>乙
A、a2℃时,三种物质的溶解度由大到小的顺序是:甲=乙>丙 B、乙中含有少量甲时,可用冷却热饱和溶液的方法提纯乙 C、a1℃时,将30g乙加入50g水中充分溶解,所得溶液中溶质与溶剂的质量比为3:5 D、将a3℃甲、乙、丙三种物质的饱和溶液分别降温至a2℃,所得溶液的溶质质量分数由大到小的顺序是:甲>丙>乙 -
13. 甲、乙、丙、丁四种金属,只有丙在自然界中主要以单质形式存在,用甲制的容器不能盛放丁盐的水溶液,用乙制的容器却可以盛放丁盐的水溶液。由此推断四种金属的活动性由强到弱的顺序是( )
A、丙>乙>甲>丁 B、甲>丁>乙>丙 C、丁>甲>乙>丙 D、甲>乙>丁>丙 -
14. 下列实验操作不能达到实验目的是( )
选项
实验目的
实验操作
A
鉴别棉纤维、羊毛纤维和涤纶
点燃后闻气味
B
鉴别KOH、(NH4)2SO4、BaCl2、HCl四种溶液
不另加试剂
C
除去铁粉中少量的铜粉
加足量盐酸,过滤、洗涤、干燥
D
除去氧化钙中少量的碳酸钙
高温煅烧
A、A B、B C、C D、D -
15. 下列图象中有关量的变化趋势正确的是( )
 A、①图向一定量的盐酸和氯化钡的混合溶液中,逐渐滴加碳酸钾溶液至过量 B、②图加热等质量的两份氯酸钾,一份加入二氧化锰,一份不加入二氧化锰 C、③图一定量的硫粉与过量的氧气在密闭容器内点燃并充分反应 D、④图向一定量的氯化亚铁和氯化铜的混合溶液中,逐渐加入镁粉至过量
A、①图向一定量的盐酸和氯化钡的混合溶液中,逐渐滴加碳酸钾溶液至过量 B、②图加热等质量的两份氯酸钾,一份加入二氧化锰,一份不加入二氧化锰 C、③图一定量的硫粉与过量的氧气在密闭容器内点燃并充分反应 D、④图向一定量的氯化亚铁和氯化铜的混合溶液中,逐渐加入镁粉至过量
二、填空题
-
16. 用正确的化学符号填空:(1)、3个氦原子;(2)、五氧化二磷;
-
17. 生活中处处蕴含着化学知识。请用所学知识回答下列问题:(1)、日常生活中常用的方法降低水的硬度;(2)、端午节临近,我们包粽子准备了如下食材:糯米、瘦肉、花生、红枣,其中瘦肉富含的营养素主要是。(3)、食品安全是一个永恒的话题。下列说法不科学的是_____(填字母)。A、霉变的花生、大米蒸煮后仍不可食用 B、不可用亚硝酸钠代替食盐腌制食物 C、使用了食品添加剂的食品对人体都有害处(4)、固体叠氮化钠(NaN3)被广泛应用于汽车安全气囊。撞击后30毫秒内,叠氮化钠迅速分解生成两种单质,写出该反应的化学方程式:。
-
18. 能源、材料和安全是人们关注的热点话题。请回答:(1)、太阳能电池路灯被越来越广泛地应用。如图所标示的路灯各主要部件中属于有机合成材料的是(填序号),电池板中用铜丝导线主要是利用了铜的。
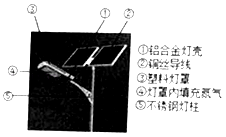
(2)、无人驾驶汽车处理系统的核心材料是高纯度硅。工业上制硅的反应之一是:2X+SiCl4=Si+4HCl,该反应中X的化学式为。(3)、恰当的安全措施能减少生命财产损失。下列措施正确的是_____ (填字母)。A、燃气泄漏,立即关闭阀门并开窗通风 B、电器着火,立即用水浇灭 C、点燃甲烷前,先检验气体纯度 D、住房着火,立即打开所有门窗 -
19. 诺贝尔生理学和医学奖的一次重大失误是1948年授予了瑞士化学家米勒,他发明的剧毒有机氯杀虫剂DDT (化学式Cl14H9C5)带来了许多环境问题,后来被禁用。试计算:(1)、一个DDT分子是由个原子构成;(2)、DDT中碳元素和氢元素的质量比为 (填最简整数比)。
-
20. 现有下列物质:①石墨②熟石灰③稀有气体④氯化钠⑤纯碱,请选择合适物质的序号填空:(1)、常用于制作电极的是;(2)、常用于消除公路积雪的是;(3)、常用于改良酸性土壤的是;
三、推断题
-
21. A~H是初中化学常见的物质,A、B、C、D、E是五种不同类别的物质。A和G的组成元素相同,D为蓝色沉淀。它们之间存在如图所示的相互关系,“→”表示在一定条件下能发生转化,“﹣”表示在一定条件下能相互反应(部分反应物、生成物和反应条件已省略)。物质可分为单质、氧化物、酸、碱、盐五类。请回答:
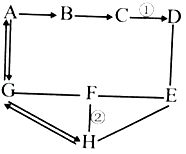 (1)、写出G的化学式:;(2)、写出反应①的化学方程式:;(3)、反应②的基本类型是反应。
(1)、写出G的化学式:;(2)、写出反应①的化学方程式:;(3)、反应②的基本类型是反应。
四、实验题
-
22. 实验课上,同学们利用下列装置进行气体制备的学习。请回答下列问题:
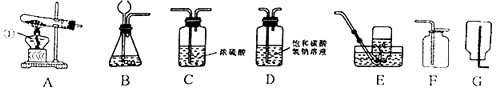 (1)、编号①的仪器名称是。(2)、用加热法制取氧气,所选择的发生装置是 (填字母,下同),收集装置是 , 反应的化学方程式为。(3)、若要制取瓶纯净、干燥的二氧化碳气体 (常混有少量氯化氢气体和水蒸气,装置连接的正确顺序是:产生气体→→→F.检验二氧化碳气体的方法是。
(1)、编号①的仪器名称是。(2)、用加热法制取氧气,所选择的发生装置是 (填字母,下同),收集装置是 , 反应的化学方程式为。(3)、若要制取瓶纯净、干燥的二氧化碳气体 (常混有少量氯化氢气体和水蒸气,装置连接的正确顺序是:产生气体→→→F.检验二氧化碳气体的方法是。
五、科学探究题
-
23. 化学兴趣小组在实验室发现一瓶氢氧化钠溶液,瓶口有少量白色固体且玻璃瓶塞打不开,这一情况激起了他们浓厚的兴趣,于是展开了如下探究:
【提出问题】瓶口白色固体的成分是什么?
【查找资料】⑴玻璃中含有二氧化硅(SiO2),试剂瓶身经抛光处理,不易反应,而瓶口和玻璃塞上的磨砂将二氧化硅裸露出来;
⑵二氧化硅能与氢氧化钠溶液反应,SiO2+2NaOH=Na2SiO3+H2O;
⑶硅酸钠(Na2SiO3)是一种白色固体,有很强的粘合性,可溶于水,溶液呈碱性;硅酸钠溶液能与强酸反应,如:Na2SiO3+2HCl=2NaCl+H2SiO3↓(白色);
硅酸钠溶液能与氯化钙溶液反应:Na2SiO3+CaCl2=2NaCl+CaSiO3↓(白色)。
(作出猜想)白色固体的成分是:
Ⅰ.硅酸钠;
Ⅱ.硅酸钠和碳酸钠;
Ⅲ.硅酸钠、碳酸钠和氢氧化钠
(1)、【实验探究】取一定量白色固体溶于适量水中形成样品溶液,分组进行如下实验并相互评价:实验操作
实验现象
结论与评价
第1组
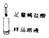
有气泡冒出且产生白色沉淀
同学们认为猜想①不成立;写出生成气体的反应化学方程式:②
第2组
第一步
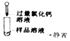
产生白色沉淀
第1组同学认为:此步骤还不能准确判断出原固体的成分。
第二部

③
大家一致认为:猜想II成立。
(2)、【反思交流】①有同学认为,第2组实验中不能用氢氧化钙溶液代替氯化钙溶液,理由是:④;
②氢氧化钠溶液必项密封保存,且试剂瓶只能用橡胶塞。
六、计算题
-
24. 小兰进行水的电解实验时,在水中加入少许硫酸钠以增强导电性。她将2.7g硫酸钠固体加入52.7g水中充分溶解,倒入电解器中通电,当正极产生4.8g氧气时结束实验。忽略气体在水中的溶解,请计算(写出计算过程):(1)、负极产生氢气的质量;(2)、实验结束时所得溶液的溶质质量分数。
