2016-2017学年甘肃省白银市会宁四中高一上学期期中化学试卷
试卷更新日期:2017-01-20 类型:期中考试
一、选择题
-
1. 在实验室中,对下列事故或药品的处理正确的是( )A、温度计不慎打破,散落的水银应用硫粉处理后收集 B、酒精灯使用完后,应及时吹灭并盖上灯帽 C、少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗 D、含硫酸的废液倒入水槽,用水冲入下水道2. 不是Fe(OH)3胶体和MgCl2溶液共同具备的性质是( )A、都比较稳定,密封放置不产生沉淀 B、都有丁达尔现象 C、加入少量NaOH溶液都可产生沉淀 D、分散质微粒均可透过滤纸3. 下列各物质,按单质、化合物、混合物的顺序排列的是( )A、干冰、铁、胆矾 B、液态氧、氧化钙、石灰水 C、氮气、氯化氢、烧碱 D、水、碘酒、熟石灰4. 当光束通过下列分散系:①尘埃的空气 ②稀硫酸 ③蒸馏水 ④墨水,能观察到有丁达尔现象的是( )A、①② B、②③ C、①④ D、②④5. 下列化学方程式中,不能用H++OH﹣=H2O表示的是( )A、2NaOH+H2SO4=Na2SO4+2H2O B、Ba(OH)2+2HCl=BaCl2+2H2O C、Cu(OH)2+2HNO3=Cu(NO3)2+2H2O D、KOH+HCl=KCl+H2O6. 绿色植物是空气天然的“净化器”,研究发现,1公顷柳杉每月可以吸收160kg SO2 , 则1公顷柳杉每月吸收的SO2的物质的量为( )A、164kg B、2.5mol C、2500mol D、2500g/mol7. 在酸性溶液中,可大量共存的离子是( )A、K+ Na+ OH﹣ SO42﹣ B、Mg2+ SO42﹣ NH4+ Cl﹣ C、K+ Na+ HCO3﹣ Cl﹣ D、K+ Na+ NO3﹣ CO32﹣8. 为了除去粗盐中的Ca2+、Mg2+、SO 及泥沙,可将粗盐溶于水,然后进行下列5项操作:①过滤;②加过量NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液.正确的操作顺序可以是( )A、⑤②④③① B、④①②⑤③ C、②⑤④①③ D、①④②⑤③9. 下列条件中,两种气体所含原子数一定相等的是( )A、同质量、不同密度的N2和CO B、同温度、同体积的H2和N2 C、同体积、同密度的C2H6和NO D、同压强、同体积的N2O和CO210. 设NA为阿伏加德罗常数,下列说法正确的是( )
①标准状况下,11.2L以任意比例混合的氮气和氧气所含的原子数为NA
②同温同压下,体积相同的氢气和氩气所含的分子数相等
③1L 2mol/L的氯化镁溶液中含氯离子为4NA
④标准状况下22.4LH2O中分子数为NA
⑤32g O2和O3混合气体中含有原子数为2NA .
A、①②③④ B、③④ C、①③④ D、①②③⑤11. 用固体NaOH配制一定物质的量浓度的NaOH溶液,下列操作正确的是( )A、称量时,将固体NaOH直接放在天平左盘上 B、将称量好的固体NaOH放入容量瓶中,加蒸馏水溶解 C、定容时如果加水超过了刻度线,用胶头滴管直接吸出多余部分 D、将烧杯中溶解固体NaOH所得溶液,冷却到室温后转移至容量瓶中12. 下列离子方程式书写正确的是( )A、铜片插入硝酸银溶液中 Cu+Ag+=Cu2++Ag B、碳酸钙与盐酸反应:CO32﹣+2H+═CO2↑+H2O C、硫酸铜溶液与氢氧化钡溶液反应:Ba2++ ═BaSO4↓ D、铁与稀硫酸反应:Fe+2H+═Fe2++H2↑13. 同温同压下,甲容器中HCl气体和乙容器中的NH3气体所含的原子个数相等,则甲、乙两容器的体积之比为( )A、2:1 B、1:2 C、1:1 D、1:414. 下列叙述正确的是( )A、液态HCl不导电,所以HCl是非电解质 B、NH3的水溶液能够导电,所以NH3是电解质 C、液态Cl2不导电,所以Cl2是非电解质 D、BaSO4溶于水的部分能够电离,所以BaSO4是电解质15. “纳米材料”(1nm=10﹣9 m)是指研究开发直径为几纳米至几十纳米的材料.如将“纳米材料”分散到某液体中,对于所得分散系的叙述不正确的是( )A、光速通过此分散系时会形成一条光亮的“通路” B、此分散系中“纳米材料”的粒子在做不停的、无序的运动 C、在外加电场作用下,“纳米材料”的粒子可能向电极做定向运动 D、用滤纸过滤的方法可以从此分散系中分离得到该“纳米材料”16. 200mLFe2(SO4)3溶液中含Fe3+56g,溶液中SO42﹣的物质的量浓度是( )A、5mol/L B、7.5 mol/L C、10 mol/L D、2.5 mol/L17. 下列常用实验仪器中,能直接加热的是( )A、分液漏斗 B、普通漏斗 C、蒸馏烧瓶 D、蒸发皿18. 对下列物质进行的分类正确的是( )A、纯碱、烧碱均属于碱 B、CuSO4•5H2O属于纯净物 C、凡能电离出H+的化合物均属于酸 D、盐类物质一定含有金属阳离子19. 下列溶液与20mL 1mol•L﹣1 NaNO3溶液中NO3﹣物质的量浓度相等的是( )A、10 mL 1 mol•L﹣1 Mg(NO3)2溶液 B、5 mL 0.8 mol•L﹣1 Al(NO3)3溶液 C、10 mL 2 mol•L﹣1AgNO3溶液 D、10 mL 0.5 mol•L﹣1 Cu(NO3)2溶液20. 如果你家里的食用花生油不小心混入了大量的水,利用你所学的知识,最简便的分离方法是( )A、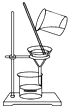 B、
B、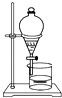 C、
C、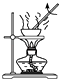 D、
D、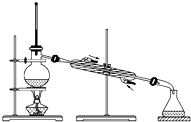
二、填空题
-
21. 用于提纯或分离物质的方法有:A,萃取分液 B,加热分解 C,蒸发结晶 D,分液 E,蒸馏 F,过滤 G,渗析等,请将提纯或分离的序号填在后面横线上.(1)、分离饱和食盐水与泥沙的混合物(2)、精制Fe(OH)3胶体(含有NaCl溶液)(3)、分离相溶的CCl4(沸点为76.75℃)和甲苯(110.6℃)的混合物(4)、从碘水里提取碘 .22. 对下列物质:①H2SO4 , ②CaO,③NaOH,④熔融BaSO4 , ⑤盐酸、⑥SO2、⑦氨水、⑧C2H5OH,⑨Cu、⑩氯化钠溶液按要求分类(填写序号)(1)、电解质:;(2)、非电解质:;(3)、能导电的:;(4)、纯净物且水溶液能导电: .23. 设NA为阿伏加德罗常数(1)、4.9g硫酸中含有 mol H原子,个O原子和 个S原子,与克H2O中所含O原子数相等,溶于水配成500mL溶液其物质的量浓度为 .(2)、同温同压下,体积相等的CO和CO2的分子数之比为 , 物质的量之比为 , 原子数之比为 , 质量之比为 ,(3)、某金属氯化物MCl227g,含有0.40molCl﹣ , 则该氯化物的物质的量为 , 摩尔质量为 , 金属M的相对原子质量为 .
三、实验题
-
24. 实验需要0.1mol/LNaOH溶液450mL,根据溶液配制中情况回答下列问题:(1)、实验中必须用到的玻璃仪器有: .(2)、根据计算得知,所需NaOH的质量为 g.(3)、配制时,其正确的操作顺序是(字母表示,每个字母只能用一次);
A.用50mL水洗涤烧杯2﹣3次,洗涤液均注入容量瓶,振荡
B.用托盘天平准确称量取所需的NaOH的质量,倒入烧杯中加入适量水,用玻璃棒慢慢搅动.
C.将已冷却的NaOH溶液沿玻璃棒注入500mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.加水至离刻度线1~2cm处改用胶头滴管加水,使溶液凹面恰好与刻度相切
(4)、下列操作对所配浓度有何影响(填写字母)偏大的有;
偏小的有;
无影响的有 .
A.称量用了生锈的砝码;
B.将NaOH放在纸张上称量;
C.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中;
D.往容量瓶转移时,有少量液体溅出
E.未洗涤溶解NaOH的烧杯
F.定容时仰视刻度线
G.容量瓶未干燥即用来配制溶液
H.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线.
25. 如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题. (1)、图中的两处明显的错误是(2)、A仪器的名称是 , B仪器的名称是(3)、实验时A中除加入自来水外,还需加入少量 , 其作用是 .
(1)、图中的两处明显的错误是(2)、A仪器的名称是 , B仪器的名称是(3)、实验时A中除加入自来水外,还需加入少量 , 其作用是 .