2018年天津市初中毕业生学业考试化学试题
试卷更新日期:2018-06-25 类型:中考真卷
一、单选题
-
1. 从环境保护的角度考虑,下列燃料中最理想的是( )A、天然气 B、氢气 C、酒精 D、乙醇汽油2. 下列变化属于化学变化的是( )A、纸张燃烧 B、盐酸挥发 C、冰雪融化 D、瓷碗破碎3. 人体内含量最高的金属元素是( )A、铁 B、锌 C、钾 D、钙4. 右图为空气成分示意图(按体积分数计算),其中“a”代表的是( )
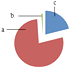 A、氧气 B、氮气 C、二氧化碳 D、稀有气体5. 在汽车加油站见到的油罐车上,所贴的危险化学品图标是( )A、
A、氧气 B、氮气 C、二氧化碳 D、稀有气体5. 在汽车加油站见到的油罐车上,所贴的危险化学品图标是( )A、 B、
B、 C、
C、 D、
D、 6. 有一位同学暑假去西藏发生了严重的高原反应,医生让他吸氧后症状缓解。吸氧可以帮助人缓解高原反应的原因是( )A、氧气是无色无味的气体 B、氧气可以支持燃烧 C、吸氧为人体呼吸提供了适量的氧气 D、氧气可以燃烧7. 下列说法正确的是( )A、木炭燃烧后生成黑色固体 B、铁丝伸入盛有氧气的集气瓶中剧烈燃烧 C、红磷在空气中燃烧产生白色烟雾 D、硫在氧气中燃烧发出蓝紫色火焰8. 人体中一些体液或排泄物的pH范围如下,其中酸性最强的是( )A、胃液0.9~1.5 B、唾液6.6~7.1 C、尿液4.7~8.4 D、胰液7.5~8.09. 下列有关农药的叙述中错误的是( )A、施用农药是最重要的作物保护手段 B、农药施用后,会通过农作物、农产品等发生转移 C、农药本身有毒,应该禁止使用农药 D、为了减少污染,应根据作物、虫害和农药的特点按规定合理施用农药10. 在反应A+3B=2C+2D中,已知A和B的相对分子质量之比为7∶8,当2.8gA与一定量B恰好完余反应后,生成3.6gD,则生成C的质量为( )A、9.6g B、8.8g C、6.8g D、4.4g11. 下列对事实的解释错误的是( )
6. 有一位同学暑假去西藏发生了严重的高原反应,医生让他吸氧后症状缓解。吸氧可以帮助人缓解高原反应的原因是( )A、氧气是无色无味的气体 B、氧气可以支持燃烧 C、吸氧为人体呼吸提供了适量的氧气 D、氧气可以燃烧7. 下列说法正确的是( )A、木炭燃烧后生成黑色固体 B、铁丝伸入盛有氧气的集气瓶中剧烈燃烧 C、红磷在空气中燃烧产生白色烟雾 D、硫在氧气中燃烧发出蓝紫色火焰8. 人体中一些体液或排泄物的pH范围如下,其中酸性最强的是( )A、胃液0.9~1.5 B、唾液6.6~7.1 C、尿液4.7~8.4 D、胰液7.5~8.09. 下列有关农药的叙述中错误的是( )A、施用农药是最重要的作物保护手段 B、农药施用后,会通过农作物、农产品等发生转移 C、农药本身有毒,应该禁止使用农药 D、为了减少污染,应根据作物、虫害和农药的特点按规定合理施用农药10. 在反应A+3B=2C+2D中,已知A和B的相对分子质量之比为7∶8,当2.8gA与一定量B恰好完余反应后,生成3.6gD,则生成C的质量为( )A、9.6g B、8.8g C、6.8g D、4.4g11. 下列对事实的解释错误的是( )选项
事实
解释
A
用洗洁精洗去餐盘上的油渍
洗洁精能溶解油渍形成溶液
B
盐酸、稀硫酸的化学性质相似
盐酸、稀硫酸中都含有氢离子
C
金刚石和石墨的物理性质存在着明显差异
它们的碳原子排列方式不同
D
6000L氧气在加压情况下可装入容积为40L的钢瓶中
加压时氧气分子变小
A、A B、B C、C D、D12. 芯片是电脑、智能家电的核心部件,它是以高纯度的单质硅(Si)为材料制成的。硅及其氧化物能发生如下反应:①Si+O2=SiO2 ②SiO2+Na2CO3 =Na2SiO3+CO2↑
③SiO2+2C=Si+2CO↑ ④Si+2NaOH+H2O=Na2SiO3+2H2↑
下列说法错误的是( )
A、反应③属于置换反应 B、上述反应中共生成三种可燃性气体 C、Na2SiO3 中 Si 为+4 价 D、Si 和 SiO2 在一定条件下可以相互转化13. 下列有关实验方案设计正确的是( )选项
实验目的
实验方案
A
检验NaOH溶液中是否含有Na2CO3
加入过量的稀盐酸,观察现象
B
鉴别纯棉线和羊毛线
观察颜色
C
除去KNO3溶液中的少量Ba(NO3)2
加入适量的Na2SO4溶液,过滤
D
除去CO2中含有的少量CO
点燃
A、A B、B C、C D、D14. 下列各组物质反应,所得溶液能使酚酞溶液变红的是( )A、一定量的稀盐酸与适量的氢氧化钠溶液恰好完会反应 B、相同质量、相同溶质质量分数的氢氧化钾溶液与盐酸相混合 C、将硫酸钾溶液滴入氢氧化钡溶液中恰好完全反应 D、将二氧化碳气体通入氢氧化钠溶液中得到碳酸钠溶液15. 某固体粉末可能含有碳酸钙、氧化铜、氧化铁、木炭粉中的几种,取mg该固体粉末按下列流程进行实验(本流程涉及到的反应均为初中化学常见的反应,且各步均恰好完全反应)。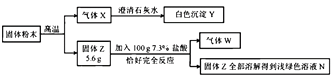
下列说法中正确的是( )
A、溶液N中只含一种溶质 B、原固体粉末中可能含有碳酸钙 C、白色沉淀Y一定是碳酸钙,气体W一定是氢气 D、原固体粉末中一定没有氧化铜,一定含有碳酸钙二、填空题
-
16. 化学就在我们身边,一些物质在生产生活中有重要的用途。现有①二氧化碳②活性炭③氮气④熟石灰⑤硝酸钾⑥不锈钢,选择适当的物质填空(填序号)。(1)、可用于冰箱除味剂的是;(2)、绿色植物进行光合作用吸收的是;(3)、与硫酸铜溶液混合可配成波尔多液的是;(4)、可充入食品包装袋中以防腐的是;(5)、可用于制造炊具的是;(6)、属于复合肥科的是。17. 生活离不开水,我们可以从组成、结构、性质等角度认识水。(1)、组成:下图所示电解水的实验中,试管 a、b 中产生气体的体积比约为 , 该 实验证明水是由组成的。
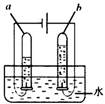 (2)、结构:每个水分子是由构成的。(3)、性质:水能与许多物质发生化学反应,写出水与氧化钙反应的化学方程式。18. 化学是在分子、原子层次上研究物质的科学。(1)、构成物质的粒子有分子、原子和。(2)、下图为三种元素的原子结构示意图。
(2)、结构:每个水分子是由构成的。(3)、性质:水能与许多物质发生化学反应,写出水与氧化钙反应的化学方程式。18. 化学是在分子、原子层次上研究物质的科学。(1)、构成物质的粒子有分子、原子和。(2)、下图为三种元素的原子结构示意图。
①氧原子在化学反应中容易电子(填“得到”或“失去”)。
②二氧化硫和二氧化碳都能与氢氧化钠溶液反应生成盐和水。将二氧化硫气体通入氢氧化钠溶液中生成亚硫酸钠(Na2SO3)和水,写出该反应的化学方程式。
③硒元素能增强人体免疫力,延缓衰老,山药等食物中富含硒元素。硒(Se)在氧气中燃烧生成二氧化硒。回答下列问题:
A.硒原子的核电荷数为。
B.硒元素与氧、硫元素的化学性质相似,原因是它们的原子相同。
C.写出硒在氧气中燃烧反应的化学方程式。
三、简答题
-
19. 写出下列反应的化学方程式。(1)、碳在氧气中充分燃烧生成二氧化碳;(2)、氢氧化钠溶液与稀盐酸混合;(3)、镁与稀硫酸反应。20.(1)、下图是利用海水提取粗盐的过程:
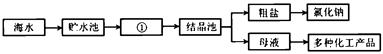
上图中①是池 (填“蒸发”或“冷却”)。
(2)、粗盐中含有少量 CaCl2、MgCl2、Na2SO4 和泥沙,某同学将该粗盐样品进行提纯。①将样品加适量水溶解,然后进行 , 除去泥沙等难溶性杂质,得到澄清溶液;
②向所得的澄清溶液中依次加入稍过量的 BaCl2 溶液、NaOH 溶液和溶液, 除去生成的沉淀后,再滴加稍过量的稀盐酸,得到较纯挣的 NaCl 溶液;
③蒸发溶液,得到较多氯化钠固体时停止加热,他注意到不能立即把直接放 在实验台上,以免烫坏实验台。
(3)、另一同学用所得的氯化钠和蒸馏水配制溶质质量分数为 6%的氯化钠溶液。配制步骤:①称量和量取②溶解③计算④装入试剂瓶贴好标签。配制上述溶液的正确顺序是 (填序号)。21. 溶液与人们的生产生活密切相关。(1)、将少量下列物质分别放入水中,充分搅拌,可以得到无色溶液的是_____(填字母)。A、高锰酸钾 B、汽油 C、面粉 D、白糖(2)、在盛有水的烧杯中加入以下某种物质,形成溶液过程中,温度没有明显变化的 是_____ (填字母)。A、烧碱 B、硝酸铵 C、氯化钠 D、浓硫酸(3)、下图 1 为甲、乙两种固体物质的溶解度曲线。
①溶解度随温度升高而增大的物质是(填 “甲”或“乙”)。
②某同学按图 2 所示进行实验,得到相应温度下的 A、B、C 溶液,在 A、B、C 三种 溶液中属于饱和溶液的是(填字母)。向溶液 C 中再加入 25g 甲,充分搅拌, 恢复到 t2℃时,所得溶液中溶质的质量分数为(结果精确到 0.1%)。
③将 t2℃时的甲、乙两种物质的饱和溶液降温至 t1℃,所得溶液中溶质的质量分数 甲乙(填“<”、“=”或“>”)。
四、实验题
-
22. 根据下列装置图回答问题:
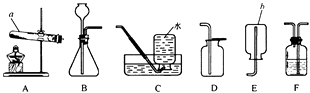 (1)、写出仪器 a 和 b 的名称:a , b。(2)、实验室用大理石和稀盐酸制取并收集二氧化碳,应选用的装置为(填字母), 若用 F 装置干燥二氧化碳气体,F 中应加入的试剂是。(3)、实验室用高锰酸钾制取气体,该反应的化学方程式为。(4)、实验室取用药品要注意节约,如果没有说明用量,一般应该取用最少量,固体药品 只需盖满试管底部,液体药品取用mL。23. 金属材料广泛应用于生产生活中。(1)、常温下大多数金属都是固体,但体温计中的金属却是液体,该金属是。(2)、铝在空气中与氧气反应,其表面生成一层致密的氧化物薄膜,从而阻止铝进一步氧化。这种氧化物的化学式为。(3)、向含有氯化铜、氯化锌、稀盐酸的混合溶液中加入过量铁粉,充分反应后过滤,滤液中含有的溶质是(写化学式)。(4)、铁矿石有多种,如赤铁矿(主要成分Fe2O3)和磁铁矿(主要成分Fe3O4)等。
(1)、写出仪器 a 和 b 的名称:a , b。(2)、实验室用大理石和稀盐酸制取并收集二氧化碳,应选用的装置为(填字母), 若用 F 装置干燥二氧化碳气体,F 中应加入的试剂是。(3)、实验室用高锰酸钾制取气体,该反应的化学方程式为。(4)、实验室取用药品要注意节约,如果没有说明用量,一般应该取用最少量,固体药品 只需盖满试管底部,液体药品取用mL。23. 金属材料广泛应用于生产生活中。(1)、常温下大多数金属都是固体,但体温计中的金属却是液体,该金属是。(2)、铝在空气中与氧气反应,其表面生成一层致密的氧化物薄膜,从而阻止铝进一步氧化。这种氧化物的化学式为。(3)、向含有氯化铜、氯化锌、稀盐酸的混合溶液中加入过量铁粉,充分反应后过滤,滤液中含有的溶质是(写化学式)。(4)、铁矿石有多种,如赤铁矿(主要成分Fe2O3)和磁铁矿(主要成分Fe3O4)等。①写出赤铁矿石中的主要成分与一氧化碳反应的化学方程式。
②冶炼2900t含四氧化三铁80%的磁铁矿石,理论上能得到含杂质2%的生铁的质量是 t(结果精确到0.1)。
(5)、含有锌粉6.5g、铁粉5.6g、铜粉3.2g、铝粉1.8g的混合物与一定质量的稀硫酸充分反应,反应停止后,有6g固体剩余。则生成氢气的质量为g。
24. 酸、碱、盐在生产生活中具有广泛的用途。(1)、化学实验室有失去标签的稀硫酸、氢氧化钠、氢氧化钙、碳酸钠、氯化钡五瓶无色 溶液,现将其任意编号:A、B、C、D、E,然后两两组合进行实验,其部分现象如下表(微溶物视为可辩物):实验
A+B
A+C
A+D
B+C
现象
产生气体
产生沉淀
产生沉淀
产生沉淀
①写出溶液B、C中溶质的化学式: B , C。
②写出溶液 A 与 D 反应的化学方程式。
(2)、我国制碱工业先驱侯德榜发明了“侯氏制碱法”,其主要化学原理:NaCl+H2O+NH3+CO2=NaHCO3↓+X; 2NaHCO3=Na2CO3+H2O+CO2↑等;
回答下列问题:
①X 的化学式为。
②将碳酸钠和碳酸氢钠的混合物10g 充分加热至质量不再改变,冷却,称量剩余固体质量为 6.9g,则原混合物中碳酸钠和碳酸氢钠的质量比为(写最简比)。
五、计算题