浙教版科学九上 1.4 常见的碱 同步练习
试卷更新日期:2018-06-22 类型:同步测试
一、单选题
-
1. 下列不属于NaOH的俗称的是( )A、苛性钠 B、烧碱 C、纯碱 D、火碱2. 下列潮湿的气体不能用固体氢氧化钠干燥的是( )A、H2 B、CO2 C、CO D、O23. 下列物质在敞口容器中久置,因发生化学变化溶液质量减小的是( )A、浓硫酸 B、浓盐酸 C、氢氧化钠溶液 D、石灰水4. 氢氧化钠是一种常见的碱,下列有关氢氧化钠的说法正确的是( )A、固态氢氧化钠具有吸水性,可以用来干燥 O2、H2、CO2 等气体 B、氢氧化钠能与酸反应,可用于治疗胃酸过多 C、氢氧化钠与氢氧化钾在水中都能解离出 OH-,化学性质相似 D、向露置于空气中的氢氧化钠溶液中滴加酚酞,溶液变红,说明氢氧化钠溶液没有变质5. 研究氢氧化钠性质实验中的部分实验及现象记录如下,其中现象不合理的是( )
序号
实 验
现 象
A
将氢氧化钠固体放在表面皿上,放置一会儿
固体受潮,逐渐溶解
B
向盛有氢氧化钠溶液的试管中滴入无色酚酞试液
溶液变红
C
向盛有氢氧化钠溶液的试管中滴加稀盐酸
有氯化钠生成
D
向盛有氢氧化钠溶液的试管中滴加硫酸铜溶液
产生蓝色沉淀
A、A B、B C、C D、D6. 将固体混合物中的NaCl、CuCl2、Mg(OH)2进行逐一分离,可选用的试剂是( )A、水 氢氧化钠溶液 B、水 氢氧化钾溶液 稀盐酸 C、水 氢氧化钾溶液 D、水 氢氧化钠溶液 稀盐酸7. 下列各组物质按酸、碱、单质、氧化物顺序排列的是( )A、H2SO4 , Na2O,C,CO B、Mg(OH)2 , CuSO4 , C,CO2 C、KOH,HNO3 , O2 , SO3 D、HCl,NaOH,O2 , P2O58. 下列实验对应的图像正确的是 ( )A
B
C
D
向稀硫酸中加入过量的锌,溶液中溶质质量
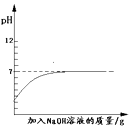
向pH=2的盐酸中滴加过量的氢氧化钠溶液
向盐酸和氯化铁的混合溶液中加入过量的氢氧化钠溶液
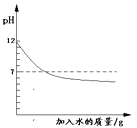
向pH=12的氢氧化钠溶液中加水稀释


 A、A B、B C、C D、D9. 下列关于氢氧化钠和氢氧化钙的描述中错误的是( )A、它们的水溶液都能使石蕊溶液变红 B、氢氧化钙的溶解度随温度升高而减小,氢氧化钠固体溶于水会放出大量的热量 C、它们的溶液敞口放在空气中都会变质 D、氢氧化钠可用来生产肥皂,氢氧化钙可用来杀菌消毒及改良酸性土壤10. 下列关于碱的叙述中,不正确的是( )A、含有氢氧根离子的化合物 B、碱溶液能使紫色石蕊试液变蓝 C、碱能跟酸反应生成盐和水 D、电离出阴离子全部都是氢氧根离子的化合物是碱11. 用稀的碱性溶液或清水浸泡,可使残留在蔬菜上的农药降低毒性。如用碱性溶液浸泡蔬菜,可在水中加入适量的 ( )A、白酒 B、纯碱 C、白糖 D、食醋12. 下列说法正确的是( )A、pH﹥7的溶液一定是碱溶液 B、碱溶液中阴、阳离子的数目相等 C、碱在电离时生成的阴离子全部是OH- D、电离时有阳离子和OH-生成的化合物叫做碱
A、A B、B C、C D、D9. 下列关于氢氧化钠和氢氧化钙的描述中错误的是( )A、它们的水溶液都能使石蕊溶液变红 B、氢氧化钙的溶解度随温度升高而减小,氢氧化钠固体溶于水会放出大量的热量 C、它们的溶液敞口放在空气中都会变质 D、氢氧化钠可用来生产肥皂,氢氧化钙可用来杀菌消毒及改良酸性土壤10. 下列关于碱的叙述中,不正确的是( )A、含有氢氧根离子的化合物 B、碱溶液能使紫色石蕊试液变蓝 C、碱能跟酸反应生成盐和水 D、电离出阴离子全部都是氢氧根离子的化合物是碱11. 用稀的碱性溶液或清水浸泡,可使残留在蔬菜上的农药降低毒性。如用碱性溶液浸泡蔬菜,可在水中加入适量的 ( )A、白酒 B、纯碱 C、白糖 D、食醋12. 下列说法正确的是( )A、pH﹥7的溶液一定是碱溶液 B、碱溶液中阴、阳离子的数目相等 C、碱在电离时生成的阴离子全部是OH- D、电离时有阳离子和OH-生成的化合物叫做碱二、填空题
-
13. 氢氧化钙俗称熟石灰,在生产和生活中有广泛的用途.(1)、熟石灰可由生石灰溶于水制得,反应的化学方程式是: . 测量其溶液的pH时,应该用 , 再用标准比色卡比较试纸显示的颜色,读取该溶液的pH.(2)、用石灰浆粉刷墙壁,干燥后墙面变硬,反应的化学方程式是: .(3)、用熟石灰粉与草木灰(主要成分:K2CO3)按一定比例混合可制得高效环保农药“黑白粉”.在有露水的早晨,把“黑白粉”撒在植物茎叶上,可杀灭某些害虫.
①“黑白粉”比熟石灰更高效,是由于生成了碱性更强的KOH,反应的化学方程式是 .
②“黑白粉”还可提供植物必需的营养素是(填元素符号).
14. 液氨(NH3)是冷饮厂常用的冷冻剂,请回答下列问题:(1)、液氨泄漏时可用水处理,说明该物质具有的物理性质;(2)、向氨水中滴加酚酞溶液,溶液变成色,说明氨水显碱性.15. 氢氧化钠溶液逐滴滴入硫酸铜、硫酸混合溶液中,生成沉淀随滴入氢氧化钠溶液的变化如图. (1)、OA 段溶液中溶质是(2)、AB 段溶液中溶质是(3)、BC 段溶液中溶质是 .16. 分析下列反应,回答有关问题.
(1)、OA 段溶液中溶质是(2)、AB 段溶液中溶质是(3)、BC 段溶液中溶质是 .16. 分析下列反应,回答有关问题.①2KOH+CO2═K2CO3+H2O ②Ca(OH)2+CO2═CaCO3↓+H2O
(1)、由上述反应可知,碱溶液与二氧化碳反应都生成和水.(2)、根据上述规律,写出Ba(OH)2与CO2反应的化学方程式 .(3)、依据所学知识推测,用二氧化碳鉴别氢氧化钠和氢氧化钙两种溶液时,无明显现象的是溶液.17. 结合NaOH、Ca(OH)2的相关知识,回答下列问题(1)、可用来改变良酸性土壤的碱是;(2)、从微观角度看,它们的溶液具有相似化学性质的原因是;(3)、除去NaOH溶液中混有的少量Ca(OH)2 , 可选用的试剂是 .18. 如图所示,向充满干燥的CO2气体的烧瓶中,第一次滴加氢氧化钠溶液,小气球发生的变化为 , 原因是 , 反应的化学方程式为;第二次再向烧瓶内溶液中滴加盐酸,小气球发生的变化为 , 其原因是(用化学方程式表示) . 19. 把NaOH溶液露置在空气中,过一段时间后,加入足量稀盐酸,一段时间有气泡产生.说明NaOH溶液发生变质.为什么一段时间后才看到气泡?原因 .
19. 把NaOH溶液露置在空气中,过一段时间后,加入足量稀盐酸,一段时间有气泡产生.说明NaOH溶液发生变质.为什么一段时间后才看到气泡?原因 . 20. 氢氧化钙和氢氧化钠都是常用的碱.(1)、请写出氢氧化钙与下列物质反应的化学方程式:
20. 氢氧化钙和氢氧化钠都是常用的碱.(1)、请写出氢氧化钙与下列物质反应的化学方程式:①与盐酸反应:
②与硫酸铜溶液反应:
上述反应中,属于所有的碱都有的共同化学性质是(填编号).
(2)、氢氧化钙的下列用途中,不能用氢氧化钠来代替的是(填编号).①中和废水中的过量硫酸②改良酸性土壤③检验二氧化碳.
三、解答题
-
21. 向一含有盐酸的氯化铁溶液中边振荡边逐滴滴入氢氧化钠溶液,直至过量,某同学画了如图,要表明反应过程中,溶液总质量与滴入氢氧化钠溶液质量的关系.请看图分析:

(1)、b点对应的溶液中,溶质的化学式为 .(2)、图中部分线段有误,请在答题卡的图中,重新画出溶液总质量与滴入氢氧化钠溶液质量的变化关系曲线(要求标出abc折线点).
22. 精盐(NaCl)和纯碱(Na2CO3)是两种常见之物.(1)、用化学方法区别这两种固体,可以选择下列哪一种物质?答:A、白酒 B、米醋 C、纯净水 D、酱油(2)、王军同学不慎在精盐中混入了少量纯碱,他想重新得到精盐,设计了以下两个实验方案:方案一:固体混合物 溶液 固体
方案二:固体混合物 溶液 固体
你认为合理的实验方案是 .
说明另一方案不合理的理由: .
(3)、假设(2)方案一的固体混合物有53克,加入160克的稀盐酸却好反应后,生成4.4克二氧化碳气体,则该固体混合物中氯化钠的质量分数是多少?反应后所得溶液的溶质质量分数(要求列式计算).23. 甲、乙、丙三位同学对氯化镁样品(仅含氯化钠杂质)进行如下检测:各取5.0 g样品溶于一定量的水中得到25. 0g溶液,再分别加入不同质量,溶质质量分数为10%的氢氧化钠溶液,反应得到沉淀的实验数据如下表:甲
乙
丙
加入氢氧化钠溶液质量 (g)
35.0
40.0
45.0
反应得到沉淀的质量 (g)
2.5
2.9
2.9
试回答下列问题:
(1)、上述实验中,同学所用的氢氧化钠溶液一定过量。(2)、求样品中氯化镁的含量(写出计算过程,结果精确到0.1%,下同)。(3)、计算乙同学实验后所得溶液中的氯化钠的质量分数。24. 向含CuCl2和HCl的100g混合溶液中,逐滴滴加溶质质量分数为10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图所示。请据图回答
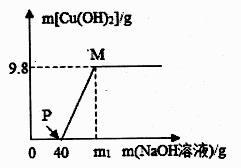 (1)、在滴加NaOH溶液过程中,原溶液中离子个数不变。(填离子符号)(2)、P点溶液中的溶质是(填化学式)。(3)、m1的值为(4)、M点溶液中的溶质质量分数是多少?
(1)、在滴加NaOH溶液过程中,原溶液中离子个数不变。(填离子符号)(2)、P点溶液中的溶质是(填化学式)。(3)、m1的值为(4)、M点溶液中的溶质质量分数是多少?四、实验探究题
-
25. 小牛同学设计如下实验(铁架台等仪器省略)制备CO2和验证CO2能与NaOH反应,(已知:HCl+NaOH=NaCl+H2O)
 (1)、仪器的名称① .(2)、装置B的作用是 .(3)、请将装置C中a、b导气管补充完整.(4)、小赵同学分析实验后,发现此装置有明显不足,至少应添加一洗气瓶F,你认为应该在(填装置编号)之间加入装有(填试剂编号)洗气瓶F.
(1)、仪器的名称① .(2)、装置B的作用是 .(3)、请将装置C中a、b导气管补充完整.(4)、小赵同学分析实验后,发现此装置有明显不足,至少应添加一洗气瓶F,你认为应该在(填装置编号)之间加入装有(填试剂编号)洗气瓶F.a.浓NaOH溶液b.澄清石灰水c.饱和NaHCO3溶液d.饱和Na2CO3溶液
(5)、打开止水夹K1 , 检查气密性,加入药品开始实验,当观察至装置E的现象是 , 可确定装置C收集满CO2 .(6)、当装置C中收集满CO2后,关闭止水夹K1 , 打开止水夹K2 , 把注射器D中的5mL浓的氢氧化钠压入到装置C中,化学方程式为 , 观察到的现象是 .(7)、小冀同学认为证明CO2与NaOH反应,还应把注射器内D中5mL浓NaOH溶液成 , 再做一次实验进行对照.26. 为研究氢氧化钠、氢氧化钡两种溶液的化学性质,进行如图所示的实验.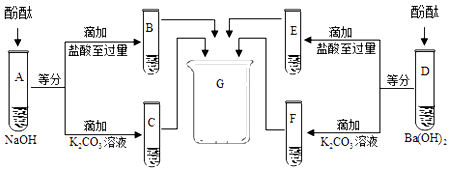 (1)、图中仪器G的名称为 .(2)、C中溶液呈性.(3)、F中沉淀的化学式是: .(4)、四支试管内的物质在G中混合后得到无色澄清溶液,其中一定含有的溶质是: , 可能含有的溶质是 .27. 同学们在验证氢氧化钙的化学性质时,分别取少量氢氧化钙溶液于四支试管中,做了以下实验:
(1)、图中仪器G的名称为 .(2)、C中溶液呈性.(3)、F中沉淀的化学式是: .(4)、四支试管内的物质在G中混合后得到无色澄清溶液,其中一定含有的溶质是: , 可能含有的溶质是 .27. 同学们在验证氢氧化钙的化学性质时,分别取少量氢氧化钙溶液于四支试管中,做了以下实验:A.
 B.
B.  C.
C.  D.
D. 
请根据实验回答下列问题。
(1)、A中观察到的现象是。(2)、C中无明显现象。为证明氢氧化钙与盐酸能发生反应,于是他们向B中滴加稀盐酸,当观察到时,说明两者发生了反应。(3)、实验结束后,同学们将上述四支试管中的物质倒入同一烧杯内,烧杯底部有白色固体,上层为有色溶液。为处理废液,过滤后,向有色滤液中加入稀盐酸,有气泡产生,继续加稀盐酸至溶液颜色恰好消失,此时溶液中的溶质为(除酚酞外)。28. 小明同学用如下实验装置探究CO2与NaOH溶液能否反应。锥形瓶中的溶液为氢氧化钠溶液或澄清石灰水(均为200mL)。
【查阅资料】
①通常状况下,1体积水能溶解1体积二氧化碳;
②CO2在酸性溶液中溶解性会大大降低,若向溶有CO2的水溶液中加入盐酸, 会将CO2从水中赶出,观察到溶液中有气泡。
(1)、小明向A装置通入的CO2气体体积V应200mL(填“>”、“<”或“=”)。(2)、A中的溶液是 , B中的溶液是 , 证明氢氧化钠溶液可以与二氧化碳反应的现象是。(3)、小红不用B装置,实验后他向锥形瓶A中的溶液中加入盐酸溶液发现有气泡产生,他判断该现象能证明二氧化碳和氢氧化钠溶液反应,你认为他的判断是否正确。小丽也不用B装置,实验后她向锥形瓶A中的溶液中加入氯化钙溶液,如出现 , 就能证明二氧化碳和氢氧化钠溶液反应。并写出相关化学方程式。