北京市朝阳区2017-2018学年中考化学二模考试试卷
试卷更新日期:2018-06-19 类型:中考模拟
一、单选题
-
1. 下列物质的性质,属于化学性质的是( )A、可燃性 B、颜色 C、密度 D、沸点2. 下列金属中,金属活动性最强的是( )A、Zn B、Al C、Ag D、Fe3. 下列方法能鉴别空气、氧气和二氧化碳3瓶气体的是( )A、闻气味 B、将集气瓶倒扣在水中 C、观察颜色 D、将燃着的木条伸入集气瓶中4. 下列符号中,表示2个氯原子的是( )A、2Cl B、2Cl- C、Cl2 D、2Cl25. 下列数据是一些物质的pH,其中酸性最强的是( )A、柠檬汁(2~3) B、酱油(4~5) C、西瓜汁(5~6) D、胡萝卜汁(6~7)6. 一种“人工固氮”的方法是:6H2O+2N2 4NH3+3O2 , 该反应属于( )A、化合反应 B、分解反应 C、置换反应 D、复分解反应7. 浓盐酸敞口放置质量减少,这说明( )A、分子的质量很小 B、分子在不断运动 C、分子间间隔变小 D、分子的体积很小8. 下列仪器中,可用作配制溶液和较大量试剂反应容器的是( )A、蒸发皿 B、量筒 C、试管 D、烧杯9. 下列不属于新能源的是( )A、潮汐能 B、太阳能 C、风能 D、石油10. 下列现象中,能用于判断铁丝燃烧是化学变化的依据是( )A、火星四射 B、放热 C、生成黑色固体 D、铁丝减少11. 甲、乙两种固体物质的溶解度曲线如图所示。下列说法正确的是( )
 A、乙的溶解度随温度的升高而增大 B、相同温度时,甲的溶解度一定大于乙的溶解度 C、将t1℃时甲的饱和溶液升温至t2℃,仍是饱和溶液 D、分别将t1℃时甲、乙的饱和溶液升温至t2℃,所得溶液中溶质的质量分数相等12. 下列图像不能正确反映其变化过程的是( )
A、乙的溶解度随温度的升高而增大 B、相同温度时,甲的溶解度一定大于乙的溶解度 C、将t1℃时甲的饱和溶液升温至t2℃,仍是饱和溶液 D、分别将t1℃时甲、乙的饱和溶液升温至t2℃,所得溶液中溶质的质量分数相等12. 下列图像不能正确反映其变化过程的是( )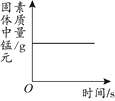


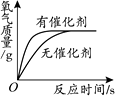
A. 加热一定质量的高锰酸钾固体
B. 向一定质量的氢氧化钠溶液中加入稀盐酸至过量
C.浓硫酸长期露置在空气中
D. 用两份等质量、等质量分数的过氧化氢溶液制取氧气
A、A B、B C、C D、D二、填空题
-
13. 铝可制成蒸锅,主要利用铝的延展性和性。14. 中草药煎制过程:①冷水浸泡 ②加热煎制 ③箅渣取液 ④灌装保存。其中属于过滤操作的是。15. 用炉灶清洁剂(主要成分NaOH)清洗炉灶时,应戴上橡胶手套,其原因是。16. “自热米饭”加热原理:生石灰与水接触放热,该反应的化学方程式为。17. 某种催化剂可将二氧化碳转化成燃料甲醇,其反应的微观示意图如下:
 (1)、在方框中补全相应微粒的图示。(2)、下列说法正确的是________。A、甲属于单质 B、乙中碳、氧元素质量比为1:2 C、丙由三种元素组成 D、反应前后分子总数不变18. 物质王国举行一场趣味篮球赛。某队由Fe、CO2、H2SO4、Ca(OH)2、CuSO4 5名“队员”组成,比赛中,场上“队员”位置及传球路线如图所示。(图中“——”表示两端物质能发生化学反应)
(1)、在方框中补全相应微粒的图示。(2)、下列说法正确的是________。A、甲属于单质 B、乙中碳、氧元素质量比为1:2 C、丙由三种元素组成 D、反应前后分子总数不变18. 物质王国举行一场趣味篮球赛。某队由Fe、CO2、H2SO4、Ca(OH)2、CuSO4 5名“队员”组成,比赛中,场上“队员”位置及传球路线如图所示。(图中“——”表示两端物质能发生化学反应) (1)、C位置“队员”所代表的物质是。(2)、写出反应②的化学方程式。19. 某小组进行了如下实验,请回答下列问题。
(1)、C位置“队员”所代表的物质是。(2)、写出反应②的化学方程式。19. 某小组进行了如下实验,请回答下列问题。序号
甲
乙
丙
实验



a、c为干燥的紫色石蕊试纸
b、d为湿润的紫色石蕊试纸
(1)、甲实验的目的是。(2)、乙实验,若电解18g 水,则试管2内得到的气体质量为g 。(3)、丙实验,说明二氧化碳密度大于空气且能与水反应的现象是。20. 某同学利用燃磷法测定空气中氧气含量,实验过程如下图所示。 (1)、该实验测得氧气的体积分数约是%。(2)、燃烧结束时,试管里剩余气体主要是(填化学式)。21. 利用下图装置完成A或B两个实验。请任选1个作答,若两题均作答,按A计分。(白磷的着火点为40℃,红磷的着火点为240℃)
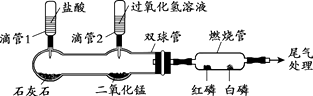
(1)、该实验测得氧气的体积分数约是%。(2)、燃烧结束时,试管里剩余气体主要是(填化学式)。21. 利用下图装置完成A或B两个实验。请任选1个作答,若两题均作答,按A计分。(白磷的着火点为40℃,红磷的着火点为240℃)A
B
挤压滴管1,一段时间后,加热燃烧管至240℃以上。
⑴双球管中发生反应的化学方程式为。
⑵燃烧管中白磷和红磷均不燃烧,其原因是。
挤压滴管2,一段时间后,微热燃烧管至80℃。
⑴双球管中发生反应的化学方程式为。
⑵得出可燃物燃烧需要温度达到着火点的结论,对应的现象是。
三、科学探究题
-
22. 阅读下面科普短文。
“菠菜豆腐”是我国的传统菜肴,近年来,有关“菠菜豆腐”的争论主要集中在钙吸收率方面。菠菜中富含易溶于水的草酸,若单独吃菠菜,其中的草酸会结合胃内食糜中的部分铁和锌,还能够进入血液,沉淀血液中所含的钙。而将豆腐与菠菜同食,豆腐中的可溶性钙与菠菜中的草酸结合成不溶性的草酸钙(CaC2O4)沉淀,既能够保护食物中的铁和锌等元素,还能保证人体内的钙不被草酸结合。因此,豆腐与菠菜同食仍不失为一个好的搭配。
研究人员以新鲜菠菜和新鲜豆腐为材料,进行了“菠菜豆腐”烹调方法的研究。
(实验1)探究菠菜质量对菜肴中可溶性钙含量的影响。实验结果如下:
豆腐/ g
10
10
10
10
10
菠菜/ g
5
10
15
20
25
可溶性钙/总钙
0.364
0.287
0.186
0.125
0.088
(实验2)探究菠菜焯水时间对菜肴中可溶性钙含量的影响。
用100g豆腐和250g菠菜(焯水时间不同)制成菜肴,测定每100g“菠菜豆腐”中可溶性钙的质量,结果见下图。
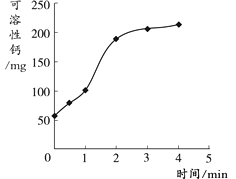
以上研究表明,烹调“菠菜豆腐”时,如能适当减少菠菜的比例,并预先将菠菜焯水,则豆腐中钙的吸收率将会显著提高。
根据文章内容,回答下列问题:
(1)、可溶性钙中的“钙”是指(“钙单质”或“钙元素”)。(2)、豆腐中富含的营养素是_____________。A、维生素 B、糖类 C、蛋白质 D、油脂(3)、结合实验1的数据分析,可得到的结论是。(4)、用焯水后的菠菜制作“菠菜豆腐”,能提高可溶性钙含量的原因是。(5)、草酸钙在高温下完全分解可得到两种气态氧化物和一种固态氧化物,该反应的化学方程式为。23. 小明发现生物老师将一勺白色粉末加入鱼缸后,水中有气泡产生,奄奄一息的鱼很快就活蹦乱跳,于是对这种“白色粉末”产生兴趣,与小刚一起进行了相关探究。(1)、实验准备①查阅资料:白色粉末的主要成分是过碳酸钠(Na2CO4),常温下与水反应生成氧气。
②用一定溶质质量分数的NaOH和Na2CO3两种溶液进行如下实验。
NaOH溶液
Na2CO3溶液
滴加酚酞溶液
溶液变红色
溶液变红色
加入稀盐酸
无明显现象
现象Ⅰ
加入澄清石灰水
无明显现象
现象Ⅱ
加入 1%的CaCl2溶液
溶液变浑浊
溶液变浑浊
加入 0.1%的CaCl2溶液
无明显现象
溶液变浑浊
表中的现象Ⅰ为 , 现象Ⅱ对应的化学反应方程式为。
(2)、实验过程实验1:检验气体
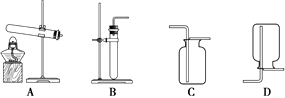
小明用白色粉末和水反应制取并收集产生的气体时,应选用的装置是(填序号)。 经检验该气体是氧气。
实验2:检验反应后溶液中的溶质成分
【猜想假设】小明猜想:Na2CO3 小刚猜想:Na2CO3和NaOH
【进行实验】小明取实验1反应后的溶液于试管中,滴加1%的CaCl2溶液,观察到有白色沉淀生成,认为自己的猜想正确。
【表达交流】①小刚对小明的实验方案提出质疑,他的理由是。
②为了证明小明的猜想是否正确,你的实验方案是。
(3)、反思拓展根据上述探究可知,保存该白色粉末时应注意。
四、流程题
-
24. MnCO3用作涂料和清漆的颜料。MnCO3不溶于水,100℃时开始分解。以软锰矿(主要成分MnO2)为原料制备高纯MnCO3的流程如下:
 (1)、反应塔1中的反应为:MnO2+SO2=MnSO4 , 其中化合价发生改变的元素是。(2)、洗涤塔中喷水的目的是。(3)、烘干塔中需选择“低温”干燥的原因是。(4)、上述流程中的产品除高纯MnCO3外,还有。
(1)、反应塔1中的反应为:MnO2+SO2=MnSO4 , 其中化合价发生改变的元素是。(2)、洗涤塔中喷水的目的是。(3)、烘干塔中需选择“低温”干燥的原因是。(4)、上述流程中的产品除高纯MnCO3外,还有。五、实验题
-
25. 利用下图装置进行实验。实验前K1、K2均已关闭。
实验装置
实验1
实验2

Ⅰ. A中盛有水,液面浸没下端导管口,B中盛有含酚酞的NaOH溶液
Ⅱ.将注射器中的浓硫酸注入A中,并保持注射器活塞不动,充分接触后,打开K1和K2
Ⅰ. A中充满CO2 , B中盛有一定量的水
Ⅱ. 将注射器中的NaOH溶液(足量)注入A中,充分反应后,打开K1和K2
(1)、检查A装置气密性:向下推注射器的活塞,松手后活塞恢复至原位,该现象说明。(2)、实验1观察到A中液体流入B中,B中溶液由红色变成无色,产生该现象的原因是。(3)、实验2不能证明二氧化碳与氢氧化钠发生反应,其理由是。
-